
36.(36分)北京时间2009年10月3日凌晨,国际奥委会第121次全会在丹麦哥本哈根举行.在2010年夏季奥运会主办地票选里,巴西里约热内卢通过三轮投票击败西班牙马德里,获得2016年第31届夏季奥林匹克运动会的举办权,这也是奥运会首次登陆南美大陆。下图为9月初国际奥委会公布的四个候选城市。结合所学知识回答问题。
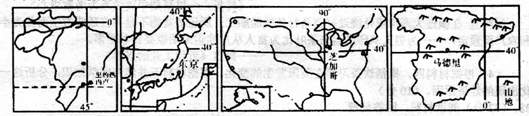
(1)据图分析里约热内卢在四个城市中的地理位置的独特性。(6分)
(2)常以“二三月如冰九月如烘”来形容马德里的气候特点。试分析其形成原因。(4分)
(3)里约热内卢所在国家,有世界上流量最大的河流,简析其成因.并评价其航运价值的大小。(18分)
(4)结合插图和所学知识分析东京、芝加哥所在国家农业生产规模的特点及其机械化发展方向。(8分)
29.(14分)有A、B、C、D四种可溶于水的电解质,它们在溶液中电离出的阴、阳离子分别是以下两组离子中的各一种(每种离子只出现一次)。
|
阳离子 |
Ag+ |
NH4+ |
Mg2+ |
Cu2+ |
|
阴离子 |
Cl– |
OH– |
SO42– |
NO3– |
现进行下列实验:将B的溶液分别加到A、D两溶液中均产生稳定的白色沉淀;C、D两溶液适量混合产生蓝色沉淀,C中阳离子与阴离子的质量比为2∶3。
据此回答下列问题:
(1)推断出四种电解质的化学式:
A_______________,B________________,C_____________,D________________。
(2)将D溶液逐滴滴加在A溶液中的现象为:
________________________________________________________________________。
(3)C、D两溶液反应产生蓝色沉淀的离子方程式为:
________________________________________________________________________。
28.(15分)有机物A(C10H20O2)具有兰花香味,可用做香皂、洗发香波的芳香赋予剂。已知:
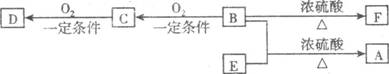
①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯原子取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有___________________(选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是________________、_________________。
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:
_________________________________________________________________。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2─甲基─1─丙醇和甲酸在一定条件下制取E。该反应的化学方程式为:
__________________________________________________________________________。
27.(16分)A、B、C、D、E、F、G、H、J、K等为中学化学常见的物质,其中C、D为非金属单质,F、G、H为金属单质,A的稀溶液呈蓝色,常温下B为无色无味的液体,K是一种污染大气的气体。物质之间的转化关系如图所示,部分反应物、产物及反应条件未标出。
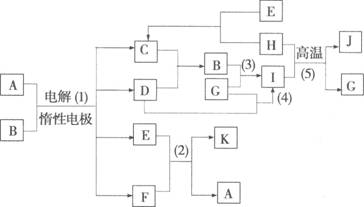
(1)请写出下列物质的化学式:
A____________,D___________,F____________,I_____________,K___________。
(2)G在周期表中的位置:在第__________周期__________族。
(3)请写出电解(1)中阳极产物_________;阴极产物___________。
(4)请写出下列几个反应的化学方程式:
反应(2)____________________________________________________________;
反应(3)____________________________________________________________;
反应(5)______________________________________________________________。
(5)通过反应(5)制备1 mol G转移的电子的物质的量为_______________。
26.(15分)某课外研究小组作了如下关于钾的探究实验。
(1)钾与水反应
实验中钾常会着火燃烧,并发生轻微爆炸,由此现象可以得出的结论是:
_________________________________________________________________(任写一个),该反应的离子方程式为___________________________________________________。
(2)钾与氯气反应
该实验所需要氯气可以选用如下方案进行制备,其中最合理的是_____________。
|
方案序号 |
制备所用试剂 |
净化剂 |
干燥剂 |
|
A |
MnO2、稀盐酸 |
饱和食盐水 |
浓硫酸 |
|
B |
Ca(ClO)2、浓盐酸 |
饱和食盐水 |
无水硫酸铜 |
|
C |
氯酸钾、浓盐酸 |
饱和碳酸钠溶液 |
浓硫酸 |
|
D |
高锰酸钾、浓盐酸 |
水 |
碱石灰 |
你所选取的最合理方案中一定会用到的仪器是____________。
a.长颈漏斗 b.圆底烧瓶 c.酒精灯 d.洗气瓶
(3)钾与氧气反应实验
经查找资料得:钾与氧气反应可能生成氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)。
 ①取一定量钾在空气中点燃,使其充分反应。
①取一定量钾在空气中点燃,使其充分反应。
②将生成物研成细粉备用。
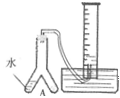
③常温常压下,利用如图所示装置探究生成物成分及含量。
据此回答如下问题:
①引发粉末与水反应的操作是:__________________________________________________。
②测量气体体积时应注意的事项是:_______________________________________________
_____________________________________________________________________________。
③若钾与氧气燃烧产物为K2O2、KO2,取该燃烧产物3.94 g进行上述实验,测得气体的体积为868.0 mL,则超氧化钾的质量分数为___________(已知:常温常压下,气体的摩尔体积为24.8 l/mol)。
13.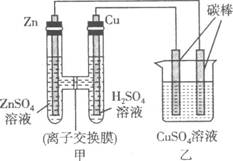 如图所示,甲、乙为原电池或电解池。接通线路使其工作一段时间(假设所提供的电能可以保证电解反应的顺利进行),下列有关说法错误的是( )
如图所示,甲、乙为原电池或电解池。接通线路使其工作一段时间(假设所提供的电能可以保证电解反应的顺利进行),下列有关说法错误的是( )
A.甲是原电池,乙是电解池
B.甲池中的离子交换膜只允许SO42–通过
C.乙池中左侧碳棒做阳极,该侧的电极反应式为:Cu2+ + 2e– = Cu
D.若甲池中有0.1 mol Zn参加反应,则乙池中必有0.1 mol Cu析出
第Ⅱ卷 ( 非选择题 共60分 )
12.利尿剂是2008年北京奥运会违禁药物,顾名思义,此类药物有稀释尿液的功能。某种利尿剂的结构如下图所示:
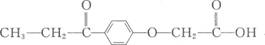
下列有关叙述正确的是( )
A.从结构上看该物质是一种酯 B.该物质的分子式是C11H12O4
C.该物质遇FeCl3溶液显色 D.该物质分子中位于同一平面内的原子最多有10个
11.某条件下,在容积固定为1 L的密闭容器中充入2 mol N2O5发生反应:
 2 N2O5(g)
4 X(g) + O2(g);△H = + 56.7 kJ/mol
2 N2O5(g)
4 X(g) + O2(g);△H = + 56.7 kJ/mol
4 min后达到平衡,测得N2O5的转化率为10%,下列有关叙述中不正确的是( )
A.X为一种常温下呈红棕色的气体
B.升高温度N2O5的转化率增大
C.4 min内用X浓度变化表示的平均反应速率为0.1 mol/(L•min)
D.达到平衡时,共有2 mol电子发生转移
10. 下列方程式书写方法正确的是( )
下列方程式书写方法正确的是( )
A.高温煅烧石英和纯碱的混合物:SiO2 + Na2CO3 Na2SiO3 + CO2↑
B.过量SO2通入到Ba(NO3)2溶液中:
3SO2 + 2NO3– + 3Ba2+ + 2H2O = 3BaSO4↓ + 2NO + 4H+
C.少量的Cl2通入到FeI2溶液中:2Fe2+ + Cl2 = 2Fe3+ + 2Cl–
D.金属Na投入到CuSO4溶液中:2Na + Cu2+ = 2Na+ + Cu
9.下表数据是对应物质的熔点,据此作出的下列判断中错误的是( )
|
化合物 |
Na2O |
CO2 |
SiO2 |
Al2O3 |
|
熔点/℃ |
920 |
–57 |
1723 |
2073 |
|
化合物 |
NaCl |
MgCl2 |
AlCl3 |
AlF3 |
|
熔点/℃ |
801 |
714 |
190 |
1291 |
A.同族元素的氧化物可形成不同类型的晶体
B.不同族元素的氧化物可形成相同类型的晶体
C.铝与活泼非金属形成的化合物都是离子晶体
D.MgO熔点可能高于714℃
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com