
31.(18分)微生态活性制剂是近几年迅速发展起来的新型绿色添加剂,能改善虾体肠道微生态环境,促进虾体生长。有人通过实验对芽孢杆菌制剂对凡纳对虾生长和消化酶活性的影响进行了研究,请利用所给材料和用具完成以下实验并回答相关问题。
实验材料和用具:
体重接近的健康凡纳对虾200尾;颗粒饲料;混有0.5%、1.0%、3.0%和5.0%芽孢杆菌制剂的颗粒饲料;70cm×70cm×100cm水池若干(流水养殖,培养时间为一个月);电子天秤
(1)课题名称:
(2)实验步骤:
①将凡纳对虾随机分为 组,每组 ,称取每只虾的重量后分别置于70cm×70cm×100cm水池中,流水养殖。
②对照每组每天饲喂适量的不添加芽孢杆菌制剂的颗粒饲料,实验组每天相同时间饲喂 颗粒饲料。
③在相同且适宜条件下培养一个月后, ,记录并求出平均值。
(3)研究人员利用一定的方法对上述实验中凡纳对虾肠道内三种消化酶活性进行测定。结果如下图所示:
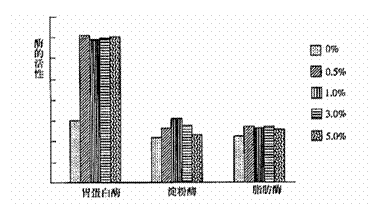

从上图可以得出的结论是① ,② ;对胃蛋白酶来说,
浓度的芽孢杆菌制剂最有利于凡纳对虾生长和降低生产成本。
(4)芽孢杆菌进入虾肠后能够调节对虾肠道微生物菌群结构,保护虾肠道免受毒害,芽孢杆菌与凡纳对虾肠道内其他微生物之间的关系是 。
(5)在实验室中纯化芽孢杆菌常用的两种方法是 。
30.(16分)下图是患甲病(显性基因为A,隐性基因为a)和乙图(显性基因为B,隐性基因为b)两种遗传病的系谱图。现已查明II-3不携带致病基因。据图回答:
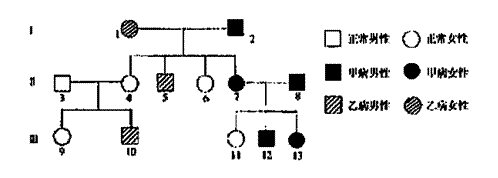

(1)甲病的致病基因位于 染色体上,乙病是 性遗传病。
(2)写出下列个体的基因型:III-9 ,III-12 。
(3)若III-9和III-12婚配,子女中只患甲或乙一种遗传病的概率为 ;同时患两种遗传病的概率为 。
(4)若III-9和一个正常男性婚配,如果你是医生,根据他们家族病史,你会建议他们生一个 (男/女)孩。
(5)若乙病在男性中的发病率为6%,在女性中的发病率约为 。
29.(16分)图1表示细胞代谢的某些过程,图2表示光照强度与二氧化碳吸收量的关系。请据图回答问题:(图中数字代表物质,a、b、c代表细胞器)


图1 图2
(1)图1中a、b、c的结构名称依次是 。
(2)图1中物质④的名称是 ,葡萄糖→③过程中还能产生的物质是 。
(3)光合作用暗反应阶层的场所是图1[ ]中的 。
(4)将植物置于完全黑暗条件下24小时后,给植物提供H218O,继续置于黑暗条件下,一段时间后除水外还能在 (填物质名称)中检测到18O。
(5)若该细胞是成熟的叶肉细胞,其吸收水分的主要方式是 。
(6)在温度、水分适宜的条件一,图2BC投限制作物增产的主因素是 ,若要进一步提高温室中农作物的产量,具体可行的措施是 (从以下选项中选出所有合理答案)
A.施用NH4HCO3 B.增加光照强度 C.使用CO2发生器
D.施农家肥 E.与鸡(猪)舍连通 F.开窗通风
28.(16分)肉桂醛在食品、医药化工等方面都有应用。
(1)质谱分析肉桂醛分子的相对分子质量为132。其分子中碳元素的质量分数为81.8%,其余为氢和氧。分子中的碳原子数等于氢、氧原子数之和。肉桂醛的分子式是
。
(2)肉桂醛具有下列性质:


请回答:
①肉桂醛是苯的一取代物,核磁共振氢谱显示,苯环侧链上有三种不同化学环境的氢原
子,其结构简式是 。(本题均不考虑顺反异构与手性异构)
②Z不能发生的反应类型是 。
A.取代反应 B.消去反应 C.加成反应 D.加聚反应
③Y与乙醇在一定条件下作用得到肉桂酸乙酯,该反应的化学方程式是 。
④Y的同分异构体中,属于酯类目苯环上只有一个取代基的同分异构体有 种。
其中任意一种的结构简式是 。
(3)已知
I.醛与醛能发生反应,原理如下:


II.合成肉桂酸醛的工业流程如下图所示,其中甲烷。
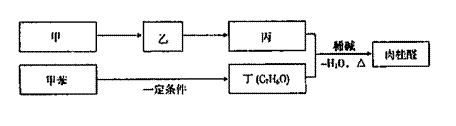

请回答:
①甲的结构简式是 。
②丙和丁生成肉桂的化学方程式是 。
③醛和酯也可以发生如“I”的反应。食用香料肉桂酸乙酯通过如下反应合成:


戊的名称是 。
27.(14分)铜及其化合物在生产、生活中有广泛的应用。
(1)铜可采用如下方法制备:

火法炼铜:Cu2S+O2 2Cu+SO2
湿法炼铜:CuSO4+Fe=====FeSO4+Cu-
上述两种方法中,铜元素均被 (填“氧化”或“还原”)成铜单质。
(2)印刷电路板上使用的铜需要回收利用。
方法一:用FeCl3溶液浸泡印刷电路板制备CuCl2·2H2O,实验室模拟回收过程如下:


①证明步骤I所加FeCl3溶液过量的方法是 。
②步骤2中所加的氧化剂最适宜的是 。
A.HNO3 B.H2O2 C.KMnO4
③步骤3的目的是使溶液的pH升高到4.2,此时Fe3+完全沉淀,可选用的“试剂1”是 。(写出一种即可)
④蒸发农缩CuCl2溶液时,要滴加浓盐酸,目的是 (用化学方程式并结合简要的文字说明),再经冷却、结晶、过滤,得到CuCl2·2H2O。
方法二:用H2O2和稀硫酸共同浸泡印刷电路板制备硫酸铜时,其热化学方程式是:
Cu(s)+H2O2(l)+H2SO4(nq)=====CuSO4(aq)+2H2O(l)△H1=-320kJ/mol
又知:2H2O(l)====2H2O(l)+O2(g) △H2=-196kJ/mol
H2(g)+ O2(g)====H2O(l)
△H3=-286kJ/mol
O2(g)====H2O(l)
△H3=-286kJ/mol
则反应Cu(s)+H2SO4(aq)====CuSO4(aq)+H2(g)的△H= 。
(3)欲实现反应Cu+H2SO2====CuSO4+H2,在你认为能实现该转化的装置中的括号内,标出电极材料(填“Cu”或“C”)
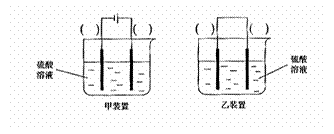

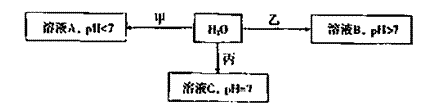
25.(14分)已知X+、Y3+、Z-、W2-是短周期元素X、Y、Z、W形成的离子,下图中的甲、乙、丙均是由上述四种离子中的两种组成的化合物。

回答下列问题:
(1)通常状况下,Z的单质是一种黄绿色气体,工业上常用电解溶液C的方法制备该单质,制备反应的化学方程式是 。
(2)①甲的化学式是 ,乙的化学式可能是 (写一种即可)
②若将溶液A与溶液B混合,产生白色沉淀,则该反应的离子方程式是 。
若W2和Z-具有相同电子层结构,则乙的电子式是 。
(3)Y单质可用来制造Y-空气燃料电池,该电池通常以溶液C或氢氧化钾溶液为电解质溶液,通入空气的电极为正极。
①若以溶液C为电解质溶液时,正极的反应式为 。
②若以氢氧化钾溶液为电解质溶液时,电池的总反应式为 。
O2 O2 O2 H2O
NH3 NO 吸收塔
某课外小组模拟上述部分过程设计了如下实验装置制备硝酸(所有橡胶制品均已被保护)


(1)工业上用氨气制取NO的化学方程式是 。
(2)连接好装置后,首先进行的操作是 。
(3)通入a气体的目的是 .
(4)盛有Na2CO3溶液的烧杯为尾气处理装置,该装置中发生反应的化学方程式是
2NO2+Na2CO3=====NaNO2+ +
(5)已知:温度低于21.15°C时,NO2几乎全部转变为N2O2。工业上可用N2O4与水反应来提高硝酸产率。N2O4与a气体在冷水中生成硝酸的化学方程式是 。
 (6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=
。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为
。
(6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K=
。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为
。
24.(20分)
如图所示为一种获得高能粒子的装置。环形区域内存在垂直纸面向外,大小可调的匀强磁场。M、N为两块中心开有小孔的极板,每当带电粒子经过M、N板时,都会被加速,加速电压均为U;每当粒子飞离电场后,M、N板间的电势差立即变为零。粒子在M、N间的电场中一次次被加速,动能不断增大,而绕行半径R不变(M、N两极板间的距离远小于R)。当t=0时,质量为m,电荷量为+q的粒子静止在M板小孔处,
(1)求粒子绕行n圈回到M板时的动能En;
(2)为使粒子始终保持在圆轨道上运动,磁场必须周期性递增;求粒子绕行第n圈时磁感应强度B的大小;
(3)求粒子绕行n圈所需总时间tn。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com