
20.反应4A(g) +5B(g) 4C(g)+6D(g)在5L的密闭容器中进行反应,30
min后,C的
4C(g)+6D(g)在5L的密闭容器中进行反应,30
min后,C的
物质的量增加了0.30 mol。下列叙述正确的是
A.30 min 中A的平均反应速率是0.010 mol•L-1•s-1
B.容器中含D的物质的量为0.45 mol
C.容器中A、B、C、D的物质的量的比一定是4∶5∶4∶6
D.容器中A的物质的量一定增加0.30 mol
第II卷(非选择题,共60分)
19.下列除去杂质的方法正确的是
A.除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离
B.除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏
C.除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶
D.除去乙醇中少量的水:加足量生石灰,蒸馏
18.下列有机化学方程式书写正确的
A.
B.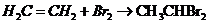
|
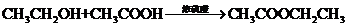
D.
17.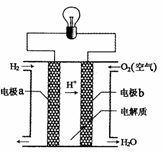 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法正确的是
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法正确的是
A.该电池工作时电能转化为化学能
B.通入氢气的一极是负极
C.外电路中电子由电极b通过导线流向电极a
D.该电池的总反应:2H2+O2=2H2O
16.根据下表中的数据,结合学过的化学知识,判断下列说法正确的是
|
物质 |
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
沸点/℃ |
1465 |
1412 |
181(升华) |
57.6 |
A.以上四种物质中,只有SiCl4是共价化合物
B.若上述数据变化规律具有普遍性,则可预测:LiCl 的沸点大于BCl3的沸点
C.因为AlCl3的沸点低,所以工业上可用电解熔融AlCl3制备Al
D.据上述数据,可判断NaCl、MgCl2为分子晶体
15.下列说法正确的是
A.在周期表中金属和非金属的分界处寻找催化剂和耐高温、耐腐蚀的合金材料
B.元素性质随着核电荷数的递增而呈周期性的变化叫元素周期律
C.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
D.相对分子质量相同,而结构不同的化合物互称为同分异构体
14. X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是
A.X的气态氢化物比Y的稳定
B.Z的非金属性比Y的强
C.W的最高价氧化物对应水化物的酸性比Z的强
D.X与Y形成的化合物都能与水反应
13.下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是
A.a原子的最外层电子数比b原子的最外层电子数少
B.a原子电子层数比b原子的电子层数多
C.1mol a 从酸中置换H+生成的H2比1 mol b从酸中置换H+生成的H2多
D.常温时,a能从水中置换出氢,而b不能
12.NA代表阿伏加德罗常数,下列说法中不正确的是
A.100 mL 0.5 mol/L的乙酸溶液中,乙酸分子的数目小于0.05 NA
B.标准状况下,22.4 L水中所含有的分予数为NA
C.0.8 mol乙烷中含4.8 NA个氢原子
D.用惰性电极电解氯化铜溶液时,若阴极增重64g,则以石墨棒为阳极能产生NA个氯气分子
11.下列各组物质的晶体中,化学键类型和晶体类型都相同的是
A.CO2和H2O B.NaOH和CH4
C.SiO2和CO2 D.NaCl和HCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com