
5、近年来,以历史为题材的电视剧持续热播。下列剧情有违史实的是:①《隋唐英雄传》中隋灭陈的战争场景炮声雷动 ②《大宋提刑官》中内阁大学士位高权重 ③《康熙大帝》中军机大臣跪奏笔录 ④《台湾1895》中的李鸿章说出“八国联军刚刚火烧了圆明园”的台词
A.②③④ B.①③④ C.①②③ D.①②③④
4、唐朝科举制规定“考核资叙郡县乡里名籍,父祖官名,内外族姻……(严禁)刑家之子,工商殊类(应试)” 该材料说明唐朝科举考试
①有一定的资格限制 ②以门第出身为标准
③体现了统治者重农抑商的观念 ④不利于扩大统治基础
A.①②④ B.①②③ C.①③ D.②④
3.斯塔夫里阿诺斯在《全球通史》中说:“在中国长达数千年的历史上,有过三次大革命,它们从根本上改变了中国的政治和社会结构。第一次发生于公元前221年……第二次发生于1911年……第三次在1949年”。第一次“革命”是指
A.中央集权制度建立 B.世袭制度确立
C.宗法式家族制度形成 D.世卿世禄制度确立
2、“它排除了丞相个人专断,相权过大威胁皇权而出现的政治危机,而且增强了决策施政的程序性和合理性,提高了行政效率。”材料中的“它”是指
A.西汉郡国并行制度 B.唐朝三省六部制度
C.元朝的行省制度 D.明朝的内阁制度
1、在近代史学大师王国维看来,周革殷命是一次非常重要的鼎革,“中国政治与文化之变革,莫剧于殷、周之际”。下列从制度文化的角度历数殷周鼎革的“剧变”的有
①封邦建国 ②加强中央集权 ③嫡长子继承制 ④百家争鸣
A.①②④ B. ①③④ C. ①③ D.②④
22.(8分)实验室里常用浓盐酸跟高锰酸钾反应来制取少量氯气,反应的化学方程式为:2KMnO4 + 16HCl(浓)== 2KCl + 2MnCl2 + 5Cl2↑+ 8H2O
现用1L密度为1.19g/cm3、质量分数为36.5%的浓盐酸与一定质量的高锰酸钾反应,产生的氯气在标准状况下的体积为1.12L。
(1)计算反应中被氧化的HCl的物质的量。
(2)计算反应后溶液中H+的物质的量浓度。
高二新课程实施教学质量调研抽测
21、(16分)铁是人类较早使用的金属之一。运用铁的有关知识,回答下列问题:
(1)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,形成该分散系的微粒大小范围是 nm
(2)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式
。
检验反应后的溶液中还存在Fe3+的试剂是
(3)欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,现有下列试剂:①蒸馏水
②铁粉③浓硝酸④浓盐酸⑤烧碱⑥浓氨水⑦氯气,需要用到的试剂是 (填序号)
整个实验过程中涉及到的离子方程式
、
、 、
、
20.(13分)某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(C1O)2+CaCl2+H2SO4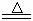 2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质。
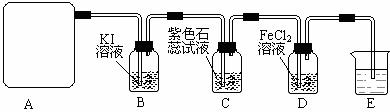
试回答下列问题:
(1)每生成1 mol Cl2,上述化学反应中转移的电子个数为______ (NA表示阿伏加德罗常数)。
(2)该实验中A处可选用装置__________ _____ (填写装置的序号)。

(3)装置B中发生反应的离子方程式为________________________________________。
(4)装置C中的现象为___________________________________________________,
试结合反应方程式解释其原因 __________________________________ _
_________________________________ 。
(5)装置E中的试剂是______________(任填一种合适试剂的名称),其作用是________
_______________________________ ______。
(6)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验步骤)
_________________________________________________________________________
___________________________________________________ ______________
19.(18分)(1)标准状况下,44.8L的NH3气体质量为 g,其中含 个氮原子,其中含 mol 氢原子。
(2)标准状况下,11.2L的H2R气体质量为17g,则H2R的摩尔质量是 ,等质量的NH3与H2R的物质的量比为 ,1.7g氨气与 mol H2O含有的电子数相等。
(3)过氧化钠几乎可与所有的常见气态非金属氧化物反应。如:
2Na2O2 + 2CO2 = 2Na2CO3 + O2 ; Na2O2 + CO = Na2CO3
试分别写出Na2O2与SO2、SO3反应的化学方程式:
(4)取黄豆粒大小的一块金属钠,用滤纸擦干其表面的煤油,然后加入到硫酸铜溶液中,观察实验现象并写出相关的化学方程式:
①实验现象
②有关的化学方程式是 。
。
18.在实验室中,对下列事故或药品的处理正确的是
A、漂白粉长期放置在烧杯中
B、金属钠着火燃烧时,不能用泡沫灭火器灭火,应该用沙子灭火
C、氯水可以用无色透明的试剂瓶盛装保存
D、有大量的氯气泄漏时,用氢氧化钠溶液浸湿软布蒙面,并迅速离开现场
高二新课程实施教学质量调研抽测
化 学
第Ⅱ卷 非选择题(共55分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com