
3.下图四个典型的被“火车拉来的城市”依次是:石家庄、株洲、郑州、宝鸡,其中表示正确是( )
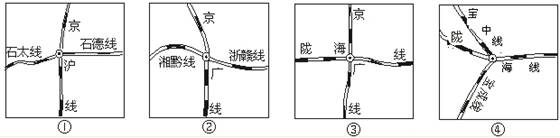 A.①石家庄 ②株洲 ③郑州 ④宝鸡
A.①石家庄 ②株洲 ③郑州 ④宝鸡
B.①石家庄 ②郑州 ③株洲 ④宝鸡 C.①郑州 ②石家庄 ③宝鸡 ④株洲
D.①石家庄 ②株洲 ③宝鸡 ④郑州
2.在节能减排中,公众可参与有利于抑制全球变暖的行动是 ( )
A.充分利用太阳能;尽量使用公共交通工具
B.采用节水措施;开发利用无污染能源
C.多种水稻;充分利用风能
D.维持能源消费结构现状;自备购物
1.对全球变暖的环境影响,叙述正确的是 ( )
A.北半球热带地区降水减少;海平面上升
B.灾害性天气频繁,中国自然带北移
C.洋流发生变化;大部分动物栖息地发生根本本性改变
D.北欧影响最大:北半球亚热带地区降水增多
26.(6分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
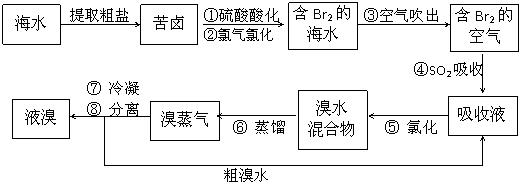

(1)步骤①中用硫酸酸化可提高Cl2的利用率,为什么? 。
(2)步骤④的离子方程式:________________________________________。
(3)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离,分离仪器的名称是_____________。
(4)提取时要经过“空气吹出、SO2吸收、氯化”的过程的目的是: 。
福州八县(市)协作校2009-2 010学年第二学期期末联考
010学年第二学期期末联考
25.(10分)为讲授“氯气的性质和用途”,某老师利用二氧化锰和浓盐酸为主要原料,设计一套如图所示的实验装置(其中A是连有注射器针头的 橡皮管,针头已插入并穿过橡皮塞)进行教学。试回答下列问题:
橡皮管,针头已插入并穿过橡皮塞)进行教学。试回答下列问题:
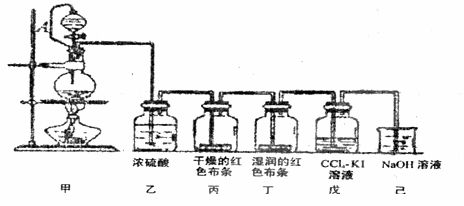
(1)甲中烧瓶发生反应的化学方程式为 。
(2)丙中的现象是 ;
己中的离子方程式:______________________________;。
(3)利用橡皮管将分液漏斗上端与烧瓶连通,其作用是 。
(4)已知氯气与冷水反应的化学方程为Cl2 + H20 = HCl + HClO。
①你认为使有色布条褪色的物质是 。
②为探究其生成物的漂白性,请设计简单的实验加以证明,写出实验的操作方法、现象和结论。
24.(8分)氯气及氯的化合物有着广泛的应用
 (1)已知可逆反应Cl2+H20 HCl+HClO,向氯水中加入NaHCO3固体后,溶液中HClO的浓度 (填增大、减小、不变),原因是:
。
(1)已知可逆反应Cl2+H20 HCl+HClO,向氯水中加入NaHCO3固体后,溶液中HClO的浓度 (填增大、减小、不变),原因是:
。
(2)我国卫生部已明确提出:逐步用二氧化氯替代氯气进行饮用水的消毒。
①用ClO2处理过的饮用水(pH为5.5-6.5)常含有一定量对人体不利的亚氯酸根离子(ClO2-)。卫生部规定,饮用水中ClO 2-的含量应不超过0.2mg·L-1 。当pH≤2.0时, ClO2-能被I-还原成Cl-。请写出反应的离子方程式
。
2-的含量应不超过0.2mg·L-1 。当pH≤2.0时, ClO2-能被I-还原成Cl-。请写出反应的离子方程式
。
②用ClO2处理过的自来水中会残留ClO2 ,可用FeCl2将ClO2还原为Cl-,该反应的氧化产物是 (填化学式)。现用V L(已换算为标准状况)ClO2处理一定量自来水,再加入a mol FeCl2可将残留的ClO2恰好除去。则该自来水中残留ClO2的物质的量为 mol。
23.(6分)通常用盛有饱和NaHCO3溶液的洗气瓶来除去混杂在CO2中的HCl气体,写出反应的化学方程式
;不允许采用NaOH溶液的原因是(用离子方程式表示) ;也不允许采用饱和Na2CO3溶液的原因是(用离子方程式表示)
。
22.(6分)实验室用高锰酸钾和浓盐酸反应制取氯气:K^S*5U.C#O
KMnO4+ HCl - Cl2↑+ MnCl2+ KCl+ H2O
(1)配平上述的反应方程式,并标出电子转移的方向和数目(用双线桥)
(2)其中还原剂是_______。若消耗0.1 mol氧化剂,则被氧化的还原剂的物质的量是____mol。
21.(4分)(1)3.4克NH3含质子的物质的量为 ,该气体在标准状况下的体积是 。
(2)已知500mL
Al2(SO4)3溶 液
液 中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为 mol/L,取上述溶液50mL加水到150mL,此溶液中SO42-的物质的量浓度为 mol/L。
中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为 mol/L,取上述溶液50mL加水到150mL,此溶液中SO42-的物质的量浓度为 mol/L。
20.某无色溶液中只可能含有Na+ 、Ba2 +、 Cl一、 Br一、SO32一、SO42一,对该溶液进行下列实验,实验操作和现象如下表:
|
步骤 |
操 作 |
现 象 |
|
(1) |
取少量溶液滴加几滴石蕊试液 |
溶液变蓝 |
|
(2) |
另取少量溶液滴加过量氯水,再加入CCl4振荡,静置 |
上层无色,下层呈橙红色 |
|
(3) |
取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3, 过滤 过滤 |
有白色沉淀产生 |
|
(4) |
向(3)的滤液中加入过量AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是( )
A.可能含有 Cl一、 SO32一、SO42一 B.肯定没有 Ba2 +、Cl一、Br一
C.不能确定 Na+ 、 SO32一、SO42一 D.肯定含有 Na+、 Br一、SO32一
第Ⅱ卷(非选择题,共40分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com