
13. 氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是
A.1mol/L氢氰酸溶液的pH约为5
B.HCN易溶于水
C.10mL 1mol/L HCN恰好与10mL 1mol/L NaOH溶液完全反应
D.在相同条件下,HCN溶液的导电性比盐酸溶液弱
12.氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,c(H+) / c(ClO-) 减小
B.通入少量SO2,溶液的漂白性增强
C.加入少量水,水的电离平衡向正反应方向移动
D.加入少量固体NaOH,一定有c(Na+) = c(Cl-)+c(ClO-)
11.对可逆反应4NH3(g) +5O2(g)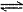 4NO(g)+ 6H2O(g),下列叙述正确的是
4NO(g)+ 6H2O(g),下列叙述正确的是
A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(NH3):n(O2)=4:5
B.反应达到平衡后,对体系一直进行加压,平衡总是逆向移动
C.反应达到平衡时,若向压强固定的密闭容器中充入稀有气体,平衡不移动
D.当v正(NH3):v正(NO) = l:1时,说明该化学反应已经达到平衡
10.关于浓度均为0.1 mol/L的三种溶液:①氨水 ②盐酸 ③氯化铵溶液,下列说法
不正确的是
A.c(NH4+):③>①
B.水电离出的c(H+):②>①
C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O)
D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
9. 以下说法中正确的是
A.pH=2的酸溶液稀释100倍后溶液的pH=4
B.c(NH4+)相等的(NH4)2SO4溶液与(NH4)2S溶液中:c[(NH4)2SO4]< c[(NH4)2S]
C.25℃时纯水的pH低于100℃时纯水的pH
D.pH=3的硫酸物质的量浓度是pH=3的醋酸物质的量浓度的0.5倍
8. 用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是
A.c(NH3•H2O)/c(OH-) B.c(H+)
C.c(H+)和c(OH-)的乘积 D.OH-的物质的量
7.25 ℃时,浓度均为0.2 mol/L的NaHCO3和Na2CO3溶液中,下列判断不正确的是
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.c(OH-)前者大于后者
D.分别加入NaOH固体,恢复到原温度,c(CO32-)均增大
6.下列离子方程式书写正确的是
A.H2PO4-在水溶液中的电离:H2PO4-+H2O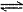 H3O++HPO42-
H3O++HPO42-
B.H2SO3在水溶液中的电离:H2SO3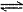 2H++SO32-
2H++SO32-
C.CO32-的水解:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
D.CaCO3的电离:CaCO3 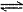 Ca2++CO32-
Ca2++CO32-
5.在25℃时,100mL 0.4mol/L的盐酸与等体积0.6mol/L的氢氧化钠溶液混合后,溶液
的pH值为(已知lg2=0.3)
A.0.7 B.1 C.13 D.13.3
4.下列物质不属于有机物的是
①CO2 ②NaCN ③CO(NH2)2 ④NaHCO3 ⑤乙醇
A.①②④ B.①④ C.③⑤ D.①②
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com