
7.C解析:在常温下pH=7的溶液中:Fe3+与氢氧根离子发生沉淀;常温下c(OH-)/c(H+)=1014的溶液中:即在碱性条件下,Mg2+与氢氧根离子发生沉淀;能与金属铝反应放出氢气的溶液中:可能是酸溶液,4H++NO3-+3Fe2+=3Fe3++NO↑+2H2O,也可能是碱溶液,Fe2+与氢氧根离子发生沉淀。
说明:在不同的介质中,考查常见离子可能发生的变化。特别是在存在HCO3-的澄清透明溶液中,几种离子存在形式,能与金属铝反应放出氢气的溶液可能是酸溶液,或者是强碱溶液,看几种离子存在形式。
7.在下列各溶液中,一定能大量共存的离子组是 ( )
A.常温下pH=7的溶液中:Fe3+、Na+、Cl-、NO3-
B.常温下c(OH-)/c(H+)=1014的溶液中:K+、Mg2+、Cl-、Br-
C.含有大量HCO3-的澄清透明溶液中:K+、C6H5O-、Cl-、Na+
D.能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Fe2+
6.A解析:NO2溶于水且与水反应生成NO,A正确;铁制品表面镀锌应用含Zn2+的电解质溶液作电解液,B不正确;浓硫酸稀释应先在烧杯稀释且冷却到室温后才能转移到容量瓶中,C不正确;Na2O2 与水作用后不能保持块状,Na2O2不适合用启普发生器来制备氧气,D不正确。
6.下列实验装置、试剂选用或操作正确的是
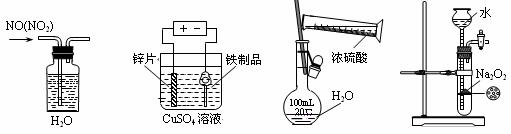
A.除去NO中的NO2 B.铁制品表面镀锌 C.稀释浓硫酸 D.制备少量O2
5.C解析:X、Y和Z分别为:N、Mg和S,则NH3溶于水显碱性,A错; X与Y形成化合物的化学式为Mg3N2,B错;MgO是离子化合物,C正确;HNO3和H2SO4都是强酸,D错。
5.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍。下列说法正确的是 ( )
A.X的氢化物溶于水显酸性 B.X与Y形成化合物的化学式为X2Y3
C.Y的氧化物是离子化合物 D.X和Z的最高价氧化物对应的水化物都是弱酸
4.C解析: NH4Cl溶液中由于NH4+的水解而使NH4+离子数目减少;常温下Cu-Zn原电池中产生的1.12 L H2一定不是0.05 mol;由于N2与H2的反应是可逆的,1.4 g N2与0.3 g反应并不能得到1.7 g(0.1 mol)NH3。
4.设阿伏加德罗常数的值为NA。下列叙述正确的是
A.1.0L0.1mol/L的NH4Cl溶液中NH4+的个数为0.1NA
B.常温下,Cu-Zn原电池中,正极产生1.12LH2时,转移的电子数为0.1NA
C.常温下,0.05mol CO2和SO2混合气体中所含氧原子数为0.1NA
D.高温高压下,1.4 g N2与0.3 g H2反应,生成的NH3分子数为0.1NA
3.D解析:众多植物通过光合作用,吸收太阳辐射能,将CO2和H2O 转为具有较高生物质能的糖类,A正确;加油站销售的汽车燃油,其中就有一部分为乙醇汽油,B正确;汽油的主要成分为烃类,而图中生物燃料主要成分常为烃的含氧衍生物,如乙醇。
3.从能源的可再生性角度来看,“在未来一个较短的时期内,最有潜力替代石油的能源是生物质能源。”下图就是生物质能源的生成与利用的循环图:
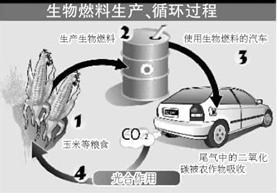
下列有关说法不正确的是
A.光能→生物质能转化的本质也是光→化学能的转换
B.为了减少化石燃料的使用,可在汽车中加入一定量的乙醇作为汽车燃料。
C.可表示图中4的反应式为:6CO2+6H2O
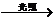 C6H12O6+6O2
C6H12O6+6O2
D.图中2生产的生物燃料主要成分为烃类
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com