
2.实验室快速制取氨气的方法是:
|
方法 |
化学方程(或原理) |
气体发生装置 |
|
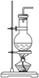
加热浓氨水 |
NH3·H2O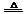 NH3↑+H2O NH3↑+H2O |
 |
|
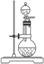
浓氨水+固体NaOH或生石灰 |
NaOH溶于水放热,促使氨水分解: NH3·H2O 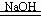 NH3↑+H2O NH3↑+H2ONH3·H2O+CaO=NH3↑+Ca(OH)2 |
 |
1.以NO为中心的转化关系图
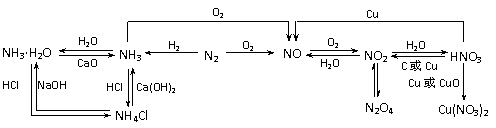
2.溶液中SO42-的检验
⑴原理:利用Ba2++ SO42-=BaSO4↓ (白色),BaSO4具有不溶于盐酸、硝酸的特性。
⑵试剂:可溶性钡盐(BaCl2或Ba(NO3)2溶液)、盐酸或稀硝酸。
⑶检验的误区:
①只加可溶性钡盐,不酸化。误将CO32-、PO43-、SO32-、Ag+等干扰离子判成SO42-,此时上述离子同样会产生BaCO3、Ba3(PO4)2、BaSO3、AgCl的白色沉淀。
②误将Ag+、Pb2+判成SO42-。如向待测液中滴加BaCl2溶液,再加盐酸有白色沉淀便断定含SO42-。其错误是未注意溶液中不含SO42-而含Ag+或Pb2+也会有同样现象。
因为Ag++Cl-==AgCl↓(白色) Pb2++2Cl-==PbCl2↓(白色)
③误将SO32-判成SO42-。如向待测液中滴加用盐酸酸化的Ba(NO3)2溶液生成白色沉淀,便误以为有SO42-。该错误是未注意NO3-具有强氧化性,在酸性环境中发生反应:
Ba2++ SO32-==BaSO3↓(白色),3BaSO3+2H++2 NO3-==3BaSO4↓(白色)+2NO↑+H2O
再如向待测液中滴加用硝酸酸化的BaCl2溶液产生白色沉淀,便错误地认定一定含SO42-,也同样是落入干扰离子转化为SO42-从而生成BaSO4的陷阱中。
⑷检验的关键:既要注意试剂的选择,又要注意操作顺序的优化,方能排除干扰离子的误导,全面考虑,综合分析,正确推导。
1.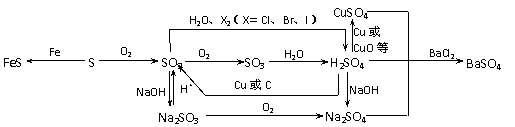 以SO2为中心的转化关系图
以SO2为中心的转化关系图
3.漂白原理的比较:
⑴氧化漂白。氯水、次氯酸盐、Na2O2和H2O2在一定条件下分解放出原子氧,原子氧(可表示为[O])的活性很强,有较强的氧化能力,能将许多有色物质氧化成无色物质,从而达到漂白的目的。被漂白的物质不变色,此类漂白剂能漂白酸碱指示剂。
⑵化合漂白。如SO2的漂白,其原理是SO2溶于水生成亚硫酸,亚硫酸与有色物质化合,形成不稳定的无色化合物,无色化合物在一定条件下(如加热)分解恢复原色。SO2不能漂白酸碱指示剂。
⑶吸附漂白。活性炭、硅藻土的漂白原理是由于有许多小孔隙,总表面积大,有较强的吸附作用,通过吸附溶液中的一些有色物质或有色离子或有色气体使之褪色,属于物理变化。
2.能与氯气反应的物质归类如下:
|
物质类别 |
非金属 单质 |
金属 单质 |
水 |
碱 |
非金属 氧化物 |
还原性 离子 |
有机物 |
|
|
代表物质 |
H2、P |
Na、Cu、Fe |
H2O |
NaOH、Ca(OH)2 |
SO2(水溶液中) |
Fe2+、SO32-、S2-、Br-、I- (水溶液中) |
烯烃、 炔烃 |
烷烃、 芳香烃 |
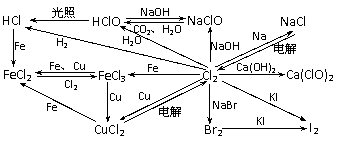
1.以Cl2为中心的转化关系图:
16.重庆市中小学“科技之星”创新大赛活动拉开序幕。
[科技创新 我动员]假如你所在的学校准备召开全体学生动员大会,请你做动员发言,你会运用思想品德所学的哪些有关知识?(2分)
[科技之星 我争创]加入你代表学校参加这次“科技之星”创新大赛,你应从哪些方面作好准备?(2分)
[智力成果 我维护]如果你的小制作、小发明取得成功,你准备怎样保护自己的智力成果?(2分)
答:(1)①科技是第一生产力,创新是一个民族进步的灵魂创新;②我国实施科教兴国、人才强国战略。③创新的希望在青少年,我们要从小培养创新精神和实践能力。(2分)
(2)①做好思想上的准备,培养自己具有不怕困难,战胜困难的进取精神。②做好知识的储备,了解、掌握相关知识。③做好物质准备,准备好所需材料和工具。(2分)
(3)申请专利权,寻求法律保护。(2分)
2.
2009年重庆思想品德中考 活动探究题 (6分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com