
19.恒容密闭容器中进行的可逆反应2NO2(g)  2NO(g)+O2(g),不能说明该反应达到平衡状态的是
2NO(g)+O2(g),不能说明该反应达到平衡状态的是
A.单位时间内生成n mo1 O2的同时生成2nmol NO2
B.混合气体的颜色不再改变
C.混合气体的密度不再改变的状态 D.混合气体的压强不再改变的状态
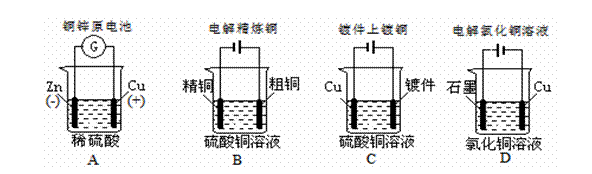
18.下列图示中关于铜电极的连接错误的是
17.下列事实不能用勒夏特列原理解释的是
A.氯水中有平衡:Cl2+H2O HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅。
HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅。
B.对CO(g)+NO2(g)
 CO2(g)+NO(g),平衡体系增大压强可使颜色变深。
CO2(g)+NO(g),平衡体系增大压强可使颜色变深。
C.升高温度能够促进水的电离。
D.SO2催化氧化成SO3的反应,往往加入过量的空气
16.下列说法正确的是
A.pH=5的盐酸,再加水冲稀1000倍,溶液的pH=8
B.给稀醋酸溶液加热,溶液pH值增大
C.pH=1的盐酸中c(H+)是pH=3的盐酸的100倍
D.在H2CO3溶液中,C(H+) :C(CO32--)=2∶1
15.高温下,某反应达平衡,平衡常数K=。恒容时,温度升高,
H2 浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.该反应化学方程式为:CO + H2 O 催化剂高温 CO2 + H2
C.增大压强,H2浓度一定不变
D.升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
14. 镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2
Cd+2NiOOH+2H2O 由此可知,该电池充电时在阴极上发生反应的是
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2
Cd+2NiOOH+2H2O 由此可知,该电池充电时在阴极上发生反应的是
A.Cd(OH)2 B.Ni(OH)2 C.Cd D.NiOOH
13.在温度相同,压强分别为P1和P2的条件下,A(g) + 2B(g) 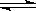 nC(g)
nC(g)
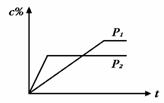 的反应体系中,C的百分含量(C%)与时间t的曲线
的反应体系中,C的百分含量(C%)与时间t的曲线
如右图所示,下面结论正确的是
A.P1>P2,n<3 B.P1<P2,n>3
C.P1>P2,n>3 D.P1<P2,n<3
12.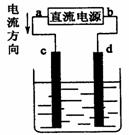 下图是电解NaCl溶液(加有酚酞)装置,其中c、d为石墨电极。下列有关的判断正确的是
下图是电解NaCl溶液(加有酚酞)装置,其中c、d为石墨电极。下列有关的判断正确的是
A.a为负极、d为阳极
B.c电极上的电极反应式为:
2H+ + 2e一== 2H2↑
C.电解过程中,d电极附近溶液变红
D.电解过程中,氯离子浓度不变
11.下列反应过程中,ΔH>0且ΔS>0的是
A.NH3(g)+HCl(g) NH4Cl(s)
NH4Cl(s)
B.CaCO3(s) CaO(s)+CO2(g)
CaO(s)+CO2(g)
C.4Al(s)+3O2(g) 2Al2O3(s)
2Al2O3(s)
D.HCl(aq)+NaOH(aq) NaCl(aq)+H2O(l)
NaCl(aq)+H2O(l)
10.在0.10 mol·L-1CH3COOH溶液中存在如下电离平衡:
 CH3COOH CH3COO-
+H+ 对于该平衡,下列叙述正确的是
CH3COOH CH3COO-
+H+ 对于该平衡,下列叙述正确的是
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.10 mol·L-1HCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com