
29.(9分)某化学实验小组从市场上买来一瓶某品牌食用白醋(主要是醋酸的水溶液),用实验室标准NaOH溶液对其进行滴定以测定它的准确浓度,完全反应时所得溶液pH大致为9 。下表是4种常见指示剂的变色范围:
|
指示剂 |
石蕊 |
甲基橙 |
甲基红 |
酚酞 |
|
变色范围(pH) |
5.0-8.0 |
3.1-4.4 |
4.4-6.2 |
8.2-10.0 |
(1)该实验应选用 作指示剂。
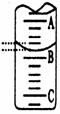 (2)右图表示50mL滴定管中液面的位置,若A与C刻度间
(2)右图表示50mL滴定管中液面的位置,若A与C刻度间
相差1mL,A处的刻度为25,滴定管中液面读数应为 mL;
反应达滴定终点时的现象为 。
(3)为减小实验误差,该同学一共进行了三次实验,假设每
次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次
实验结果记录如下:
|
实验次数 |
第一次 |
第二次 |
第三次 |
|
消耗NaOH溶液体积/mL |
26.02 |
25.35 |
25.30 |
 从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是 。
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是 。
A.实验结束时,俯视刻度线读取滴定终点时NaOH溶液的体积
B.滴定前滴定管尖嘴有气泡,滴定结束尖嘴部分充满溶液
C.盛装白醋溶液的滴定管用蒸馏水洗过,未用白醋溶液润洗
D.锥形瓶预先用食用白醋润洗过
E.滴加NaOH溶液时,未充分振荡,刚看到溶液变色,立刻停止滴定
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):C= mol/L。
|
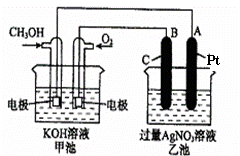 2CH3OH+3O2+4KOH
2CH3OH+3O2+4KOH 2K2CO3+6H2O
(1)请回答图中甲、乙两池的有关问题:
甲池是 装置,
B(石墨)电极的名称是 。
(2)写出电极反应式:
通入O2的电极的反应式 。
A(Pt)电极的反应式为 ,
(3)乙池中反应的化学方程式为 。
(4)若乙池溶液体积为500mL,且忽略电解过程中溶液体积的变化,当乙池中A极的质量增加5.40g时:
①甲池中理论上消耗O2体积为 (标准状况下);
②乙池中所得溶液的pH= 。
28.下列有关判断正确的是
A.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+
B.由Mg、Al、NaOH溶液组成原电池,其负极反应式为: Al-3e-+3OH-=Al(OH)3
C.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+ D.用原电池和电解池装置都能实现2HCl + Cu CuCl2
+ H2↑ 反应
CuCl2
+ H2↑ 反应
27.已知:在100℃时,纯水的c(H+)为1×10-6,此时将pH=12的NaOH溶液V1 L与pH=l的H2SO4溶液V2 L混合,若所得混合溶液的pH=10,则V1∶V2为
A.1∶9 B.10∶1 C.9∶1 D.1∶10
26.有等体积、等pH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是
A.V3>V2>V1 B.V3=V2=V1 C.V1=V2>V3 D.V3>V2=V1
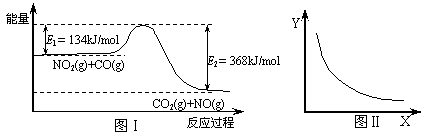
25.下图Ⅰ是NO2(g)+CO(g)  CO2(g)+NO(g) 反应过程中能量示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ。下列有关说法正确的是
CO2(g)+NO(g) 反应过程中能量示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ。下列有关说法正确的是
A.该反应的焓变△H=234kJ/mol
B.若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C.若X表示温度,则Y表示的可能是CO2的物质的量浓度
D.若X表示反应时间,则Y表示的可能是混合气体的密度
24.在以下四种溶液中,各离子一定能大量共存的是
A.滴加酚酞试液显红色的溶液:Fe3+、NH4+、Cl-、CO32-
B.所含溶质为MgCl2的溶液:K+、NO3-、SO42-、Al3+
C.水电离出来的c(H+)=10-13mol/L的溶液:K+、Na+、HCO3-、Br-
D.pH=1的溶液: Fe2+、Na+、I-、NO3-
23.(12分)右图是铜锌原电池装置。其电池的总反应是:
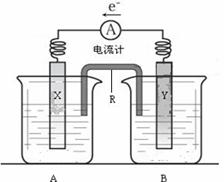 Zn(s) + CuSO4(aq)==
ZnSO4(aq) +
Cu(s)。
Zn(s) + CuSO4(aq)==
ZnSO4(aq) +
Cu(s)。
请回答以下问题:
⑴R的名称是__________________,R中的阳离子移向_______(填A或B)中的溶液
⑵电极Y的材料是________,B中的电解质溶液是________________。
⑶X为原电池的______极,其电极反应式是____________________________。
第Ⅱ卷 (共50分)
注意:将第Ⅱ卷的选择题答案按照题号正确添涂在机答卡上
22.(14分)在一恒容密闭容器中发生某化学反应2A(g) 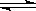 B(g)+ C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始量都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图所示:
B(g)+ C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始量都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图所示:
试回答下列问题:
(1)在实验Ⅰ中,反应在20 min至40 min内A的平均反应速率为
mol·L-1min-1。
(2)根据实验Ⅲ和实验Ⅰ的比较,可推测该反应降低温度,平衡向 (填“正”或“逆”)反应方向移动,该正反应是_________(填“放热”或“吸热”)反应。
(3)若将实验Ⅰ中A的起始浓度改为0.8 mol·L-1,其它条件不变,与实验Ⅰ相比,则达平衡时所需时间________实验Ⅰ(填写“大于”、“等于”或“小于”)。
(4)实验Ⅱ和实验I相比,可能隐含的反应条件是____________________。
A.升高温度 B.增大压强 C.使用了催化剂 D.增大A的浓度
(5)800℃时,A达平衡时的转化率为 ,此温度下该反应的化学平衡常数K值为 。
21.(14分)
(1)火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。
已知:N2(g) + 2O2(g)= 2NO2(g) △H = +67.7 kJ/mol;
N2H4(g)+ O2(g)=N2(g)+2H2O(g) △H=-534 kJ/mol
则N2H4和NO2反应生成氮气和水蒸气的热化学方程式为__________________ 。
(2)已知:常温下0.1mol/L的某酸H2A的pH=4,则该酸为 酸(填“强”或“弱”), H2A的电离方程式为 ,该溶液中由水电离出的c(H+)= 。
(3)一定温度下,两种酸:a、盐酸 b、醋酸:
①当两种酸的物质的量浓度相同时,c(H+):a b(填“>”、“<”或“=”,下同)
②在pH相同、体积相同的两种酸溶液中加入过量的铁粉,反应结束时生成H2的总体积:a b。
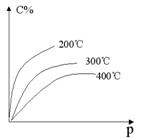
 ③将pH相同,体积相同的两种酸溶液分别加水稀释100倍,所得溶液的pH值:a b
③将pH相同,体积相同的两种酸溶液分别加水稀释100倍,所得溶液的pH值:a b
20. 对于mA(s) +
nB(g)
对于mA(s) +
nB(g) 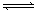 eC(g) +
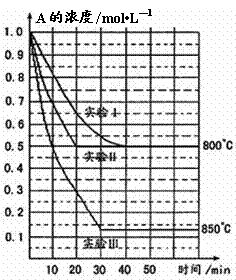
f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)和压强(P)的关系如图,
eC(g) +
f D(g),反应过程中,当其它条件不变时,C的百分含量(C%)和压强(P)的关系如图,
下列叙述正确的是
A.达到平衡后,加入催化剂,则C%增大
B.达到平衡后,若升温,平衡逆向移动
C.化学方程式中n<e +f
D.达到平衡后,增加A的量,平衡正向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com