
4.某农科院在2×2的4块式验田中选出2块种植某品种水稻进行试验,则每行每列都有一块试验田种植水稻的概率为 ( )
A. B.
B.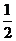 C.
C.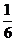 D.
D.
3.已知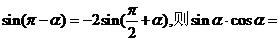 ( )
( )
A.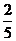 B.
B.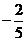 C.
C.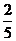 或
或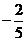 D.
D.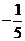
2.复数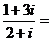 ( )
( )
A.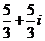 B.
B.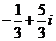 C.
C.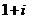 D.
D.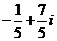
1.已知集合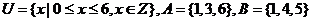 ,则
,则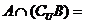 ( )
( )
A.{1} B.{3,6} C.{4,5} D.{1,3,4,5,6}
20、为证明乙醇分子中含有氧原子,现采用一套装置进行实验。试根据装置示意图、试剂及实验现象,回答有关问题。
Ⅰ.装置中所装的试剂:
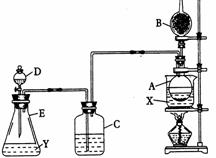 ① A瓶装无水乙醇,内放无水CuSO4 ② B干燥管中装生石灰
③ C和D中都装浓硫酸 ④ E瓶中装入试剂Y为浓盐酸
① A瓶装无水乙醇,内放无水CuSO4 ② B干燥管中装生石灰
③ C和D中都装浓硫酸 ④ E瓶中装入试剂Y为浓盐酸
Ⅱ.实验操作及现象:用水浴加热A瓶;将D中浓硫酸缓缓滴入E中与浓盐酸作用;发现C中导管有大量气泡放出;A瓶内无水CuSO4逐渐变成蓝色,在B管口挥发出的气体可点燃。请回答以下问题:
(1)E瓶用于制取 气体。
(2)D中浓硫酸所起的作用是
;
C瓶中浓硫酸所起的作用是 。
(3)A瓶中发生反应的化学方程式为
反应类型为 ,所生成的 (填名称)在B出口处点燃。
(4)此实验能证明乙醇分子中含有氧原子的理由是
(5)若将实验装置中的C瓶取走,能否达到实验目的 (填“能”或
“否”),原因是
18、实验室用下列装置所示的流程进行气体性质实验。图中用箭头表示气体的流向,A为一种纯净、干燥的气体,B是另一种气体,己中有红棕色气体出现。实验中所用的药品只能从下列物质中选取:Na2CO3、NaHCO3、Na2O、Na2O2、NaCl、无水CaCl2、(NH4)2CO3、碱石灰等固体和蒸馏水。
根据图中装置和现象回答:
(1)丙中发生反应的化学方程式为_______________________________
(2)丁中应选用的干燥剂是___ __,为什么不选用所给的另一种干燥剂______ __
(3)甲中发生反应的化学方程式__________________________________
(4)戊中发生的主要反应的化学方程式___ 。此反应是吸热反应还是放热反应__ __,估计可看到什么现象足以说明你的判断________________________________ ____。
(5)当己中充满红棕色气体后,停止给丙加热并关闭a、b两个活塞。若将己浸入冰水中,则己中将有什么现象发生?简述发生此现象的原因________________
17、合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4︰5,其中Fe2+与Fe3+物质的量之比为___________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1︰2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为___________(用小数表示,保留2位小数)。
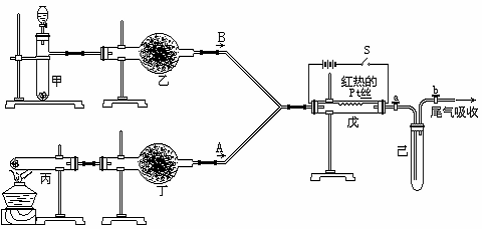
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:
2Fe2O3+C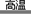 4FeO+CO2↑。为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为_________g。
4FeO+CO2↑。为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为_________g。
16、将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
(1)NO的体积为 L,NO2的体积为 L。
(2)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为 mol/L。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水 g。
15、为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加Ag NO3溶液,产生白色沉淀。
根据实验以下推测正确的是( )
A.一定有SO32-离子 B.一定有CO32-离子
C.不能确定Cl-离子是否存在 D.不能确定HCO3-离子是否存在
14、下面是实验室制取氨气的装置和选用的试剂,其中错误的是( )
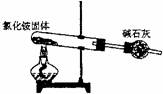
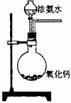


A B C D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com