
1. 下列实验操作中,仪器需插入液面下的有( )
A. 制备氢气,简易装置中长颈漏斗的下端管口
B. 用水吸收氨气时的导气管
C.
向试管中的 溶液滴加稀盐酸
溶液滴加稀盐酸
D.
制备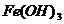 ,用胶头滴管将
,用胶头滴管将 溶液滴入
溶液滴入 溶液中
溶液中
3. 常见气体的制备与净化:
(1)气体的发生装置:
|
类型 |
固+固 气 气 |
固+液 气 气 |
固+液 气+液 气+液 |
|
发生装置 |
 |
 |
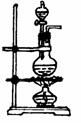 |
|
所制气体 |
 、 、 、 、 |
 、 、 、 、 、 、 、 、 、 、 |
 、 、 、 、 、 、 、 、 |
(2)气体的收集方法:
① 排水法和排饱和食盐水方法
② 排气法
(3)气体的净化和干燥:
① 气体除杂的四项原则:不损失主体气体;不引入新的杂质气体;在密闭装置中进行;先易后难。
常见气体的除杂试剂:
|
杂质 气体 |
 |
 、 、 |
 |
 |
    |
   |
  |
  |
 |
|
除杂 试剂 |
水或饱和食盐水 |
饱和 溶液 溶液 |
 或 或 |
浓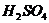 |
碱石灰 |
强碱 溶液 |
溴水 |
灼热 |
灼热铜网 |
② 气体的干燥:
干燥剂的选择及干燥装置;常见的干燥剂及使用范围:
|
类型 |
干燥剂 |
可干燥的气体 |
|
酸性干燥剂 |
浓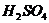 P2O5、硅胶 |
N2、O2、H2、Cl2、CO、CO2、NO2、CH4、SO2、HCl N2、O2、H2、Cl2、HCl、H2S、CO、CO2、NO2、SO2、CH4、C2H2、C2H4 |
|
碱性干燥剂 |
碱石灰 |
N2、O2、H2、CH4、C2H2、C2H4、NH3 |
|
中性干燥剂 |
无水 |
N2、O2、H2、HCl、H2S、CO、CO2、SO2、CH4、C2H2、C2H4 |
(4)尾气处理
(5)制取气体的装置安装顺序:
发生装置 净化装置
净化装置 干燥装置
干燥装置 收集装置
收集装置 吸收装置
吸收装置
[典型例题]
[例1] 下列实验操作中,错误的是( )
A. 配制5%食盐溶液时,将称量的食盐放入烧杯中加计量的水搅拌溶解
B. 硫酸铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C. 测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2-3次
D. 配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
解析:容量瓶是用来配制准确的物质的量浓度溶液的仪器,不能用来长期盛装试剂,更不能用来溶解固体或稀释液体及盛装热的溶液。稀释浓H2SO4时会放出大量的热,所以D不正确。
答案:D
[例2] 资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行NH3与氧气在不同条件下反应的实验。



A B C
(1)用装置A制取纯净、干燥的NH3,大试管内碳酸盐的化学式是 ,碱石灰的作用是 。
(2)将产生的NH3与过量的O2通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①  催化氧化的化学方程式是
;试管里气体变为红棕色,该反应的化学方程式是
。
催化氧化的化学方程式是
;试管里气体变为红棕色,该反应的化学方程式是
。
② 停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因。
(3)将过量的O2与A产生的NH3分别从 、
、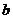 两管进气口通入到装置C中,并在
两管进气口通入到装置C中,并在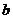 管上端点燃
管上端点燃 :
:
① 两气体通入的先后顺序是 ,其理由是 。
② 氨气燃烧的化学方程式是 。
解析:
(1)实验室一般使用铵盐和强碱共热来制取 ,这里使用的铵盐可以是
,这里使用的铵盐可以是 或者
或者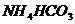 。
。 或者
或者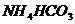 受热分解还会产生H2O和CO2,需要利用碱石灰除去。
受热分解还会产生H2O和CO2,需要利用碱石灰除去。
(2)工业上利用 催化氧化法制取
催化氧化法制取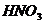 ,原理和该反应类似。发生的反应分别是:
,原理和该反应类似。发生的反应分别是: ,
,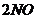 (无色气体)+
(无色气体)+
 (红棕色气体)试管中存在平衡:
(红棕色气体)试管中存在平衡: (红棕色气体)
(红棕色气体)
 (无色气体),正反应为放热反应。用冰水冷却时,平衡向正反应方向移动,气体颜色变浅。
(无色气体),正反应为放热反应。用冰水冷却时,平衡向正反应方向移动,气体颜色变浅。
(3)通入气体的顺序是:先通 ,后通
,后通 。因为先通
。因为先通 不能在空气中燃烧,必须在浓度较高的
不能在空气中燃烧,必须在浓度较高的 中才能燃烧。如果先通
中才能燃烧。如果先通 ,
, 就会直接逸出,造成污染。发生的化学反应为:
就会直接逸出,造成污染。发生的化学反应为: 。
。
答案:
(1) 或
或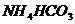 ;可除去产生的
;可除去产生的 和
和
(2)① 

② 因试管中存在

 的平衡,冷却时平衡向生成
的平衡,冷却时平衡向生成 的方向移动,使颜色由
的方向移动,使颜色由 (红棕)变为
(红棕)变为 (无色),颜色变浅。
(无色),颜色变浅。
(3)① 先通 ,后通
,后通 。理由(略)
。理由(略)
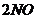 (无色气体)
(无色气体) =
= (红棕色气体)
(红棕色气体)
② 
[例3] 用示意图中的装置进行A、B、C、D四组实验,在 、
、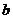 、
、 中加入的试剂如表中所示,填写表中空格。
中加入的试剂如表中所示,填写表中空格。
|
|
 |
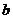 |
 |
实验现象 |
解释 |
|
|
A |
饱和 食盐水 |
碳化钙 |
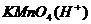 溶液 |
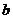 中 中 |
|
/ |
 中 中 |
|
|
||||
|
B |
浓盐酸 |
 |
 溶液 溶液 |
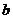 中 中 |
|
|
 中 中 |
|
|
||||
|
C |
稀盐酸 |
大理石 |
 溶液 溶液 |
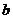 中 中 |
|
/ |
 中 中 |
|
|
||||
|
D |
浓硫酸 |
浓盐酸 |
紫色石蕊溶液 |
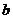 中 中 |
|
|
 中 中 |
|
/ |
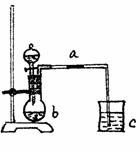
解析:A中用饱和食盐水和碳化钙反应制乙炔时,反应快但不剧烈,有利于得到平稳的乙炔气流。B中 的氧化性较强,在常温下即可氧化HCl制得
的氧化性较强,在常温下即可氧化HCl制得 。D中向浓盐酸中滴加浓
。D中向浓盐酸中滴加浓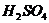 ,由于混合放热及浓
,由于混合放热及浓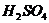 的吸水性,导致
的吸水性,导致 大量挥发,从而制得
大量挥发,从而制得 气体。
气体。
答案:
|
A |
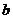 中 中 |
有气泡生成 |
/ |
 中 中 |
溶液紫色褪去 |
乙炔易被氧化剂氧化 |
|
|
B |
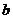 中 中 |
有黄绿色气体生成 |
 氧化性比 氧化性比 强 强 |
 中 中 |
溶液由无色变橙色 |
 氧化性比 氧化性比 强 强 |
|
|
C |
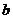 中 中 |
有气泡生成 |
/ |
 中 中 |
有白色胶状沉淀生成 |
碳酸的酸性比硅酸强 |
|
|
D |
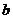 中 中 |
有白雾生成,放出大量的热 |
浓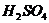 稀释时放出大量热;盐酸挥发出 稀释时放出大量热;盐酸挥发出 与水蒸气结合成酸雾。 与水蒸气结合成酸雾。 |
 中 中 |
紫色石蕊试液变红色 |
/ |
[模拟试题]
2. 化学实验基本操作:
(1)药品的取用
(2)检查装置的气密性
① 微热法(基本方法)
② 液差法
<1> 启普发生器气密性检查
<2> 简易气体发生装置气密性检查
③ 液封法
(3)物质的称量和液体的量取
(4)溶解、过滤、洗涤
1. 常用药剂的贮存方法:
|
分类 |
试剂名称 |
保存方法 |
|
碱 |
强碱 |
橡胶塞、密闭、玻璃瓶 |
|
氨水 |
密闭、橡胶塞、玻璃瓶、冷暗处 |
|
|
酸 |
浓硫酸 |
密闭、玻璃塞、玻璃瓶 |
|
浓硝酸 |
低温、棕色玻璃瓶 |
|
|
浓盐酸 |
密闭、玻璃瓶 |
|
|
冰醋酸 |
常温以下(16.6℃)、玻璃瓶 |
|
|
氢氟酸 |
塑料瓶 |
|
|
盐 |
苏打水 水玻璃 |
橡胶塞、密闭、玻璃瓶 |
|
其 他 |
白磷 |
少量时,保存在水中;大量时,密闭封存 |
|
液溴 |
水封、玻璃塞、棕色玻璃瓶 |
|
|
钾、钙、钠 |
少量时,保存在煤油中;大量时,密闭封存 |
|
|
汽油等 |
密闭保存、玻璃塞、远离火源、置于阴凉处 |
|
|
用棕色瓶保存的药品有: 浓硝酸、硝酸银、氯水、溴水、碘水、某些有机物 |
化学实验(一)常用试剂的使用与贮存,化学实验基本操作 气体的制备与净化
30、1873年,法国某报纸刊登的一封读者来信写到:“我们是工业家和土地所有者,需要秩序,并不喜欢共和政体。但是,如果‘联合派’(属于君主派)获得胜利,那些现在还留在我们方面的大部分人将投入极端共和派的怀抱去了。”这段话反映出当时在法国 A. 政治局面错综复杂 B. 无产阶级建立了共和政体 C. “联合派”能带来社会安定 D. 共和派已获得政治上的绝对优势
29、1787年宪法使独立后的美国从邦联发展成为联邦制共和政体,其重要作用是
①结束了松散状态,维护了国家统一 ②满足了人民群众众多权益的要求
③确立了美国的责任制内阁 ④促进了美国资本主义的发展
A、①④ B、①② C、②③ D、③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com