
8. 下列实验方法或操作错误的是( )
A.
将3滴甲苯加入2mL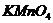 酸性溶液振荡可褪色
酸性溶液振荡可褪色
B.
用干净的玻璃棒蘸取待测液,滴在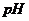 试纸上以测定溶液
试纸上以测定溶液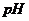
C. 中和滴定时,用洗净但未经干燥的锥形瓶盛待测液
D. 制取酚醛树脂后的试管,可以用乙醇清洗
7. 确证汽油是混合物的一种方法是( )
A. 测量密度 B. 测量沸点 C. 将它燃烧 D. 闻气味
6. 下列制备实验中都使用硫酸,其中必须使用稀硫酸的是( )
① 制二氧化硫 ② 制硫化氢 ③ 制氯化氢
④ 制硝基苯 ⑤ 由氧化铜制硫酸铜 ⑥ 由铁屑制绿矾
A. ②⑤⑥ B. ①②④ C. ①⑤⑥ D. ②③④
5. 足量的镁与一定量的盐酸反应制取氢气,为了减慢反应速率。但不影响产生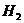 的总量,可以加入下列固体中的( )
的总量,可以加入下列固体中的( )
A. 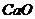 B.
B. 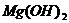 C.
C. 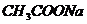 D.
D. 
4. 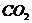 气体通入下列溶液中,不变浑浊的是( )
气体通入下列溶液中,不变浑浊的是( )
A. 苯酚钠溶液 B.  溶液 C.
溶液 C. 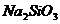 溶液 D.
溶液 D. 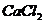 溶液
溶液
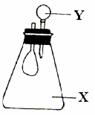
3. 下图中,锥形瓶内盛有气体X,滴管内盛有液体Y,若挤压滴管胶头,使液体Y滴入瓶中,振荡,一会儿可见小气球鼓起,气体X和液体Y不可能是( )
A.
X是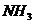 ,Y是水
,Y是水
B.
X是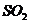 ,Y是
,Y是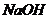 溶液
溶液
C.
X是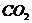 ,Y是稀硫酸
,Y是稀硫酸
D.
X是 ,Y是
,Y是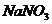 稀溶液
稀溶液
2. 为验证淀粉能水解,且水解的生成物有还原性能,可能用到如下某些实验步骤:① 加入稀硫酸 ② 加入几滴硫酸铜溶液 ③ 加热 ④ 加入蒸馏水 ⑤ 加入烧碱溶液至显碱性 ⑥ 加入新制氢氧化铜
正确的最佳程序应是( )
A. ④①③⑥③ B. ④③①⑥⑤③
C. ①③②⑥③ D. ④①③⑤⑥③
1. 下列反应中有黄色物质生成的是( )
A. 鸡蛋白和几滴浓硝酸混合,微热
B.
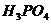 溶液和
溶液和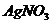 溶液混合
溶液混合
C.
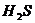 气体通过灼热的玻璃管
气体通过灼热的玻璃管
D. 苯酚溶液和氧化铁溶液作用
3. 具体示例:
(1)乙二酸化学性质实验方案的设计;(运用上述思路和给出乙二酸性质的相关资料拟定实验方案)
(2)铜和铜的化合物性质实验方案的设计:
铜的性质--弱还原性
铜的化合物性质--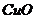 、
、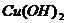 、
、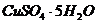
(3)红砖中氧化铁的成分检验
[典型例题]
[例1](1)将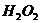 溶液滴入含有酚酞的
溶液滴入含有酚酞的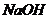 溶液中,红色消失。甲同学认为这是由于
溶液中,红色消失。甲同学认为这是由于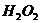 是二元弱酸(
是二元弱酸(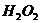

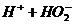 ),消耗了
),消耗了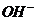 ,而使红色褪去。乙同学认为
,而使红色褪去。乙同学认为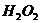 具有强氧化性,将酚酞氧化,红色消失。试设计一个实验论证甲、乙两位同学的解释中谁正确。
具有强氧化性,将酚酞氧化,红色消失。试设计一个实验论证甲、乙两位同学的解释中谁正确。
答: 。
(2)甲同学向品红溶液中通入一种气体后,品红褪色。乙同学设计了一个很简便的实验便知甲同学通的是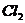 还是
还是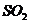 。他的实验方案是 。
。他的实验方案是 。
解析:
(1)依题意可知:
甲--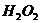 与
与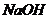 发生中和反应,酚酞未被消耗。
发生中和反应,酚酞未被消耗。
乙--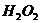 氧化酚酞,
氧化酚酞,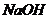 未消耗。
未消耗。
只需通过实验验证,酚酞和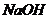 哪一种物质存在即可。
哪一种物质存在即可。
设计方案有二种:
其一--取溶液少量继续加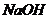 ,看溶液是否变红,若变红证明酚酞尚存则甲正确,否则乙正确。
,看溶液是否变红,若变红证明酚酞尚存则甲正确,否则乙正确。
其二--取溶液少量滴加酚酞,若溶液变红,证明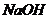 尚存,则乙正确,否则甲正确。
尚存,则乙正确,否则甲正确。
证明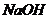 尚存,则乙正确,否则甲正确。
尚存,则乙正确,否则甲正确。
(2)由于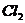 的漂白性与
的漂白性与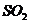 漂白性的原理不同。
漂白性的原理不同。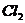 为通过氧化进行漂白,是永久漂白。而
为通过氧化进行漂白,是永久漂白。而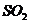 是与某些有机色素化合生成不稳定无色物质,加热可恢复原色,乙同学可利用此性质进行实验设计。
是与某些有机色素化合生成不稳定无色物质,加热可恢复原色,乙同学可利用此性质进行实验设计。
只需取少量溶液加热即可。若仍不能恢复红色,则为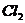 ,否则为
,否则为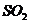 。
。
答案:略。
[例2] 为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。
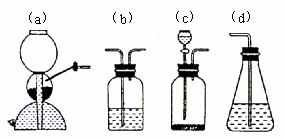

(电石、水)( ) ( ) 溴水
乙同学发现甲同学实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得乙炔中还有可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。
请你回答问题:
(1)写出甲同学实验中两个主要的化学方程式 。
(2)甲同学设计的实验 (填能或不能)验证乙炔与溴发生加成反应,其理由是 。
① 使溴水褪色的反应,未必是加成反应
② 使溴水褪色的反应,就是加成反应
③ 使溴水褪色的物质,未必是乙炔
④ 使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是 ,它与溴水反应的化学方程式是 。验证过程中必须全部除去。
(4)请你选用上列四个装置(可重复使用)来实现乙同学的实验方案,将它们的编号填入方框,并写出装置内所放的化学药品。
(5)为验证这一反应是加成而不是取代,丙同学提出可用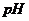 试纸来测试反应后溶液的酸性,理由是
。
试纸来测试反应后溶液的酸性,理由是
。
解析:该题为有机化合物性质的实验。已知乙炔与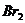 发生加成生成1,1,2,2--四溴乙烷成或1,2一二溴乙烯,不会产生淡黄色沉淀。则电石与
发生加成生成1,1,2,2--四溴乙烷成或1,2一二溴乙烯,不会产生淡黄色沉淀。则电石与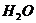 反应生成气体物质中必含还原性物质。
反应生成气体物质中必含还原性物质。
答案:
(1)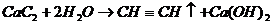
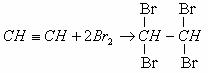 或
或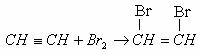
(2)不能;(由于生成的气体中混有还原性气体,也会使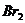 水褪色,则在净化前不能直接与
水褪色,则在净化前不能直接与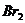 反应。)①、③
反应。)①、③
(3)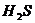 ;
;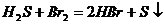
(4)c(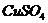 溶液);b(
溶液);b(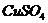 溶液)。
溶液)。
(5)如若发生取代反应,必定生成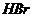 ,溶液酸性将会明显增强,故可用
,溶液酸性将会明显增强,故可用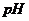 试纸验证。
试纸验证。
[模拟试题]
2. 性质实验方案设计的一般思路:
分析结构 对比回顾相关知识
对比回顾相关知识 预测性质
预测性质 拟定方案
拟定方案
分子结构 同系物 稳定性
原子结构 元素周期表 酸、碱性
氧化还原性
官能团反应
常识了解
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com