
9.下列各项表述中正确的是
A.硫离子的核外电子排布式:1s22s22p63s23p4
B.NH3、H2O、CO2、HCl分子中,CO2孤对电子对最多
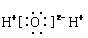 C.水分子的电子式:
C.水分子的电子式:
D.次氯酸的结构式:H-O-Cl
8.现有四种元素的基态原子的电子排布式如下:①ls22s22p63s23p4 ②ls22s22p63s23p3
③ls22s22p3 ④ls22s22p5 , 则下列有关比较中正确的是
A.第一电离能:④>③>②>①
B.原子半径:④>③>②>①
C.电负性:④>③>②>①
D.最高正化合价:④>③=②>①
7.下面的排序不正确的是
A.晶体熔点的高低: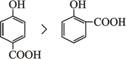
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.熔点由高到低:Na>Mg>Al
D.晶格能由大到小:NaF> NaCl> NaBr>NaI
6.叠氮酸(HN3)与醋酸酸性相似,下列错误的是
A.HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3-)>c(OH-)
B.HN3与NH3作用生成的叠氮酸铵是共价化合物
C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3-) >c(OH-)>c(H+)
D.N3-与CO2所含电子数相等
5.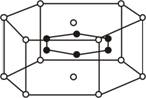 2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录。该化合物的晶体结构单元如右图所示:镁原子间形成正六棱柱,且棱柱的上下底面还各有一个镁原子,六个硼原子位于正六棱柱内,则该化合物的化学式可表示为
2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录。该化合物的晶体结构单元如右图所示:镁原子间形成正六棱柱,且棱柱的上下底面还各有一个镁原子,六个硼原子位于正六棱柱内,则该化合物的化学式可表示为
A.MgB B.MgB2
C.Mg2B D.Mg3B2
4.下图中能正确表示基态硅原子的是

A B C D
3.下列说法中正确的是
A.干冰升华时分子内共价键会发生断裂
B.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
C.分子晶体的熔沸点低,常温下均呈液态或气态
D.金属导电的原因是在外加电场的作用下金属产生自由电子,电子定向运动
2.与NH4+互为等电子体的分子是
A.H3O+ B.OH- C.NH3 D.CH4
1.元素“氦、铷、铯”等是用下列哪种科学方法发现的
A.红外光谱 B.质谱 C.原子光谱 D.核磁共振谱
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com