
19.(11分)A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素原子的最外层电子数是其电子层数的3倍,C元素原子的M能层的p能级有3个未成对电子,D元素原子核外的M能层中只有2对成对电子。
请回答下列问题:
(1)当n=2时,AB2属于 分子(填“极性”或“非极性”),分子中
有 个σ键、 个π键。
(2)当n=3时,A与B形成的晶体属于 晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种原子的电负性由大到小的顺序是 (用元素符号表示)。
(4)已知某红紫色配合物的组成为CoCl3·5NH3·H2O。该配合物中的中心离子钴离子在基态时的核外电子排布式为 ,作为配位体之一的NH3分子的空间构型为 。
18.(10分)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1)
|
元素代号 |
I1 |
I2 |
I3 |
I4 |
|
Q |
2080 |
4000 |
6100 |
9400 |
|
R |
500 |
4600 |
6900 |
9500 |
|
S |
740 |
1500 |
7700 |
10500 |
|
T |
580 |
1800 |
2700 |
11600 |
|
U |
420 |
3100 |
4400 |
5900 |
请回答下列问题:
(1)在周期表中,最可能处于同一族的是
A.Q和R B.S和T
C.T和U D.R和U
(2)电解它们的熔融氯化物,阴极电极反应式最可能正确的是
A.U2++2e-→U B.R2++2e-→R
C.S3++3e-→S D.T3++3e-→T
(3)它们的氯化物的化学式,最可能正确的是
A.UCl4 B. RCl
C.SCl3 D.TCl
(4)S元素最可能是
A.s区元素 B.p区元素
C.过渡金属 D.d区元素
(5)下列元素中,化学性质和物理性质最像Q元素的是
A.硼(1s22s22p1) B.铍(1s22s2)
C.锂(1s22s1) D.氦(1s2)
17.下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数, Y为元素的有关性质)。下列有关说法错误的是
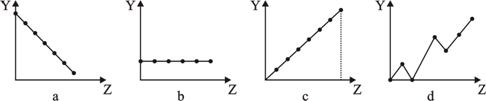
A.a图表示第三周期元素的原子半径(稀有气体除外)
B.b图表示ⅡA族元素的最外层电子数
C.c图表示第三周期元素的最高化合价
D.d图表示第三周期元素单质的熔沸点
第Ⅱ卷
16.根据中学化学教材所附元素周期表判断,下列叙述不正确的是
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有短周期元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
15.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法不正确的是
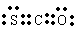 A.羰基硫属于极性分子
A.羰基硫属于极性分子
B.羰基硫的电子式为:
C.羰基硫沸点比CO2低
D.羰基硫分子中三个原子处于同一直线上
14.X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,下列判断错误的是
A.X的电负性大于Y的电负性
B.X的原子半径大于Y的原子半径
C.X的氧化性大于Y的氧化性
D.X的第一电离能大于Y的第一电离能
13.第3周期元素的原子,其最外层3p亚层上有一个未成对电子,它的最高价氧化物对应水化物的酸根离子可能是
A.RO5- B.RO3- C.RO42- D.RO4-
12.在乙烯分子中有5个σ键、1个π键,它们分别是
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键
D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键
11.根据键能数据估算CH4 (g)+4F2 (g)=CF4(g)+4HF(g)的反应热ΔH为
|
化学键 |
C-H |
C-F |
H-F |
F-F |
键能/(kJ·mol ) ) |
414 |
489 |
565 |
155 |
A.–1940 kJ · mol-1 B.1940 kJ · mol-1
C.–485 kJ · mol-1 D.485 kJ · mol-1
10.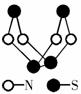 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是
A.该物质的分子式为SN
B.该物质的分子中既有极性键又有非极性键
C.该物质具有很高的熔、沸点
D.该物质与化合物S2N2互为同素异形体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com