
11ЃЎЪЏФЋФмгыШлШкН№ЪєМизїгУЃЌаЮГЩЪЏФЋМфЯЖЛЏКЯЮяЃЌKдзгЬюГфдкЪЏФЋИїВуЬМдзгжаЁЃБШНЯГЃМћЕФЪЏФЋМфЯЖЛЏКЯЮяЪЧЧрЭЩЋЕФЛЏКЯЮяЃЌЦфЛЏбЇЪНПЩаДГЩCxKЃЌЦфЦНУцЭМаЮМћЯТЭМЃЌдђxжЕЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
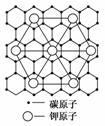
AЃЎ8ЁЁBЃЎ12ЁЁCЃЎ24ЁЁDЃЎ60
[НтЮі]ЁЁвдШ§ИіМидзгаЮГЩЕФаЁШ§НЧаЮЮЊМЦЫуЕЅЮЛЃЛЦфЭъШЋеМгаЕФЬМдзгЪ§ЮЊ4ЃЛеМгаЕФМидзгЮЊЁС3ЃНЃЌЙЪдзггыМидзгИіЪ§БШЮЊ8?1ЁЃ
[Д№АИ]ЁЁA
10ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎЖўбѕЛЏЬМЗжзгжаДцдкЙВМлМќКЭЗжзгМфзїгУСІ
BЃЎМзЭщЁЂАБКЭЫЎЖМЪЧгЩМЋадМќНсКЯЖјГЩЕФМЋадЗжзг
CЃЎЭЌжїзхВЛЭЌдЊЫиЕФзюИпМлбѕЛЏЮяЃЌвЛЖЈОпгаЯрЭЌЕФОЇЬхНсЙЙ
DЃЎЗњЛЏЧтЕФЗаЕуИпгкТШЛЏЧтЕФЗаЕуЃЌе§ЖЁЭщЕФЗаЕуИпгквьЖЁЭщЕФЗаЕу
[НтЮі]ЁЁЗжзгМфзїгУСІДцдкгкЗжзгМфЃЌCH4ЪєЗЧМЋадЗжзгЃЌCO2ЁЂSiO2ЕФОЇЬхРраЭВЛЭЌЁЃ
[Д№АИ]ЁЁD
9ЃЎЙВМлМќЁЂРызгМќКЭЗЖЕТЛЊСІЖМЪЧСЃзгжЎМфЕФВЛЭЌзїгУСІЃЌЯТСаЮяжЪЭЌЪБКЌгаЩЯЪіСНжжзїгУСІЕФзщКЯЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
ЂйNa2O2ЁЁЂкSiO2ЁЁЂлЪЏФЋЁЁЂмН№ИеЪЏЁЁЂнNaClЁЁЂоАзСз
AЃЎЂйЂкЂм ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁBЃЎЂйЂлЂо
CЃЎЂкЂмЂо ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁDЃЎЂлЂмЂн
[НтЮі]ЁЁNa2O2жаNa+гыOжЎМфвдРызгМќНсКЯЃЌOжаO-OвдЙВМлМќНсКЯЃЌЗћКЯЬѕМўЃЛЪЏФЋжаУПвЛВуФквдЬМЬММќНсКЯЃЌВугыВужЎМфвдЗжзгМфзїгУСІНсКЯЃЌЗћКЯЬѕМўЃЛАзСз(P4)ЗжзгФкP-PвдЙВМлМќНсКЯЃЌЖјP4ЗжзгжЎМфвдЗжзгМфСІНсКЯЃЌвВЗћКЯЬтвтЃЛSiO2ЁЂН№ИеЪЏжЛгаЙВМлМќЃЌЮЊдзгОЇЬхЃЌNaClжажЛгаРызгМќЁЃ
[Д№АИ]ЁЁB
8ЃЎЯТСаИїзщЮяжЪЕФОЇЬхжаЃЌЛЏбЇМќРраЭЯрЭЌЃЌОЇЬхРраЭвВЯрЭЌЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎSiO2КЭSO2ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎCO2КЭH2O
CЃЎNaClКЭHClЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎCCl4КЭKCl
[НтЮі]ЁЁSiO2ЪЧЙВМлМќаЮГЩЕФдзгОЇЬхЃЌSO2ЪЧЙВМлМќаЮГЩЕФЗжзгОЇЬхЃЌAДэЃЛCO2КЭH2OОљЮЊЙВМлМќЃЌЖјЧвЪЧЗжзгОЇЬхЃЌBЖдЃЛNaClЪЧРызгМќаЮГЩЕФРызгОЇЬхЃЌHClЪЧЙВМлМќаЮГЩЕФЗжзгОЇЬхЃЌCДэЃЛCCl4ЪЧЙВМлМќаЮГЩЕФЗжзгОЇЬхЃЌKClЪЧРызгМќаЮГЩЕФРызгОЇЬхЃЌDДэЁЃ
[Д№АИ]ЁЁB
7ЃЎЕЊЛЏЙш(Si3N4)ЪЧвЛжжаТаЭЕФФЭИпЮТФЭФЅЫ№ВФСЯЃЌдкЙЄвЕЩЯгаЙуЗКгУЭОЃЌЫќЪєгк(ЁЁ)
AЃЎдзгОЇЬхЁЁ BЃЎЗжзгОЇЬх
CЃЎН№ЪєОЇЬхЁЁ DЃЎРызгОЇЬх
[НтЮі]ЁЁФЭИпЮТФЭФЅЫ№ЫЕУїШлЕуИпЃЌгВЖШДѓЃЌвђДЫЪЧдзгОЇЬхЁЃ
[Д№АИ]ЁЁA
6ЃЎNaFЁЂNaIЁЂMgOОљЮЊРызгОЇЬхЃЌЯжгаЯТБэЫљЪОЪ§ОнЃЌЪдХаЖЯетШ§жжЛЏКЯЮяШлЕугЩИпЕНЕЭЕФе§ШЗЫГађЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
|
ЮяжЪ |
ЂйNaF |
ЂкNaI |
ЂлMgO |
|
РызгЕчКЩЪ§ |
1 |
1 |
2 |
|
МќГЄ/(10Ѓ30m) |
2.31 |
3.18 |
2.10 |
A.ЂйЃОЂкЃОЂлЁЁЁЁЁЁЁЁBЃЎЂлЃОЂйЃОЂк
CЃЎЂлЃОЂкЃОЂйЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁDЃЎЂйЃОЂкЃОЂл
[Д№АИ]ЁЁB
5ЃЎЯТСаИїЮяжЪжаЃЌАДШлЕугЩИпЕНЕЭЕФЫГађХХСае§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎCH4>SiH4>GeH4>SnH4
BЃЎKCl>NaCl>MgCl2>MgO
CЃЎRb>K>Na>Li
DЃЎЪЏФЋ>Н№ИеЪЏ>SiO2>ФЦ
[Д№АИ]ЁЁD
4ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎдзгОЇЬхжажЛДцдкЗЧМЋадЙВМлМќ
BЃЎЯЁгаЦјЬхаЮГЩЕФОЇЬхЪєгкЗжзгОЇЬх
CЃЎИЩБљЩ§ЛЊЪБЃЌЗжзгФкЙВМлМќЛсЗЂЩњЖЯСб
DЃЎН№ЪєдЊЫиКЭЗЧН№ЪєдЊЫиаЮГЩЕФЛЏКЯЮявЛЖЈЪЧРызгЛЏКЯЮя
[Д№АИ]ЁЁB
3ЃЎЯТСаЫЕЗЈДэЮѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎЖўбѕЛЏЬМКЭЖўбѕЛЏЙшЖМЪєгкдзгОЇЬх
BЃЎЗжзгОЇЬхЕФзДЬЌБфЛЏЃЌжЛашПЫЗўЗжзгМфзїгУСІ
CЃЎН№ЪєОЇЬхЭЈГЃОпгаЕМЕчЁЂЕМШШКЭСМКУЕФбгеЙад
DЃЎРызгОЇЬхдкШлЛЏзДЬЌЯТФмЕМЕч
[Д№АИ]ЁЁA
2ЃЎЯТСагаЙиЛЏбЇМќгыОЇЬхНсЙЙЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ)
AЃЎСНжждЊЫизщГЩЕФЗжзгжавЛЖЈжЛгаМЋадМќ
BЃЎРызгЛЏКЯЮяЕФШлЕувЛЖЈБШЙВМлЛЏКЯЮяЕФИп
CЃЎЗЧН№ЪєдЊЫизщГЩЕФЛЏКЯЮявЛЖЈЪЧЙВМлЛЏКЯЮя
DЃЎКЌгавѕРызгЕФЛЏКЯЮявЛЖЈКЌгабєРызг
[Д№АИ]ЁЁD
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com