
34.燕麦的颖色受两对等位基因(B-b,Y-y)控制,有黑色B__ __ __,黄色bbY__,白色bbyy三种类型,现有黑颖(甲)和黄颖(乙)两纯合亲本杂交,F1全为黑颖,F1自交后,F2为黑莹;黄颖;白颖=12:3:1。请回答下列问题:
(1)两纯合亲本基因型为:甲__________,乙___________。
(2)请问这两对等位基因是否位于两对同源染色体上?__________,(填“是”或“不是”)并用遗传图解进行解释。
(3)若F1与白颖燕麦杂交,则子代性状分离比为__________________。
(4)若基因型为BBYY的燕麦具有更强的抗逆性和更高的蛋白质含量,下面是利用甲、乙两亲本培育出此品种的育种方案,请补充完整。
育种过程:
①杂交,得到F1:BbYy(黑颖);
②取F1配子→____________→单倍体幼苗→___________→纯系植株;
③随机选取黑颖植株并编号,其基因型为_____________,选取后,每株的部分种子留存,部分种子种值,并与白颖植株杂交,得F3;
④将F3自交,观察后代性状分离情况,若后代______________,则原黑颖植株所界种子即为BBYY;否则应淘汰。



33.在2009年下半年,我国许多地区发生甲型H1N1流感疫情。甲型H1N1流感病毒对热,消毒剂敏感,而对干燥和低温的抵抗力强。其核酸由8个片段组成,分别编码10种蛋白质。下图表示其活动周期,A、B表示物质,请据图回答:
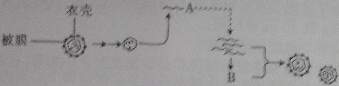
(1)该病毒由________外壳(衣壳)和__________组成。被膜中含有病毒融合蛋白,它在病毒进入宿主细胞时起关键作用。
(2)能正确表示病毒侵入机体后,引起血液中抗体浓度变化的是(①表示第一次感染,②表示第二次感染)_______________。
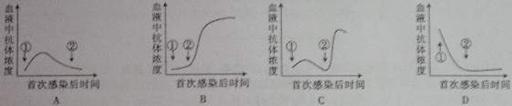
(3)根据病毒入侵机体后引起血液中抗体浓度变化的规律,为提高人体对病毒预防能力,应采取的措施是向人体注射__________。
A.疫苗 B.抗体 C.抗生素 D.抗病毒药物
(4)接种过甲型H1N1流感疫苗的健康人在一段时间内也可能再次感染甲型H1N1流感,其原因可能是______________________________。B淋巴细胞和T淋巴细胞依靠细胞膜表面的____________识别抗原。
(5)机体能合成数百万种特异性抗体,抗体种类如此多的原因是其分子结构中的_______
_______________________不同。
32.果实成熟到一定程度死时,乙烯含量明显上升。研究表明;果实中乙烯含量的增加与呼
吸速率上升的时间进程一致。某实验小组探究不同浓度的乙烯对果实呼吸作用的影响得
到如甲图所示的结果:
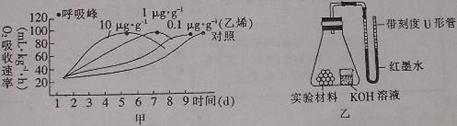
(1)实验表明:
①随乙烯浓度增大,呼吸峰出现的时间将_______;
②随乙烯浓度增大,呼吸峰的强度将__________。
(2)试利用图乙实验装置设计实验,验证实验小组的探究结果。
材料:未成熟的小番茄。
试剂:20%KOH溶液、红墨水、蒸馏水、不同浓度的乙烯利溶液(实验提示:乙烯利溶液浸泡果实1min,在细胞液的pH条件下能缓慢分解释放出乙烯,具有与乙烯相同的生理效应。每隔一定时间,利用该装置测定1h,计算呼吸速率)。
步骤:
①___________________________________________________________________;
②___________________________________________________________________;
③___________________________________________________________________;
(3)研究表明乙烯能增加果皮细胞通透性,试推测乙烯促进果实成熟的原因:_______
_____________________________________。
31.2008年11月,巫山县渝东珍稀植物园负责人透露;两个月前,该园的镇园之宝--最高的一株珍稀龙舌兰根部腐烂,叶子萎蔫、干枯。经植物专家全面体检和精心治疗,目前这株2.3m高的龙舌兰已经重现生机。请回答下列相关问题:
(1)专家认为该龙舌兰患病是雨下得太多造成的。用高中生物知识对此进行简要解释,可以表示为如下图解:
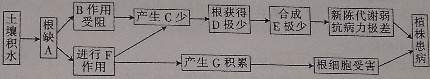
若图解中E代表蛋白质等有机物,则A代表的物质是_______,C代表的物质是______,D代表的物质是________,物质G是指根细胞产生的_________。
(2)在对症治疗上,除了挖沟排水外,专家还为龙舌兰建立了保温室。因为龙舌兰本是热带植物,其_______性决定了温室有利于其康复。温室使它的________提高。加快了新陈代谢的进行。
(3)在第十一届全国运动会开幕前夕,预在济南奥体中心场馆周围建设龙舌兰绿化带,需对该龙舌兰叶肉细胞进行组织培养,达到快速繁殖的目的。
①这种组织培养依据的原理是_______________,属于___________生殖类型。
②在得到该龙舌兰的_________后,经过消毒就可以在培养基上进行培养。在人工合成的培养基中,__________是龙舌兰细胞脱分化及再分化不可缺少的调节物质。
30.有机物A能发生如图所示的转化。A-F六种物质的均含有苯环,其中C能使溴的四绿化碳溶液褪色且不能发生银镜反应;D不含甲基,在一定条件下能发生消去反应。
请回答下列问题:
(1)A分子中含氧官能团的名称为___________,C的结构简式为_________。
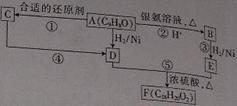 (2)C-→D的反应类型为________(填字母,下同)。
(2)C-→D的反应类型为________(填字母,下同)。
a.氧化反应 b.还原反应
c.加成反应 d.取代反应
(3)反应②中银氨溶液还可以用______代替。
A.酸性KMnO4溶液 B.溴水
C.氨水 D.新制Cu(OH)2悬浊液
(4)A-F六种化合物中能与金属钠反应,但不能与氢氧化钠溶液反应的是______(填字母)。
(5)反应⑤的化学方程式为________________________。
(6)能与FeCl3溶液发生显色反应,苯环上有2个取代基,且与D互为同分异构体的有机物有_________种。
29.由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH4+、Mg2+、Ba2+、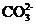 、
、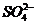 。将该混合物溶于水后得澄清溶液,现取三粉100mL该溶液分别进行如下实验:
。将该混合物溶于水后得澄清溶液,现取三粉100mL该溶液分别进行如下实验:
|
实验序号 |
实验内容 |
实验结果 |
|
1 |
加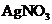 溶液 溶液 |
有白色沉淀生成 |
|
2 |
加足量NaOH溶液并加热 |
收集到气体1.12L(已折算成标准状况下的体积) |
|
3 |
加足量BaCl2溶液,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27g,第二次称量读数为2.33g |
请回答下列问题:
(1)根据实验1对Cl-是否存在的判断是___________(填“一定存在”、“一定不存在”或“不能确定”);根据实验1-3判断原混合物中一定不存在的离子是________________。
(2)试确定溶液中一定在的阴离子及其物质的量浓度(可不填满);
|
阴离子符号 |
物质的量浓度(mol·L-1) |
|
|
|
|
|
|
|
|
|
(3)试确定K+是否存在?________,判断的理由是_________________________________
______________________________________________。
28.已知V、W、X、Y、Z五种周期元素在周期表中的位置如图所示,W的气态氢化物
 与Z的气态氢化物的反应只能生成一种盐,请回答下列问题:
与Z的气态氢化物的反应只能生成一种盐,请回答下列问题:
(1)X在元素周期表中的位置为________________。
(2)Y、Z两种元素的简单离子的半径大小关系是____________(用离子符号表示)。
(3)W、Y的最高价氧化物对应的水化物的浓溶液均能与金属铜发生反应,写出有关的化学方程式:_______________________、____________________________。
(4)五种元素的最简单氢化物中,沸点最高的是____________(填化学式)。
(5)由五种元素组成的中学化学常见单质及化合物中,涉及的晶体类型有_________。
A.离子晶体 B.分子晶体 C.金属晶体 D.原子晶体
(6)Y2Z2分子中,Y与Z均满足8e-稳定结构,则Y2Z2的电子式为______________。
27.无水氯化铜为棕色固体,熔点为498℃,在空气中易潮解变质,实验室可用铜粉与氯气反应制得。现有以下药品,①NaOH溶液 ②CuO粉末 ③Cu粉 ④MnO2粉末 ⑤浓盐酸 ⑥浓硫酸 ⑦浓硝酸请从下图中选用所需的仪器(可重复选用)组成一套制取CuCl2的装置(连接和固定仪器用的玻璃导管、胶管,铁夹,铁架台及加热装置均略去)。
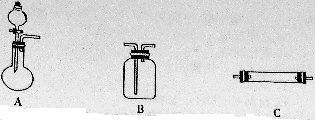
将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中所加试剂的名称及其作用;
|
选用的仪器(填字母) |
加入的试剂 |
作用 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
26.如图所示,与竖直方向的夹角为45°的直线边界左下方有一正交的匀强电、磁场、磁场方向垂直于纸面向里。磁感应强度大小为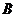 ,电场方向竖直向上,场强大小为
,电场方向竖直向上,场强大小为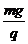 ,一质量为
,一质量为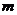 电荷量为
电荷量为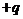 的小球从边界上
的小球从边界上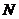 点正上方高为
点正上方高为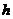 处的
处的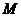 点静止释放,下落到
点静止释放,下落到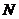 点时小球瞬间爆炸成质量、电荷量均相等的
点时小球瞬间爆炸成质量、电荷量均相等的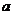 、
、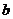 两快(不计爆炸过程中的质量损失),已知爆炸后
两快(不计爆炸过程中的质量损失),已知爆炸后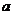 向上运动,能达到的最大高度为
向上运动,能达到的最大高度为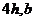 向下运动进入电、磁场区域,求。
向下运动进入电、磁场区域,求。
(1)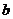 刚进入电、磁场时的速度大小
刚进入电、磁场时的速度大小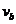
(2)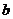 第二次进入电、磁场区域时的速度大小
第二次进入电、磁场区域时的速度大小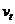
(3)设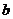 第二次进入电,磁场时,它与边界
第二次进入电,磁场时,它与边界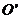 的交点为
的交点为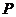 ,求
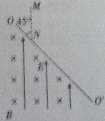
,求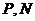 之间的距离
之间的距离
25.如图所示,两个圆形光滑细管在竖直平面内交叠,组成“8”字形通道,在“8”字形通道顶端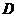 处连接一内径相同的光滑水平管
处连接一内径相同的光滑水平管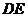 ,而在“8”字形通道底部
,而在“8”字形通道底部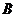 处连结一内径相同的粗糙水平直管
处连结一内径相同的粗糙水平直管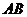 ,已知
,已知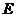 处距地面的高度
处距地面的高度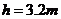 ,一质量
,一质量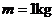 的小球
的小球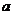 从A点以
从A点以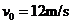 的速度向右进入直管道,到达
的速度向右进入直管道,到达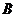 点后沿“8”字形轨道向上运动,到达
点后沿“8”字形轨道向上运动,到达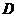 点时恰能进入
点时恰能进入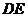 管,并与原来静止于
管,并与原来静止于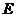 处的质量
处的质量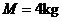 的小球
的小球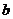 发生正碰(
发生正碰(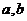 均可视为质点)。已知碰撞后
均可视为质点)。已知碰撞后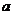 球沿原路返回,速度大小为碰前速度大小的
球沿原路返回,速度大小为碰前速度大小的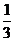 ,而
,而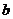 球从
球从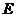 点水平抛出,其水平射程
点水平抛出,其水平射程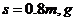 取
取
(1)求“8”字形管道上下两圆的半径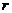 、R。
、R。
(2)若小球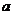 在管道
在管道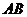 中运动时所受阻力为定值,请判断
中运动时所受阻力为定值,请判断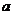 球返回到
球返回到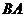 管道中时能否从
管道中时能否从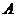 端穿出。
端穿出。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com