
3.读算法语句,输入a,b,c
If a > b Then m = a
Else m = b
If m > c Then输出m
Else m = c
输出m
End
若输入10,8,6,则运算结果为 ( )
A.10 B.8 C.6 D.10,8,6
2.设向量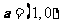 ,
,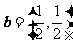 ,则下列结论中正确的是
( )
,则下列结论中正确的是
( )
A.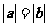 B.
B.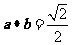
C. 与
与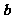 垂直
D.
垂直
D.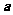 ∥
∥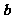
1.若集合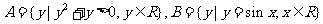 ,则
,则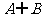 = ( )
= ( )
A.R B. C.
C. D.
D.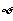
22.(9分)“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有: 。(填字母)
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能.风能
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
a.6CO2 + 6H2O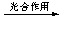 C6H12O6+6O2 b.CO2 + 3H2
C6H12O6+6O2 b.CO2 + 3H2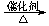 CH3OH
+H2O
CH3OH
+H2O
c.CO2 + CH4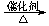 CH3COOH d.2CO2
+ 6H2
CH3COOH d.2CO2
+ 6H2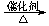 CH2==CH2
+ 4H2O
CH2==CH2
+ 4H2O
以上反应中,最节能的是 ,原子利用率最高的是 。
(3)文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:
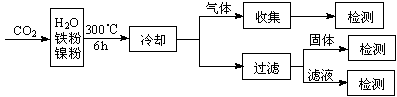
反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。CH4.HCOOH.H2的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):
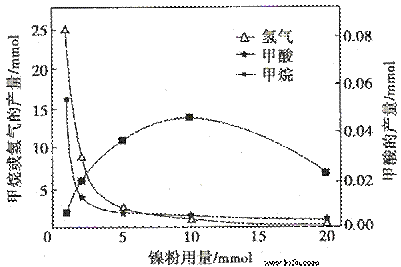
研究人员根据实验结果得出结论:
HCOOH是CO2转化为CH4的中间体,即:CO2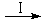 HCOOH
HCOOH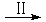 CH4
CH4
①写出产生H2的反应方程式 。
②由图可知,镍粉是 。(填字母)
a.反应Ⅰ的催化剂 b.反应Ⅱ的催化剂
c.反应Ⅰ.Ⅱ的催化剂 d.不是催化剂
③当镍粉用量从1 mmol增加到10 mmol,反应速率的变化情况是 。(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应Ⅰ.Ⅱ的速率均不变
d.反应Ⅰ.Ⅱ的速率均增加,且反应Ⅰ的速率增加得快
e.反应Ⅰ.Ⅱ的速率均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
21.(8分)燃烧法是测定有机化合物化学式的一种重要方法。在一定温度下取0.1 mol某气态烃A在O2中完全燃烧,生成CO2和水蒸气,放出热量Q kJ,将生成物依次通过浓硫酸和碱石灰,浓硫酸增重7.2 g,碱石灰增重17.6 g。将烃A加入酸性KMnO4溶液或Br2的CCl4溶液,均能使它们褪色。
(1)写出烃A的分子式 ;
(2) 已知烃A分子结构高度对称且有两个甲基,请写出烃A的结构简式 ;
(3)写出烃A使Br2的CCl4溶液褪色的化学方程式 ;
(4)烃A在一定条件下可以通过加聚反应合成一种塑料,则该反应的化学方程式是
。
20.(9分)实验室用如图所示的装置制取乙酸乙酯.
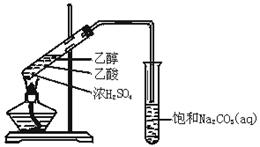
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合溶液的方法是: ,然后轻轻振荡试管,使之混合均匀。
(2)装置中通蒸气的导管要插在饱和Na2CO3溶液的液面上,不能插入溶液中,目的是防止Na2CO3溶液的倒吸、造成倒吸的操作上的原因是 。
(3)浓硫酸的作用是① ; ② .
(4)饱和Na2CO3溶液的作用是 。
(5)乙酸乙酯的密度比水 (填“大”或“小”),有 味.
(6)若实验中温度过高,使反应温度达到140℃左右时,副反应的主要有机产物是
(填物质名称).
19.(8分)以乙烯为原料合成化合物C的流程如下所示:

(1)写出A的结构简式 。
(2)反应①④的反应类型分别为 . 。
(3)写出反应②和④的化学方程式:
② ;④ 。
18.(12分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语
回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X.Y.Z.M.N可发生以下反应:

X溶液与Y溶液反应的离子方程式为_______________________________,
N→⑥的单质的化学方程式为______________________________________。
17.(6分)请选择合适方法的字母代号填空
(1)从煤焦油中提取二甲苯
(2)从海水中提取粗盐
(3)丁烷转变为乙烷和乙烯
(4)从铁矿石中提取金属铁
(5)煤转化为焦炭.煤焦油等
(6)提纯氢氧化铁胶体(除去其中的杂质离子)
A.过滤 B.裂解 C.分馏 D.裂化 E.干馏 F.还原 G.电解 H.渗析
I.蒸发 J.氧化
16.已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1 mol H-H键断裂时吸收热量为 ( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com