
13.用惰性电极电解一定量的硫酸铜溶液,实验装置如图①。电解过程中的实验数据如图②, 横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积 (标准状况)。则下列说法正确的是 ( )

A.电解过程中,b电极表面先有红色物质析出,后有气泡产牛
B.a电极上发生的反应方程式为:2H++2e-一H2↑和4OH--4e-==2H2O十O2↑
C.曲线0-P段表示H2和O2混合气体的体积变化,曲线P-Q段表示O2的体积变化
D.从开始到Q点时收集到的混合气体的平均摩尔质量为17g·mol-1
12.一定温度下,lmol X和n mol Y在锌积为2L的密闭容器中发生如下反应:
X(g)+Y(g) 2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是 ( )
2Z(g)+M(s),5min后达到平衡,此时生成2a mol Z。下列说法正确的是 ( )
A.用X表示此反应的反应速率是(0.1-0.2a)mol·(L·min)-1
B.向l平衡后的体系中加入lmol M,平衡向逆反应方向移动
C.当混合气体的质量不再发生变化时,说明反应达到平衡状态
D.向上述平衡体系中再充入lmol X,v(正)增大,v(逆)减小,平衡正向移动
11.乙酸乙酯的制备实验中,得到乙酸乙酯、乙酸和乙醇的混合物。下列有关分离、提纯的方法可行的是 ( )
A.在混合物中继续加入浓硫酸、加热可得到纯净的乙酸乙酯
B.先加入氢氧化钠浓溶液,再进行蒸馏可得到乙酸乙酯
C.先加入饱和碳酸钠溶液,再进行分液可得到乙酸乙酯
D.分离出乙酸乙酯后的混合液,可继续用分液漏斗分离乙酸和乙醇
9.下列说法正确的是 ( )
A.pH=2和pH=l的硝酸中c(H+)之比为10:1
B.一元酸与一元碱恰好完全反应后的溶液中一定存在c(H+)=c(OH-)
C.KAl(SO4)2溶液中离子浓度的大小顺序为
c(SO2-4)>c(K+)>c(Al3+)>c(H+)>c(OH-)
D.常温下,将pH均为12的氨水和NaOH溶液分别加水稀释100倍后,NaOH溶液的 pH较大
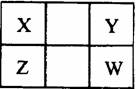 10.已知X、Y、Z、W是四种短周期非金属元素,在周期表中的
10.已知X、Y、Z、W是四种短周期非金属元素,在周期表中的
相对位置如下图所示,下列说法不正确的是 ( )
A.Z元素的最高化合价可能比Y元素的高
B.X、Y、Z、W的氢化物中,X的氢化物沸点可能最低
C.Z的单质为原子晶体时,W的单质可能为分子晶体
D.X的最高价氧化物对应水化物与其氢化物不可能相互反应
8. 某电解质溶液中可能大量存在H+、Mg2+、CO2-3、OH-、Cl-等离子中的几种,下列有关说法正确的是 ( )
某电解质溶液中可能大量存在H+、Mg2+、CO2-3、OH-、Cl-等离子中的几种,下列有关说法正确的是 ( )
A.一定没有Mg2+、CO2-3、OH- B.一定有Cl-
C.还需要进一步确认的离子是H+、Cl- D.无法判断
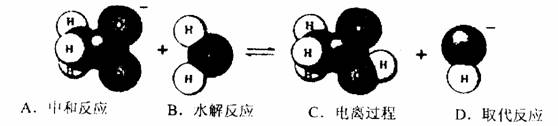
7.下图表示某物质发生的是 ( )
6.下列说法正确的是 ( )
A.棉花、木材及草类的纤维都足天然纤维
B.所有分散系的分散质粒子都能透过半透膜
C.16O与18O互为同素异形体
D.H2、D2、T2互为同位素
12.(2010年河南中考模拟题4)解不等式组: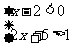
答案:解:由<1>解得: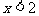 , 由<2>解得:
, 由<2>解得:
因此原不等式组的解集为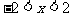 。
。
11.(2010年河南中考模拟题2) 求不等式组 的整数解。
答案:解不等式组得-1<x≤3,即整数解为0、1、2、3
10.(2010年江西省统一考试样卷)请从下列四个不等式中,选择其中两个组成一个你喜欢的不等式组,并求出 它的解集.
它的解集.
①1-x<0;
②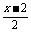 <1; ③2x+3>1; ④2(x+2)-1<3.
<1; ③2x+3>1; ④2(x+2)-1<3.
解:答案不惟一,任意两个不等式都可组成不等式组的形式.例如:
选①②组成的不等式组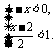
由不等式1-x<0,解得x>1.
由不等式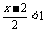 ,解得x<4.
,解得x<4.
 ∴选做的不等式组的解集是1<x<4.
∴选做的不等式组的解集是1<x<4.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com