
4.ABCDE五人排成一行,A与C不相邻的概率为( )
A.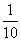 B.
B. C.
C.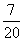 D.
D.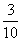
3.若函数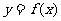 的图象与函数
的图象与函数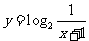 的图象关于
的图象关于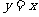 对称,则
对称,则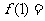 ( )
( )
A.1 B.-1 C.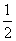 D.
D.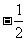
2.已知单位向量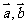 满足
满足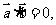 则
则 的值为( )
的值为( )
A.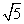 B.5 C.1 D.
B.5 C.1 D.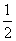
1.已知集合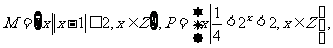 则
则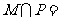 ( )
( )
A.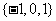 B.
B.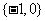 C.
C.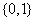 D.
D.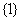
19.100多年来科学家没有间断对纯氮物种的研究和发现。第一次是 1772年分离出N2,第二次是1890年合成了重氮离子,1999年是高能氮阳离子,甚至科学家预计能合成N8。
⑴.1890年合成的重氮离子(N3-)中有一个氮氮三键,请写出其电子式 。
⑵.经分析,1999年合成的高能氮阳离子中有5个氮原子,它们成V字形,且含有2个氮氮叁键,每个氮原子最外层均达到8电子稳定结构,试推断该离子所带的电荷数为 ,写出其电子式和结构式
。
⑶.请你预计科学家即将合成的N8的电子式 以及它的结构式 ;N8属于 (填写“单质”、“共价化合物”、“离子化合物”);其含有的化学键有
;预计它在常温下是 体,熔沸点 ,熔融状态下 (会、不会)导电。
18.已知HCN是一种极弱酸,其电离产生的CN-离子能与人体血红蛋白中心离子Fe2+结合,因而有剧毒。通常Fe2+、Fe3+均易与CN-形成络离子:[Fe(CN)6]3-、[Fe(CN)6]4-,其中[Fe(CN)6]3-在中性条件下能发生水解,生成Fe(OH)3。试回答下列问题:
⑴.写出HCN分子的结构式_________,电子式___ __________;
⑵.[Fe(CN)6]3-在中性条件下水解可生成Fe(OH)3,同时还能生成的微粒有_ __、_____。
17. 下列物质结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键。示例:
下列物质结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键。示例:

根据各图表示的结构特点,写出该分子的化学式:
A_______________,B______________,C_______________,D____________。
16、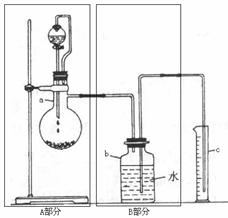 某探究学习小组用下面这套装置测定乙醇结构:已知乙醇的分子组成为C2H6O,为探究其结构式究竟是以下(Ⅰ)式还是(Ⅱ)式中的哪一种,该小组同学利用乙醇与金属钠的反应进行如下探究:
某探究学习小组用下面这套装置测定乙醇结构:已知乙醇的分子组成为C2H6O,为探究其结构式究竟是以下(Ⅰ)式还是(Ⅱ)式中的哪一种,该小组同学利用乙醇与金属钠的反应进行如下探究:
(Ⅰ)
(Ⅱ)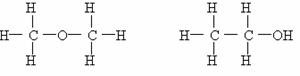
① 所测得的一组实验数据如下:
|
第一记录项 |
第二记录项 |
第三记录项 |
|
实验次数 |
取用乙醇的物质的量 |
与足量钠反应产生氢气的体积(换算成标准状况) |
|
第1次 |
0.020mol |
0.223L |
|
第2次 |
0.010mol |
0.114L |
|
第3次 |
0.010mol |
0.111L |
他们根据以上数据推断乙醇的合理结构不应是 式(填写“I”或“II”),理由为:
。
② 从实验的实际过程中,该组同学体会到,他们的数据记录方式存在科学性问题,即记录的不是原始数据而是换算数据。你认为表中的第二记录项应改为
,第三记录项应改为 ,为使实验记录更加科学、准确,还应增加的一个实验记录项是
。
15、已知反应:① H2+Cl2=2HCl;② H2+Br2=2HBr。试利用下表中数据进行计算,等物质的量的H2分别与足量的Cl2、Br2反应,反应 (填写反应序号)释放的能量多;由计算结果说明,HCl、HBr分子中, 更容易受热分解生成对应的两种单质。
|
键 |
H—H |
Cl—Cl |
Br—Br |
H—Cl |
H—Br |
|
键能/kJ·mol-1 |
436.0 |
242.7 |
193.7 |
431.8 |
366.0 |
14、向盛有CuSO4水溶液的试管里加入氨水,首先看到溶液中生成 色沉淀,其化学式为 ,溶液颜色由 色逐渐消失;继续滴加氨水,看到沉淀会逐渐 ,得到 色的透明溶液;再加入适量的乙醇,将析出深蓝色的晶体。加乙醇前的溶液和加乙醇后析出的深蓝色晶体中均含有阳离子的化学式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com