
1.下列加点字注音全都正确的一组是
A.偌大(ruò) 焖饭(mèn) 强颜欢笑(qiǎng) 精神萎靡(mǐ)
B.央浼(miǎn) 绮丽(qǐ) 韦编三绝(wéi) 谆谆教导(zhūn)
C.漱口(shù) 克扣(kē) 嘉言懿行(yì) 顺蔓摸瓜(wàn)
D.豢养(huàn) 卡壳(qiǎ) 怅望低徊(huái) 拾级而上(shè)
28.(14分)近年来,碳和碳的化合物在生产生活实际中应用广泛。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知 ① 2 CH4 (g) + 3O2 (g) = 2 CO (g) + 4 H2O(l) △H1 = -1214.6 KJ/mol
② 2 CO (g) + O2(g) = 2 CO2 (g) ΔH2 = -566 kJ/mol
则反应CH4(g) + 2 O2 (g) = CO2 (g) + 2 H2O (l) 的△H = 。
(2)将两个石墨电极插人KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。通入CH4的一极,其电极反应式是:CH4 + 10 OH―― 8e-= CO32-+ 7 H2O;通入O2的一极,其电极反应式是 。
(3)若用石墨做电极电解500 ml饱和食盐水,写出电解反应的离子方程式为: ;电解一段时间后两极共收集到标准状况下的气体1.12 L(不考虑气体的溶解)。停止通电,假设反应前后溶液体积不变,则所得溶液的pH= 。
 (4)将不同量的CO (g) 和H2O (g) 分别通入到体积为2 L的恒容密闭容器中,进行反应
(4)将不同量的CO (g) 和H2O (g) 分别通入到体积为2 L的恒容密闭容器中,进行反应
CO (g) + H2O (g) CO2 (g) + H2 (g),得到如下三组数据:
|
实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所 需时间/min |
||
|
H2O |
CO |
CO2 |
CO |
|||
|
1 |
650 |
2 |
4 |
1.6 |
2.4 |
5 |
|
2 |
900 |
1 |
2 |
0.4 |
1.6 |
3 |
|
3 |
900 |
a |
b |
c |
d |
t |
① 实验1中以υ(H2) 表示的反应速率为 。
② 实验2中的平衡常数是 (计算结果保留两位小数)。
③ 该反应的正反应为 (填“吸”或“放”)热反应。
④ 若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),
则a、b应满足的关系是 (用含a、b的数学式表示)。
27.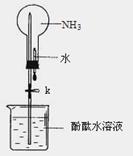 (16分)氨是一种重要的化工原料,某学习小组欲制取氨气并探究其性质。请回答:
(16分)氨是一种重要的化工原料,某学习小组欲制取氨气并探究其性质。请回答:
(1)实验室制取氨气的化学方程式是 。
(2)①右图是进行氨气喷泉实验的装置,引发喷泉的操作步骤是 。
②氨气使烧杯中溶液由无色变为红色,其原因是_______________________________(用电离方程式表示)。
(3)该小组同学设计了下图所示的实验装置(部分夹持仪器未画出),探究氨气的还原性并检验产物。
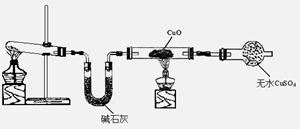
① 实验现象为:黑色CuO变为红色;白色无水CuSO4粉末变为蓝色;同时生成一种无色气体,该气体无污染。请写出氨气与CuO反应的化学方程式 。
② 碱石灰的作用是 。
③该装置存在明显缺陷,请指出存在的问题并提出改进意见
。
 (4)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+ Cu + Cu2+)。
(4)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+ Cu + Cu2+)。
请你设计一个简单的实验检验该红色物质中是否含有Cu2O。
;
(5)工业废气中的氮氧化物是主要的大气污染物之一。为了治理污染,工业上常用氨气与之发生反应:NOx+NH3→N2+H2O,使其转化为无毒的N2 。现有NO2和NO的混合气体3.0 L,跟3.4 L(同温同压下)NH3反应,恰好使其全部转化为氮气,则原混合气体中,NO2与NO的体积比是__________。
26.(13分)A、B、C、D、E为短周期元素,其原子序数依次增大。其中,A元素原子半径最小;B元素原子的电子总数与最外层电子数之比为3 :2;C元素最高价氧化物对应水化物与其氢化物反应生成一种盐甲。A、E同主族,A、B、C、E四种元素都能与D元素形成原子个数比不相同的常见化合物。请回答:
(1)写出B元素在周期表中的位置 , C单质的电子式是____________。
(2)A、D、E组成的化合物乙与氯化亚铁溶液反应的实验现象为 。
(3)常温下,甲的水溶液pH_______7(填>、<或=),其原因是(用离子方程式表示)_____________________。
(4)乙和B、D、E组成的化合物丙,它们的水溶液pH均为12时,两溶液中由水电离出的c(OH-),乙 :丙= 。
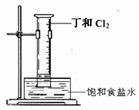 (5)A和B组成化合物丁,其相对分子质量为16。将右图装置放置在光亮的地方(日光没有直接照射),一会儿后,观察到量筒壁上有油状液滴生成等现象。油状液滴的成分可能是(写分子式) 。
(5)A和B组成化合物丁,其相对分子质量为16。将右图装置放置在光亮的地方(日光没有直接照射),一会儿后,观察到量筒壁上有油状液滴生成等现象。油状液滴的成分可能是(写分子式) 。
25.(15分)乙基香兰素是当今世界上最重要的合成香料之一,其结构简式如下图所示。
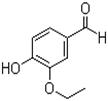 (1)以下推测正确的是 (填字母)。
(1)以下推测正确的是 (填字母)。
a.该物质能发生银镜反应
b.从分子结构上看,它应该属于芳香烃
c.1 mol该物质最多能与4 mol H2发生加成反应
d.该物质的一个分子内含有一个碳氧双键、三个碳碳双键
(2)乙基香兰素的同分异构体X,其分子中苯环上有2个取代基。X可以发生水解反应生成M和N两种有机物。M可与饱和溴水反应生成白色沉淀。N的质谱图显示相对分子质量为32,红外光谱图上发现有O-H键、C-H键和C-O键的振动吸收。写出2种符合上述要求的X的结构简式 ; 。
(3)乙基香兰素的另一种同分异构体Y,分子中苯环上只有1个取代基,它可以和碳酸氢钠反应生成CO2。

① Y分子中含氧官能团的名称是 。
② 由Y→B的反应属于_______________(填反应类型)。
③ A与新制Cu(OH)2反应的化学方程式是 。
④ 由B生成C的化学方程式是 。
⑤ Y发生缩聚反应所得产物的结构简式是 。
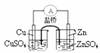
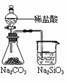
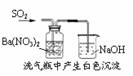
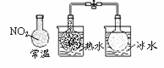
12.下列实验对应的结论正确的是
|
实验 |
 |
 |
 |
 |
|
结论 |
能组成 Zn、Cu原电池 |
能证明非金属性 Cl>C>Si |
白色沉淀 为BaSO3 |
说明反应 2NO2  N2O4
△H>0 N2O4
△H>0(无色) |
|
选项 |
A |
B |
C |
D |
11. 室温下,下列各项中的比值为2 : 1的是
A.0.2mol/L醋酸溶液与 0.1mol/L醋酸溶液中c(H+)之比
B.(NH4)2SO4溶液中c(NH4+)和c(SO42-)的物质的量浓度之比
C.pH= 2的盐酸和pH=12的Ba(OH)2溶液中溶质的物质的量浓度之比
D.0.2 mol/LCH3COONa溶液与 0.1mol/L Na2CO3溶液中c(CH3COO-)与c(CO32-)之比
10.下列离子方程式书写正确的是
A.用含氢氧化铝的胃舒平治疗胃酸过多:OH- + H+ = H2O
B.向AgCl的悬浊液中加入KI溶液:AgCl(s) + I-  AgI(s) + Cl-
AgI(s) + Cl-
C.苯酚钠溶液与二氧化碳反应: 2C6H5O-+ CO2 + H2O = 2C6H5OH + CO32-
D.稀硝酸与过量的铁屑反应: Fe + 4H+ + NO3- = Fe3+ + NO↑ + 2 H2O
9. 右表是元素周期表主族元素的一部分,已知短周期元素A最外层电子数是次外层的三倍。下列关于这四种元素说法正确的是
A.气态氢化物的稳定性:A<D
B.原子半径:B<C<A<D
C.A与B组成的两种化合物均只由离子键构成
D.B、C、D三种元素的最高价氧化物对应水化物间可两两反应
8.下列说法正确的是
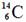 A. 0.1 mol 原子中含中子数为0.8×6.02×1023
A. 0.1 mol 原子中含中子数为0.8×6.02×1023
B. 0.5 mol/L CuCl2溶液中含有的Cu2+数为0.5×6.02×1023
C. 1 mol CO和 CO2混合物中,含有的碳原子数为2×6.02×1023
D. 2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1×6.02×1023
|
|
|
|
|
|
A |
|
B |
|
C |
|
|
D |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com