
2.已知集合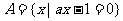 ,
,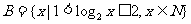 ,且
,且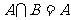 ,则
,则 的所有可能值组成的集合是
( )
的所有可能值组成的集合是
( )
A.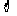 B.
B.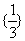 C.
C.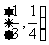 D.
D.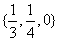
1.设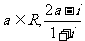 是一个纯虚数,则实数
是一个纯虚数,则实数 是
( )
是
( )
A.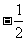 B.
B.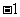 C.
C.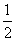 D.
D.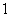
31.(18分)
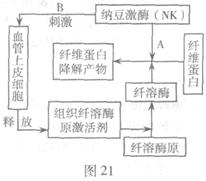 血栓主要由不溶性的纤维蛋白等物质组成。纳豆激
血栓主要由不溶性的纤维蛋白等物质组成。纳豆激
酶(NK)是一种在纳豆发酵过程中由纳豆菌产生的
蛋白酶,它不但能直接作于纤维蛋白(A过程),还
能间接激活体内纤溶酶原(B过程)。图21是有关
纳豆激酶溶栓机理简图,请据图回答问题:
(1)研究NK直接水解作用:给定纤维蛋白平板,
将 滴加其上,若出现相应的溶解圈,
则可说明 。
(2)NK的间接作用是通过 激
活体内纤溶酶原,增加纤溶酶的量和作用,溶解血栓。
(3)清根据下列出示的实验材料,比较NK与内源性纤溶酶溶栓效果,并在下面横线位置上,补全相应内容。
实验材料:NK溶液、内源性纤溶酶溶液、纤维蛋白块、缓冲液、量筒、试管和秒表。
实验步骤:
|
|
加入物质的成分 |
试管1 |
试管2 |
|
1 |
纤维蛋白块 |
1g |
1g |
|
2 |
缓冲液 |
1mL |
1mL |
|
3 |
纳豆激酶(NK)溶液 |
1mL |
/ |
|
4 |
|
/ |
1mL |
观察记录:观察纤维蛋白块分解情况,并记录分解的 。
请预测一种实验结果并分析:
(4)继续研究NK的化学组成:因为纳豆激酶存在于 ,可直接利用纳豆菌发酵液的上清液,进一步 ,鉴定其化学组成。
(5)由于NK在60℃时迅速失活,可通过 (现代生物技术)提高其热稳定性。
30.(16分)
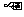 氨基丁酸(GA-BA)作为哺乳动物中枢神经系统中广泛分布的神经递质,在控制疼痛方面的作用不容忽视,其作用机理如图20所示。请回答有关问题:
氨基丁酸(GA-BA)作为哺乳动物中枢神经系统中广泛分布的神经递质,在控制疼痛方面的作用不容忽视,其作用机理如图20所示。请回答有关问题:
(1)GABA在突触前神经细胞内合成后,贮存在 内,以防止被胞浆内其它酶系所破坏。当兴奋抵达神经末梢时,GABA释放,并与位于图中 上的GABA受体结合。该受体是膜上某些离子的通道。当GABA与受体结合后,通道开启,使 离子内流,从而抑制突触后神经细胞动作电位的产生。上述过程体现出细胞膜具有 功能。如果用电生理微电泳方法将GABA离子施加到离体神经细胞旁,可引起相同的生理效应,从而进一步证明GABA是一种 性的神经递质。
(2)释放的GABA可被体内氨基丁酸转氨酶降解而失活。研究发现癫痫病人体内GABA的量不正常,若将氨基丁酸转氨酶的抑制剂作为药物施用于病人,可缓解病情。这是由于 ,从而可抑制癫痫病人异常兴奋的形成。
(3)图中麻醉剂分子嵌入的结构是 ,它的嵌入起到了与GABA一样的功能,从而可 (缩短/延长)该离子通道打开的时间,产生麻醉效果。
29.(16分)
科学家们用长穗偃麦草(二倍体)与普通小麦(六倍体)杂交培育小麦新品种--小偃麦。相关的实验如下,请回答有关问题:
(1)长穗偃麦草与普通小麦杂交,F1体细胞中的染色体组数为 。长穗偃麦草与普通小麦杂交所得的F1不育,其原因是 ,可用 处理F1幼苗,获得可育的小偃麦。
(2)小偃麦中有个品种为蓝粒小麦(40W+2E),40W表示来自普通小麦的染色体,2E表示携带有控制蓝色色素合成基因的1对长穗偃麦草染色体。若丢失了长穗偃麦草的一个染色体则成为蓝粒单体小麦(40W+1E),这属于 变异。为了获得白粒小偃麦(1对长穗偃麦草染色体缺失),可将蓝粒单体小麦自交,在减数分裂过程中,产生两种配子,其染色体组成分别为 ,这两种配子自由结合,产生的后代中自粒小偃麦的染色体组成是 。
(3)为了确定白粒小偃麦的染色体组成,需要做细胞学实验进行鉴定。取该小偃麦的作实验材料,制成临时装片进行观察,其中 期的细胞染色体最清晰。
28.(16分)
I.某校化学实验小组探究浓度对化学反应速率的影响,并测定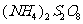 和KI反应的化学反应速率。进行如下实验探究:
和KI反应的化学反应速率。进行如下实验探究:
[实验原理]
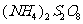 和KI反应的离子方程式为:
和KI反应的离子方程式为:
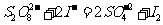 (1)
(1)
平均反应速率的计算式为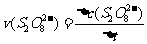 。
。
实验时,向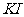 、
、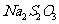 和淀粉指示剂混合溶液中加入
和淀粉指示剂混合溶液中加入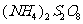 溶液,不断搅拌。
溶液,不断搅拌。
在反应(1)进行的同时,发生反应:
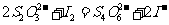 (2)
(2)
反应(1)生成的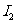 立即与
立即与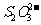 反应,生成无色的
反应,生成无色的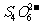 和
和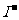 。
。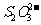 耗尽时,反应(1)继续生成的
耗尽时,反应(1)继续生成的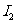 才与淀粉作用呈现蓝色。从加入
才与淀粉作用呈现蓝色。从加入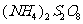 溶液到出现蓝色的时
溶液到出现蓝色的时
间为 。
。
[实验内容]
(1)实验小组设计的实验记录表和数据记录如下,请将表中字母表示的空格填上。
|
实验编号 |
①[ |
② |
③ |
④ |
⑤ |
|
|
试剂] 用量 (mL) |
0.20 mol·L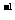 (NH4)2S2O8
溶液 (NH4)2S2O8
溶液 |
20.0 |
10.0 |
b |
20.0 |
20.0 |
0.20
mol·L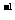 KI溶液 KI溶液 |
20.0 |
20.0 |
20.0 |
10.0 |
5.0 |
|
0.010
mol·L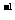 Na2S2O3溶液 Na2S2O3溶液 |
a |
8.0 |
8.0 |
8.0 |
8.0 |
|
|
0.2%淀粉溶液 |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
|
0.20
mol·L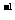 KNO3溶液 KNO3溶液 |
0 |
0 |
0 |
10.0 |
c |
|
0.20
mol·L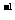 (NH4)2SO4 溶液 (NH4)2SO4 溶液 |
0 |
10.0 |
15.0 |
0 |
0 |
|
20℃时,反应时间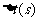 |
32 |
67 |
130 |
66 |
135 |
|
|
为了使溶液的离子强度和总体积保持不变,减少的(NH4)2S2O8溶液或KI溶液的用量,分别用(NH4)2SO4溶液或KNO3溶液补足;溶液混合后体积不变 |
(2)为了使反应充分进行,减少数据误差,实验过程中应该不断进行的操作是 。
(3)第①组实验的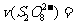 mol·(L·s)
mol·(L·s)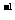 。
。
(4)根据上表数据分析,可以得到的结论有(写出一条即可) 。
 II.实验小组查资料得知,向含有NaCO3的Na2S溶液中通入SO2,可以制备上述实验所需的Na2S2O3。反应如下:
II.实验小组查资料得知,向含有NaCO3的Na2S溶液中通入SO2,可以制备上述实验所需的Na2S2O3。反应如下:

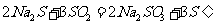
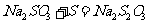
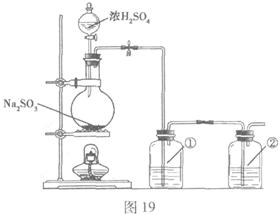
该小组根据上述原理设计如图19所示
装置制备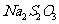 。
。
(1)实验应避免有害气体排放到空气中。
装置①、②中盛放的试剂依次是① ;
② 。
(2)实验过程中,随着气体的通入,装置①中有大量黄色固体析出,继续通入气体,可以观察到的现象是 。
(3)反应结束后,从制得的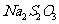 稀溶液中得到
稀溶液中得到 晶体的主要操作包括:
。
晶体的主要操作包括:
。
27.(14分)
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0-6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。
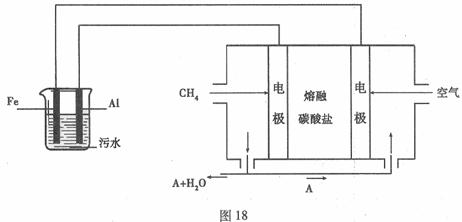
某科研小组用电浮选凝聚法处理污水,设计装置如图18所示:
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的 。
a.H2SO4 b.BaSO4 c.N2SO4 d.NaOH e.CH3CH2OH
(2)电解池阳极的电极反应分别是① ;
②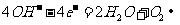 。
。
(3)电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是 。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。
已知负极的电极反应是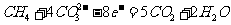 。
。
①正极的电极反应是 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是 。
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况) L。
26.(12分)
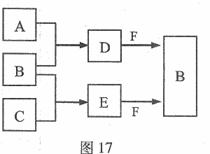
A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图17 (反应条件和部分产物略去)。试回答:
(1)E的电子式是 。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是 。
(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是 。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+) 。
(5)E的大量排放会引发很多环境问题。有科学家提出,用E和H2合成CH3OH和H2O,对E进行综合利用。25℃,101 kPa时,该反应的热化学方程式是 。(已知甲醇的燃烧热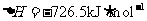 ,氢气的燃烧热
,氢气的燃烧热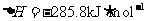 )
)
25.(16分)
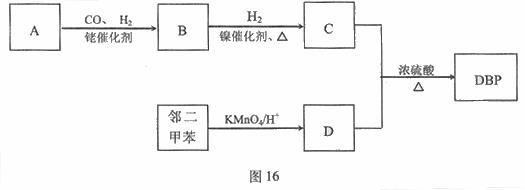
有机物DBP常用作纤维素树脂和聚氯乙烯的增塑剂,特别适用于硝酸纤维素涂料。具有优良的溶解性、分散性和粘着性。由有机物A和邻二甲苯为原料可以合成DBP。
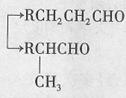
|
 已知:①RCH=CH2+CO+H2
已知:①RCH=CH2+CO+H2
②烃A是有机合成的重要原料。A的质谱图表明其相对分子质量为42,红外光谱表明分子中含有碳碳双键;B能发生银镜反应;有机物c的核磁共振氢谱显示其分子中含有5种氢原子,且其峰面积之比为3:2:2:2:1;DBP分子中苯环上的一溴取代物只有两种。
(1)A的结构简式是 。
(2)B含有的官能团名称是 。
(3)有机物C和D反应生成DBP的化学方程式是 。
(4)下列说法正确的是(选填序号字母) 。
a.A能发生聚合反应、加成反应和氧化反应
b.和C互为同分异构体,且含有相同官能团的有机物有2种
c.邻二甲苯能氧化生成D说明有机物分子中基团之间存在相互影响
d.1 mol DBP可与含2 mol NaOH的溶液完全反应
(5)工业上常用有机物E(C8H4O3)代替D生产DBP。反应分为两步进行:
① ②
②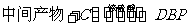
工业生产中在第②步中使用油水分离器将反应过程中生成的水不断从反应体系中分离除去,其目的是 。
(6)工业上生产有机物E的反应如下:
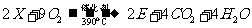
芳香烃X的一溴取代物只有两种,X的的结构简式是 。
24.(20分)
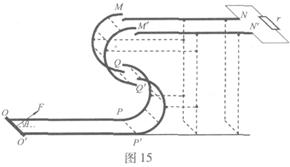
如图15所示,固定在上、下两层水平面上的平行金属导轨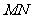 、
、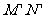 和
和 、
、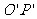 间距都是
间距都是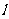 ,二者之间固定有两组竖直半圆形轨道
,二者之间固定有两组竖直半圆形轨道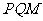 和
和 ,两轨道间距也均为
,两轨道间距也均为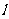 ,且
,且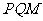 和
和 的竖直高度均为4R,两组半圆形轨道的半径均为R。轨道的
的竖直高度均为4R,两组半圆形轨道的半径均为R。轨道的 端、
端、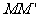 端的对接狭缝宽度可忽略不计,图中的虚线为绝缘材料制成的固定支架,能使导轨系统位置固定。将一质量为
端的对接狭缝宽度可忽略不计,图中的虚线为绝缘材料制成的固定支架,能使导轨系统位置固定。将一质量为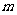 的金属杆沿垂直导轨方向放在下层导轨的最左端
的金属杆沿垂直导轨方向放在下层导轨的最左端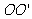 位置,金属杆在与水平成
位置,金属杆在与水平成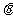 角斜向上的恒力作用下沿导轨运动,运动过程中金属杆始终与导轨垂直,且接触良好。当金属杆通过4R的距离运动到导轨末端
角斜向上的恒力作用下沿导轨运动,运动过程中金属杆始终与导轨垂直,且接触良好。当金属杆通过4R的距离运动到导轨末端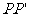 位置时其速度大小
位置时其速度大小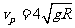 。金属杆和导轨的电阻、金属杆在半圆轨道和上层水平导轨上运动过程中所受的摩擦阻力,以及整个运动过程中所受空气阻力均可忽略不计。
。金属杆和导轨的电阻、金属杆在半圆轨道和上层水平导轨上运动过程中所受的摩擦阻力,以及整个运动过程中所受空气阻力均可忽略不计。
(1)已知金属杆与下层导轨间的动摩擦因数为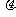 ,求金属杆所受恒力F的大小;
,求金属杆所受恒力F的大小;
(2)金属杆运动到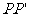 位置时撤去恒力F,金属杆将无碰撞地水平进入第一组半圆轨道
位置时撤去恒力F,金属杆将无碰撞地水平进入第一组半圆轨道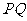 和
和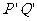 ,又在对接狭缝
,又在对接狭缝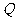 和
和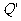 处无碰撞地水平进入第二组半圆形轨道
处无碰撞地水平进入第二组半圆形轨道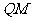 和
和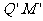 的内侧,求金属杆运动到半圆轨道的最高位置
的内侧,求金属杆运动到半圆轨道的最高位置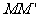 时,它对轨道作用力的大小;
时,它对轨道作用力的大小;
 (3)若上层水平导轨足够长,其右端连接的定值电阻阻值为
(3)若上层水平导轨足够长,其右端连接的定值电阻阻值为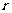 ,导轨处于磁感应强度为B、方向竖直向下的匀强磁场中。金属杆由第二组半圆轨道的最高位置
,导轨处于磁感应强度为B、方向竖直向下的匀强磁场中。金属杆由第二组半圆轨道的最高位置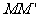 处,无碰撞地水平进入上层导轨后,能沿上层导轨滑行。求金属杆在上层导轨上滑行的最大距离。
处,无碰撞地水平进入上层导轨后,能沿上层导轨滑行。求金属杆在上层导轨上滑行的最大距离。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com