
27.⑴肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,agN2H4在氧气中完全燃烧生成氮气,放出热量QkJ(25℃时),N2H4完全燃烧反应的热化学方程式是 。
⑵肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。肼-空气燃料电池放电时:正极的电极反应式是 。
 负极的电极反应式是
。
负极的电极反应式是
。
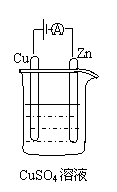
⑶右图是一个电化学过程示意图。
①锌片上发生的电极反应是 。
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128g,
则肼一空气燃料电池理论上消耗标准状况下的空气 L
(假设空气中氧气体积含量为20%)
⑷传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的离子方程式
。
26.元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子最外层电子数与次外层电子数之比为3∶4;N-、Z+、X+离子的半径逐渐减小;化合物XN常温下为气体。据此回答:
(1)M、N的最高价氧化物的水化物中酸性较强的是(写出化学式) 。
(2)Z与M可形成常见固体化合物C,用电子式表示C的形成过程 。
(3)已知通常状况下1g X2在Y2中完全燃烧放出a kJ的热量,请写出表示X2燃烧热的热
化学方程式 。
(4)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,
写出该反应的化学方程式 。
(5)化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比为1∶1∶1,A溶液中水的电离程度比在纯水中小。则化合物A中的化学键类型为 ;若B为常见家用消毒剂的主要成分,则B的化学式是 。
(6)均由X、Y、Z、M四种元素组成的两种盐发生反应的离子方程式是 ;其中一种是强酸所成的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式 。
13.常温时,将V1mLc1mol·L-1的醋酸溶液滴加到将V2mLc2mol·L-1的NaOH溶液中,若c1V1﹥c2V2,则反应后的溶液PH为:( )
A.等于7 B。大于7 C。小于7 D。无法确定
12.2008 年北京奥运会主体育场的外形好似“鸟巢” ( The Bird Nest )。有一类化学物质硼烷也好似鸟巢,故称为巢式硼烷。巢式硼烷除 B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化。下图是三种巢式硼烷,有关说法正确的是

A.这类巢式硼烷的通式是 C nH n + 4
B.2B5H9 + 12O2 5B2O3 十9H2O ,l molB5H9完全燃烧转移25mol电子
5B2O3 十9H2O ,l molB5H9完全燃烧转移25mol电子
C.8 个硼原子的巢式硼烷化学式应为 B8H10
D.硼烷与水反应是非氧化还原反应
11.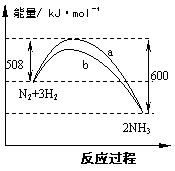 右图是778K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是( )
右图是778K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是( )
A.此反应2NH3  N2 +3H2为放热反应
N2 +3H2为放热反应
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的△H变大
D.在728K下,该反应的△H值将减小
10.甲烷、乙烯和乙炔组成的混合气体aL,与相同状况下的bL氢气恰好完全加成生成饱和烃。如果a<b,则原混合气体中甲烷和乙炔的体积比为
A.1∶1 B.大于1∶1 C.小于1∶1 D.任意比
9.要提纯下列物质(括号内物质为杂质),实验操作最合理的是 ( )
A.碳酸钠溶液(碳酸氢钠):加入过量氢氧化钠溶液,蒸发结晶
B.氢氧化铁胶体(氯化铁):加入足量硝酸银溶液,过滤
C.乙酸乙酯(乙酸):加入适量乙醇和浓硫酸,加热,蒸馏
D.氢氧化镁(氢氧化钙):放入水中搅拌成浆状后,加入足量氯化镁溶液,充分搅拌,过滤,沉淀用蒸馏水洗涤
8.下列反应的离子方程式正确的是( )
A.在H2O2中加入酸性KMnO4溶液:2MnO4-+5H2O2+6H+=2Mn2+ +5O2↑+8H2O
|
C.含有氢氧化铝的药品治疗胃溃疡:Al(OH)3+3HCl=AlCl3+3H2O
D.用氯化铁溶液腐蚀电路板:Fe3++Cu=Fe2++Cu2+
7.充分利用能源、提高原子利用率、减少向环境排放废弃物等都是绿色化学基本要求。
①在有机实验中,用溴的四氯化碳溶液代替溴的水溶液;②用稀硝酸代替浓硝酸溶解、回收含银镜试管里的银; ③用水浴加热代替直接用酒精灯加热;④接触法制硫酸中采用“热交换器”,利用余热预热冷原料气和烧水;⑤工业合成氨中分离产物得到氢气和氮气再循环使用; ⑥电解法冶炼钠和镁,选择电解氯化钠和氯化镁,不电解对应的金属氧化物。
上述主要不是从绿色化学角度考虑的是
A.①③ B.②④ C.⑤⑥ D.③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com