
27.(14分)已知A-N为中学化学中常见物质,有如下图所示的转化关系。其中,反应①和②都是重要的工业反应。D为红棕色粉末;H常温下为固体,部分反应物和生成物及反应条件未列出。
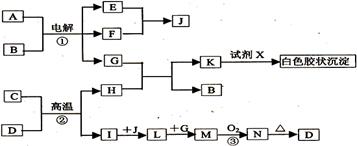
请根据以上信息回答下列问题:
(1)固体H化学式为_____ __ ,在工业上的主要用途____ ____。
(2)实验室实现K→白色胶状沉淀转化最理想的试剂X是____ _____(填化学式);
其反应的离子方程式是_____________________ ______ ___________________________
(3)M→N的实验现象是:
(4)反应①的离子反应方程式是:____________________________________________
26.(16分)有X、Y、Z、W四种元素,已知:①X、Y、W三种元素位于短周期,且X、W同主族;
②Z与Y可组成化合物ZY3,ZY3溶液遇KSCN溶液呈血红色;③X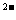 、Y
、Y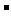 均与Y的气态氢化物分子具有相同的电子数。请回答下列问题:
均与Y的气态氢化物分子具有相同的电子数。请回答下列问题:
(1)Y的最高价氧化物对应水化物的化学式是 ;Y的最高价氧化物为无色液体,0.25 mol该氧化物与一定量水反应得到一种稀溶液,并放出Q kJ的热量,该反应的热化学方程式为 。
(2)将ZY3溶液滴入沸水可得红褐色液体,该反应的离子方程式为 。
(3)X单质在W单质中燃烧生成无色有刺激性气味的气体A。
①将气体A通入Y单质的水溶液中,反应的离子反应方程式为 。
②气体A与Y的一种含氧酸(该酸的某盐常用于实验室制取氧气)溶液反应,可生成一种强
酸和一种氧化物。若1 mol该含氧酸参与反应,转移6.02×1023个电子,则反应的化学方程式是 。
(4)比较X、Y气态氢化物的稳定性: > 。(用化学式表示)
13.56gFe粉投入500g稀HNO3中,两者恰好完全反应放出NO,溶液增重31g,则反应后溶液中两种金属阳离子比例为
A. 2︰1 B. 1︰1 C. 1︰2 D.无法确定
第Ⅱ卷
12.用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨
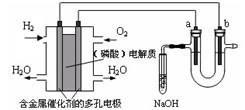 电极),下列说法正确的是
电极),下列说法正确的是
A.电池工作时,正极反应式为:O2 + 2H2O + 4e- == 4 OH-
B.电解时,a电极周围首先放电的是Cl-,电极反应为:2Cl- - 2e- == Cl2 ↑
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量消耗,当电池中消耗0.02g H2时,b极周围会产生0.02g H2
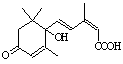
11.农艺师对鲜花施用了S-诱抗素剂(分子结构如右图),
可使鲜花按时盛开。我国在全球S-诱抗素研究领域处于领
先地位。下列说法正确的是
A.S-诱抗素的分子式为C15H22O4
B.S-诱抗素既能发生加聚反应,又能发生缩聚反应
C.1 molS-诱抗素最多能和含2molNaOH的水溶液发生反应
D.S-诱抗素既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色
10.下列有关溶液中微粒的物质的量浓度关系正确的是
A.pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中,c (NH4+)大小顺序为①=②>③
B.在NaHA溶液中(H2A为弱酸):c(Na+)>c(HA-)>c(H+)>c(OH-)
C.0.1mol/LNaHCO3溶液中:2c(CO32-)+c(OH-)+c(HCO3-)= c(Na+)+c(H+)
D.0.1 mol/L-NH4Cl溶液与0.05 mol/L NaOH溶液等体积混合:
 c
(Cl-)>c (Na+)>c(NH4+)>c (OH-)>c (H+)
c
(Cl-)>c (Na+)>c(NH4+)>c (OH-)>c (H+)
9.在容积恒定的密闭容器中充人2molA和1molB,发生如下反应2A(g)+B(g)  xC(g),达到平衡后,C的体积分数为a%;若维持容器的容积和温度不变,按起始物质的量A为0.6mol、B为0.3mol、C为2.8mol充人容器中,达到平衡后,C的体积分数仍为a%,则x的值是
xC(g),达到平衡后,C的体积分数为a%;若维持容器的容积和温度不变,按起始物质的量A为0.6mol、B为0.3mol、C为2.8mol充人容器中,达到平衡后,C的体积分数仍为a%,则x的值是
A.只能为3 B.只能为4
C.可能为3,也可能为4 D.无法确定
8.下列反应的离子方程式书写正确的是
A.向澄清石灰水中滴加稀硫酸:2H++SO42-+Ca2++2OH-= 2H2O+CaSO4↓
B.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑
C.小苏打与氢氧化钠溶液混合:HCO3-+OH-= CO2↑+H2O
D.Ca(HCO3)2溶液中加入过量KOH溶液:Ca2+ + HCO3- +OH-= CaCO3↓+ H2O
7.若NA表示阿伏加德罗常数,则下列说法正确的是
A.常温常压下,100mL 0.1 mol/L的HCOOH 溶液中含 H+数目为 0.0lNA
B.常温常压下,28gN2和CO的混合气体含有的原子数为2NA
C.24g石墨中含有的C-C键个数为2NA
D.标准状况下,22.4L CHCl3所含有的分子数为 NA
6.下列说法正确的是
A.乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
B.钢铁在海水中比在河水中更容易腐蚀,主要原因是海水含氧量高于河水
C.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源
D.凡含有食品添加剂的食物对人体健康均有害,不宜食用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com