
3、已知实数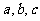 满足
满足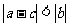 ,则下列不等式一定成立的是( )
,则下列不等式一定成立的是( )
A 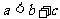 B
B 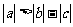 C
C 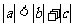 D
D 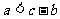
2、参数方程 为参数)表示的曲线是( )
为参数)表示的曲线是( )
A 抛物线 B 双曲线 C 双曲线的一部分 D 抛物线的一部分
1、圆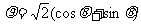 的圆心坐标是( )
的圆心坐标是( )
A (2,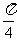 ) B (1,
) B (1,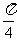 ) C (
) C (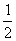 ,
,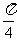 ) D (
) D (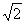 ,
,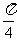 )
)
23.(10分)
A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为 ,B为 ,C为 。D的最高价氧化物的水化物是 。
(2)写出A、B的化合物与E反应的化学方程式:
(3)A、B两元素形成化合物属 (“离子”或“共价”)化合物。
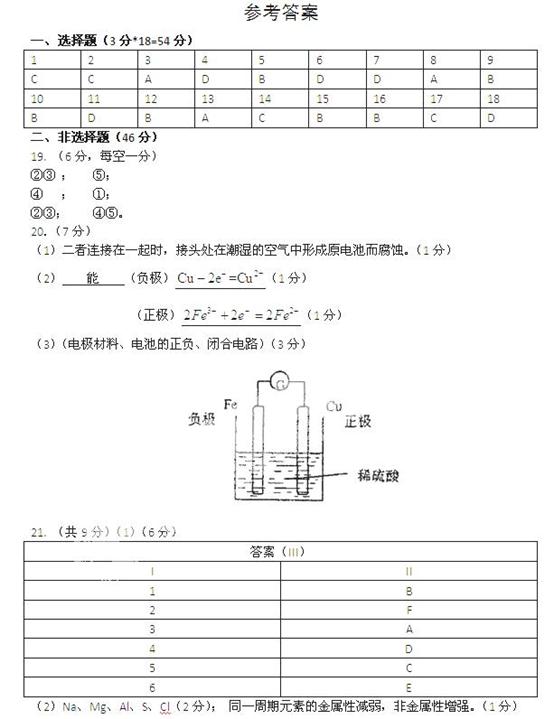
(4)写出D的最高价氧化物的水化物和A反应的化学方程式:

22.(14分)
 下表是元素周期表的一部分,请回答有关问题:
下表是元素周期表的一部分,请回答有关问题:
|
主族 周 期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
① |
② |
|
③ |
|
|
3 |
|
|
⑤ |
|
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
④ |
|
|
|
|
⑩ |
|
(1)表中化学性质最不活泼的元素,其原子结构示意图为 。
(2)表中能形成两性氢氧化物的元素是 (用元素符号表示),写出该元素的
质与⑨最高价氧化物的水化物反应的化学方程式
(3)④元素与⑦元素形成化合物的电子式
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是
(填化学式)。
(5)③元素与⑩元素两者核电荷数之差是 。
(6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。
|
实验步骤 |
实验现象与结论 |
|
|
|
21.(9分)
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:(1)请从下表中实验现象(Ⅱ)(填A、B、C……)中选出与方案(I)(填1、2、3……)对应的实验现象,填入答案(Ⅲ)中。
实验方案( I) I) |
实验现象(Ⅱ) |
答案(III) |
|
|
实验方案I |
实验现象II |
||
|
1.用砂纸擦后的镁带与沸 水反应,再向反应液中滴 加酚酞 |
A浮与水面,剧烈反应,放出气体, 熔成-个小球,在水面上无定向移 动,随之消失,溶液变红色。 |
1 |
|
|
2.向新制的H2S饱和溶 液中滴加新制的氯水 |
B.产生大量气体,可在空气中燃 烧,溶液变成浅红色 |
2 |
|
|
3.钠与滴有酚酞的冷水反应 |
C.反应不十分剧烈,产生的气体 可以在空气中燃烧 |
3 |
|
|
4.镁带与2mol/L的盐酸 反应 |
D.剧烈反应,产生的气体可以在 空气中燃烧 |
4 |
|
|
5铝条与2mol/L的盐酸 反应 |
E.生成白色絮状沉淀,继而沉淀 消失 |
5 |
|
6.向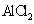 溶液中滴加 溶液中滴加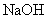 溶液至过量 溶液至过量 |
F.生成淡黄色沉淀 |
6 |
|
(2)通过以上实验分析了同周期元素的符号 ,从实验结果可以得出的结论是 。
下列五种物质中,①Ar ②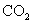 ③
③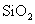 ⑤
⑤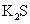 ,只存在共价键的是
,只存在离子键的是
,既存在离子键又存在共价键的是
,不存在化学键的是
。属于共价化合物的是
属于离子化合物的是
。
,只存在共价键的是
,只存在离子键的是
,既存在离子键又存在共价键的是
,不存在化学键的是
。属于共价化合物的是
属于离子化合物的是
。
20. 已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液: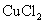 溶液、
溶液、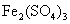 溶液、盐酸。按要求回答下列问题:
溶液、盐酸。按要求回答下列问题:
(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用。请说明原因
(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池
,若能,请写出电极反应式,负极 ,正极 。(若不能,后两空不填)
(3)设计一种以铁和硫酸反应为原理的原电池,要求画出装置图:(需标明电极材料及电池
的正负。)
18.下列各组物质中化学键的类型相同的是
A.HCI 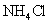 B.
B.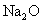
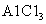
C. NaOFI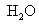 D.
D.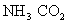


第Ⅱ卷(非选择题共46分)
17.某课外活动小组使用下列用品设计原电池。用品:铜片、铁片、导线、金属夹、发光
二极管、果汁(橙汁、苹果汁)500mL,、烧杯。下列说法正确的是
A.该装置能将电能转化为化学能 B.实验过程中铜片逐渐溶解
C电子由铁片通过导线流向铜片 D.铁片上会析出红色的铜
16.锗(Ge)是第四周期第ⅣA元素,处于周期表中金属区与非金属区的交界线上,
列叙述正确的是
A.锗是一种金属性很强的元素 B.锗的单质具有半导体的性能
C.锗化氢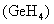 稳定性很强 D.锗酸(
稳定性很强 D.锗酸(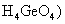 是难溶于水的强酸
是难溶于水的强酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com