
22、短周期元素X、Y、Z的离子具有相同的核外电子排布,原子半径X大于Z,离子半径Y大于Z,Y与Z可形成常见的离子化合物,则下列说法中不正确的是( )
A.原子序数一定是Z>X>Y B.X、Z两种元素的单质的沸点一定是Z>X
C.Z的最高价氧化物一定能溶于X、Y的最高价氧化物的水化物
D.工业上获得X、Z单质的方法主要是电解
21、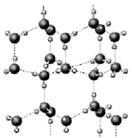 右图为冰晶体的结构模型,大球代表O原子,小球代表H原子。
右图为冰晶体的结构模型,大球代表O原子,小球代表H原子。
下列有关说法正确的是( )
A. 冰晶体熔化时,水分子之间的空隙增大
B.冰晶体具有空间网状结构,是原子晶体
C.水分子间通过H-O键形成冰晶体
D.冰晶体中每个水分子与另外四个水分子形成四面体
20、关于下列图示的说法中正确的是( )
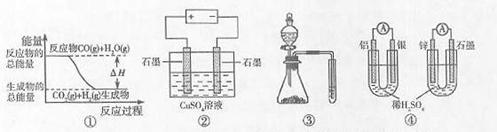
 A.图①表示可逆反应:“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0
A.图①表示可逆反应:“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0
B.图②为电解硫酸铜溶液的装置,一定时间内,两电极产生单质的物质的量之比一定为1:1
C.图③实验装置可完成比较乙酸、碳酸、苯酚酸性强弱的实验
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的最也相同
19、海底黑烟囱可在海底堆积硫化物的颗粒,形成多种金属矿产。若从海底黑烟囱附近的矿产物中分离出富铜矿CuFeS2,可用于冶炼铜,熔炼过程主要反应为:
2CuFeS2 = Cu2S+2FeS+S…………………………… ①
2Cu2S+3O2=2Cu2O+2SO2………………………………… ②
Cu2O+FeS = Cu2S+FeO……………………………… ③
2FeS+3O2+SiO2 = 2FeO·SiO2+2SO2………………… ④
2FeO+SiO2 = 2FeO·SiO2……………………………… ⑤
Cu2S+2Cu2O = 6Cu +SO2 ……………………………… ⑥
下列有关说法不正确的是( )
A.反应④转移12e- B.该厂可同时建硫酸厂和炼铁厂
C.该厂的原料除富铜矿外,还需空气和硅石 D.上述反应均属于氧化还原反应
18、 X、Y、Z、W有如右图所示的转化关系,且△H=△H1+△H2,则X、Y可能是( )
X、Y、Z、W有如右图所示的转化关系,且△H=△H1+△H2,则X、Y可能是( )
①C、CO ②S、SO2 ③AlCl3、Al(OH)3
④Na2CO3、NaHCO3 ⑤Fe、FeCl2
A.①②③④⑤ B.②④⑤ C.①③④ D.①②③
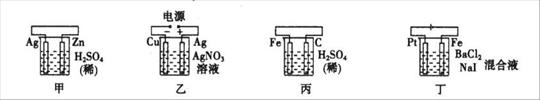
17、有关甲、乙、丙、丁四个图示的叙述正确的是( )
A.甲中负极反应式为:2H++2e-=H2↑ B.乙中阳极反应式为:Ag++e-== Ag
C. 丙中H+向碳棒方向移动 D.丁中电解开始时阴极产生黄绿色气体
16、下列说法或表示方法正确的是( )
A.反应物的总能量低于生成物的总能量时,该反应一定不能发生
B.化学键和分子间作用力都对物质的性质有一定的影响
 C.已知:2SO2 (g) + O2 (g) 2SO3
(g) ;△H = -98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
C.已知:2SO2 (g) + O2 (g) 2SO3
(g) ;△H = -98.3 kJ/mol。将1 mol SO2和0.5 mol O2充入一密闭容器中反应,放出49.15 kJ 的热量
D.由石墨比金刚石稳定可知:C(金刚石,s)= C(石墨,s) ;△H<0
15、根据实验目的判断下列实验操作或装置正确的是 ( )
|
目的 |
实验室制O2 |
配制稀硫酸溶液 |
在铁制品上镀铜 |
净化、精制淀粉胶体 |
|
装置 或操作 |
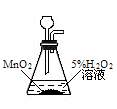 |
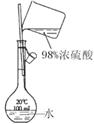 |
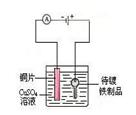 |
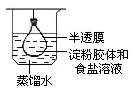 |
|
选项 |
A |
B |
C |
D |
14、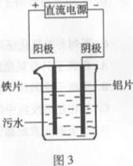 电浮选凝聚法是工业上采用的一种污水处理方法.图3
电浮选凝聚法是工业上采用的一种污水处理方法.图3
是电解污水的实验装置示意图,实验用污水中主要含有可被吸附
的悬浮物(不导电)。下列有关推断明显不合理的是( )
A.阴极的电极反应式为: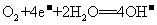
B.通电过程中烧杯内产生可以吸附悬浮物的Fe(OH)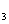
C.通电过程中会产生气泡,把悬浮物带到水面形成浮渣弃去
D.如果实验用污水导电性不良,可加入少量Na2SO4 固体以增强导电性
13、铅蓄电池用途极广,电解液为30% H2SO4 溶液,电池的总反应式可表示为:
Pb(s)+PbO2(s)+2H2SO4(aq)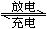 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
下列有关叙述正确的是( )
A.放电时电解液的浓度不断增大
B.放电时电子从Pb通过导线转移到PbO2
C.充电时Pb极与外电源的负极相连
D.充电时PbO2电极发生还原反应,Pb电极上发生氧化反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com