
7.下列离子方程式正确且表示复分解反应的是
A.亚硫酸钠溶液与双氧水混合:SO32-+2H2O2=SO42-+2H2O+O2↑
B.硅酸钠溶液中通入过量的CO2:SiO32-+CO2+H2O=H2SiO3↓+CO32-
C.氯气通入水中:Cl2+ H2O=2H++Cl-+ClO-
D.将0.1 mol·L-1 Na2CO3数滴缓缓滴入0.1 mol·L-1 25 mL 盐酸溶液中,并不断搅拌:
2H+ + CO32-=CO2↑+H2O
6.分类是学习和研究化学的一种常用的科学方法。下列分类肯定合理的是
A.根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等
B.根据电解质在水中或熔融状态下能否完全电离将电解质分为强电解质和弱电解质
C.根据元素原子最外层电子数的多少将元素分为金属和非金属
D.根据氧化物与水反应是否生成酸或碱将氧化物分为酸性氧化物和碱性氧化物
5.下列叙述中正确的是
A.胶体区别于其他分散系的本质特征是丁达尔现象
B.原子晶体的熔点一定比金属晶体高
C.离子反应中,阴离子与阳离子结合时不一定生成离子化合物
D.NaCl既可表示氯化钠的组成,又能表示其分子式
4.设NA表示阿伏加德罗常数,下列说法正确的是
A.1 mol NaHSO4晶体中离子总数为3 NA
B.2.24 L 14CH4分子中所含中子数为0.8 NA
C.0.1 L 3 mol·L-1的NH4NO3溶液中含有的NH4+数目为0.3 NA
D.标况下,将FeSO4溶液置于空气中,被氧化的Fe2+为0.2 NA,吸收O2为1.12 L
3.下列有关物质性质的比较中,正确的是
A.熔点:CO2<H2O<SiO2<KCl B.还原性:S2->I->Br->Cl-
C.酸性:H3PO4>H2SO4>HClO4>H2SiO3 D.稳定性:H2O<NH3<PH3<SiH4
2.表示下列变化的化学用语正确的是
A.乙烯的分子式:CH2=CH2
B.NaHCO3的电离:HCO3-+ H2O 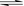 H3O+ + CO32-
H3O+ + CO32-
C. NaOH的结构式:Na-O-H

D.NH4Cl的电子式:
1.据报道,德国Integral公司研究出一种新的冷却技术,并荣获德国环境大奖。这种技术是用水和冰组成的物质代替传统的制冷制--氟里昂或氨。关于这一新的制冷剂,以下叙述不正确的是
A.该制冷剂对环境不产生任何污染
B.该制冷剂的作用原理与氟里昂或氨基本相同
C.该制冷剂为混合物
D.该制冷剂具有与水相同的化学性质
12.(2010·银川模拟)1689年英国的《权利法案》、美国1787年宪法、法国1875年宪法、1871年德意志帝国宪法的颁布,都标志着这些国家资本主义代议制政体的建立, 这说明
( )
A.从“人治”到“法治”是近代社会的突出特征
B.共和政体的确立
C.资本主义在全世界范围内最终确立
D.欧洲资本主义制度诞生
答案 A
解析 英国和德意志帝国的政体不是共和政体,排除B;这几个国家确立了资本主义制度,不能说明资本主义在全世界范围内最终确立,排除C;首先,美国不属于欧洲,其次,英国、法国、德意志帝国这几个国家资本主义代议制政体的建立也不能说明欧洲资本主义制度的诞生,排除D项。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com