
17.短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10。A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数。则下列叙述正确的是
A.四种元素的原子半径:A<B<D<C
B.D元素处于元素周期表中第3周期第Ⅵ族
C.B、D的最高价氧化物中,B、D与氧原子之间均为双键
D.一定条件下,D单质能置换出B单质,C单质能置换出A单质
16. 反应N2O4(g)
反应N2O4(g)
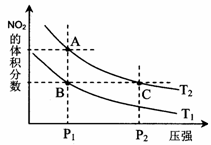
 2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
A.A、C两点的反应速率:A>C
B.B、C两点的反应速率:B = C
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的颜色:A深,C浅
15.用A、B、C、D四种酸进行下列实验:
①25℃时, PH=a的酸A,与PH=b的NaOH溶液等体积混合,混合后测得溶液的PH=7,且a+b>14;
②B与NaCl不反应,能与Na2CO3反应生成CO2;
③向浓度为10-2 mol·L-1的C溶液中滴加甲基橙试液,溶液呈黄色;
④酸D的钠盐不止一种,向两种D的钠盐水溶液中分别滴加紫色石蕊试液时,一个显红色,一个显蓝色。从上述实验数据和现象中,可以用来确定是弱酸的实验是
A.②③ B.①③④ C.②③④ D.全部
14.F2和Xe在一定条件下可生成氧化性极强且极易水解的XeF2、XeF4和XeF6三种化合物。如XeF4与水可发生如下反应:6XeF4+12H2O==2XeO3+4Xe↑+24HF+3O2↑。下列判断中正确的是
A.XeF2分子中各原子均达到8电子稳定结构
B.XeF6分子中Xe的化合价为+6价
C.上述反应中氧化剂和还原剂的物质的量之比为2∶3
D.XeF4按上述方式水解,每生成4 mol Xe,转移12 mol电子
13.下图是KNO3 和NaCl 的溶解度曲线。下列说法中正确的是
A.NaCl 的溶解度不受温度的影响
B.t1℃时,100 g KNO3 饱和溶液中含有20 g KNO3
C.t2℃时,KNO3的饱和溶液和NaCl 的饱和溶液中溶质的质量分数不一定相等
D.温度高于t2℃时,KNO3的溶解度大于NaCl 的溶解度
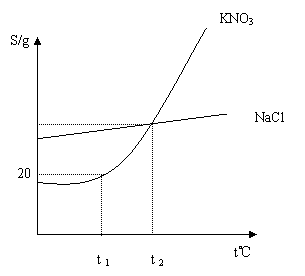
12.下列关于反应能量的说法正确的是
A.Zn(s) +CuSO4 (aq) = ZnSO4 (aq) +Cu(s) ;△H =-216 kJ·mol-1。则反应物总能量 >生成物总能量
B.相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子的能量为E2。则2E1 = E2
C.l0l kPa时,2H2 (g)+ O2 (g) = 2H2O(1) ;△H =-571.6 kJ·mol-1 ,则H2的燃烧热为571.6 kJ·mol-1
D.H+(aq) +OH-(aq) =H2O(l) ;△H=-57.3 kJ·mol-1 ,含 1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量
11.元素周期表的第7周期称为不完全周期,若将来发现的元素把第7周期全排满,则下列推论错误的可能性最大的是
A.该周期有32种元素
B.该周期的元素,原子序数最大为118
C.该周期的ⅦA族元素是金属元素
D.该周期的ⅢA族元素的氢氧化物具有两性
10.在容积不变的密闭容器中,在一定条件下发生反应:2A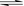 B(g)+C(g),且达到平衡。当升高温度时气体的密度增大,则
B(g)+C(g),且达到平衡。当升高温度时气体的密度增大,则
A.若正反应是吸热反应,则A为非气态 B.若正反应是吸热反应,则A为气态
C.若正反应是放热反应,则A为气态 D.若正反应是放热反应,则A为非气态
9.“XYn”表示不同卤素之间靠共用电子对形成的卤素互化物(非金属性:X<Y), 其化学性质和卤素单质相似。下列说法中正确的是
A.ICl与水生成 HCl 和 HIO的反应是氧化还原反应
B.某温度,液态 IF5电离:2IF5 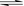 IF4+
+IF6-, 则 c (IF4+)×c (IF6-) 是一个常数
IF4+
+IF6-, 则 c (IF4+)×c (IF6-) 是一个常数
C.BrCl的沸点比Br2的沸点高
D.XYn 与卤素单质一样都是非极性分子
8.下列各组离子在溶液中按括号中的物质的量之比混合,得到无色、酸性、澄清溶液的是
A.Fe3+、Na+、Cl-、S2-(1︰2︰3︰1)
B.NH4+、Ba2+、OH-、Cl-(1︰1︰1︰2)
C.K+、H+、I-、HSO3-(1︰2︰2︰1)
D.Na+、Al3+、Cl-、OH-(4︰1︰3︰4)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com