
18.在体积均为1 L,pH均等于2的盐酸和醋酸中,分别投入0.12 g镁粉充分反应后,下图中比较符合反应事实的曲线是


17、下面有关电化学的图示,完全正确的是( )

16.用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
A.直线形;三角锥形 B.V形;三角锥形
C.直线形;平面三角形 D.V形;平面三角形
15.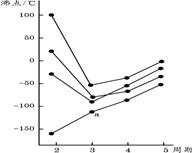 右图中每条折线表示周期表ⅣA-ⅦA中的某一族
右图中每条折线表示周期表ⅣA-ⅦA中的某一族
元素氢化物的沸点变化,每个小黑点代表一种氢化物,
其中a点代表的是 ( )
A.H2S B.HCl C.PH3 D.SiH4
14. “类推”是一种重要的学习方法,但有时会产生错误的结论,下列类推结论中正确的( ) A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 B.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 C.二甲苯的沸点顺序是:邻二甲苯>间二甲苯 >对二甲苯;则羟基苯甲醛的沸点顺序也是:邻羟基苯甲醛 >对羟基苯甲醛
D.根据“相似相溶”,乙醇能与水以任意比互溶,则戊醇也能与水以任意比互溶
13.已知含氧酸可用通式XOm(OH)n来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大的是强酸,m小的是弱酸。下列各含氧酸中酸性最强的是( )
A.H2SeO3 B.HMnO4 C.H3BO3 D.H3PO4
12.Co(Ⅲ)的八面体配合物CoClm· nNH3 ,若1mol配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是( )
A.m=1 n=5 B.m=3 n=4 C.m=5 n=1 D.m=4 n=5
11.下列化合物中含有2个手性碳原子的是 ( )
( )

10.某装置如图所示,下列有关叙述正确的是 ( )
A.该装置为电解池
B.用铜导线代替盐桥,该装置依然能正常工作
C.该装置中总反应为;Cu+2Ag+=Cu2++2Ag
D.Ag一极的反应为:2H++2e一=H2↑
9.氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ( )
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
 C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
D.氨气分子是极性分子而甲烷是非极性分子。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com