
6.已知棱锥的顶点P在底面上的射影为O,PO=a,现在用平行于底面的平面去截这个棱锥,截面交PO于点M,并使得截得的两部分侧面积相等。设OM=b,则a与b的关系是( )
A.  B.
B. 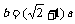 C.
C.  D.
D. 
5.顶点在同一球面上的正四棱柱ABCD-A1B1C1D1中,AB = 1,AA1 =  ,则A、C两点间的球面距离为( )
,则A、C两点间的球面距离为( )
A.  B.
B. 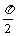 C.
C. 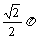 D.
D. 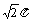
4.甲组有5名男同学,3名女同学;乙组有6名男同学、2名女同学。若从甲、乙两组中各选出2名同学,则选出的4人中恰有1名女同学的不同选法共有( )
A.150种 B.180种 C.300种 D.345种
3. (x-2)6的展开式中含x3项的二项式系数是( )
A.160 B.20 C.-160 D.-20
2.若A与B是互斥事件,其发生的概率分别为 ,则A、B同时发生的概率为( )
,则A、B同时发生的概率为( )
A. B.
B.  C.
C.
 D. 0
D. 0
1.如果一个球的半径为1,那么这个球的表面积是( )
A.
2 B. 4
B. 4 C.
C.  D.
D. 
25.
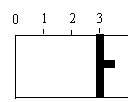
一定温度下,向如图所示带有可移动活塞的密闭容器中充入2 L SO2 和1 L
O2 的混合气体,发生如下反应2 SO2 (g) + O2
(g)  2
SO3 (g) 。
2
SO3 (g) 。
(1) 若活塞可自由移动,平衡后,活塞停止在“2.1”处,则该反应中SO2 的转化率为 。
 (2)
若开始时,充入容器的起始物质分别是
(2)
若开始时,充入容器的起始物质分别是
①2 L SO2 和1 L O2 ;
②2 L SO3 (g) 和 1 L N2 ;
③1 L SO2 、1 L O2 和 1 L SO3 (g),
使活塞固定在“3”处,达到平衡后,容器中SO3 (g)占反应混合物的体积分数的大小关系是:
(用序号和“<”、“=”、“>”表示)。
(3) 向(1)平衡后的容器中充入0.2 mol 的SO3,活塞移动后再次达到平衡时,测得此过程中从外界共吸收了1.96 kJ 的热量。
写出SO2 发生氧化反应的热化学方程式: 。
浙江嘉兴一中09-10学年高二下学期4月月考
24.现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_______p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(保持体系体积不变),则A的转化率_________,B的转化率_________。
(4)若升高温度,则平衡时B、C的浓度之比 将______ ___。
将______ ___。
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
23. 如下图所示的装置,C、D、E、F都是惰性电极。
将电源接通后,向乙中滴入酚酞试液.在F极附近显红色。试回答以下问题:
(1)电极A的名称是 。
(2)甲装置中电解反应的总化学方程式是 ______________________________ 。

(3)若用惰性电极电解饱和NaCl溶液一段时间,当阳极产生56L(标准状况下)气体,电解后溶液体积为500L时,产物的物质的量浓度为__________。
(4)欲用丙装置给铜镀银,G应该是 (填“银”或“铜”), 电镀液的主要成分是(填化学式) 。
22. ⑴北京奥运会祥云火炬将中国传
⑴北京奥运会祥云火炬将中国传
统文化、奥运精神以及现代高科技融为一体。
火炬内熊熊大火来源于丙烷的燃烧,丙烷是
一种优良的燃料。试回答下列问题:
① 右图是一定量丙烷完全燃烧生成
CO2和1mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“-”。
②写出表示丙烷燃烧热的热化学方程式:
___________________________________。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为_______。
⑵盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
已知: H2O(g)=H2O (l) △H1=-Q1 kJ/mol
C2H5OH(g)=C2H5OH (l) △H2=-Q2 kJ/mol
C2H5OH (g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3 kJ/mol
若使23g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为____________kJ。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com