
5.1917年,中国北洋政府对德宣战,并派出大批劳工到欧洲战场服役。80多年后,时任法国总统的希拉克曾这样评价说,“任何人都不会忘记这些远道而来的、在一场残酷的战争中与法国共命运的勇士,他们以自己的灵魂和肉体捍卫了法国的领土、理念和自由”。结合上述材料,对中国参战的诸多评价中,你最赞成的是
A.对德宣战导致不少中国劳工丧生
B.对德宣战是段祺瑞政府的错误决策
C.对德宣战客观上提高了中国的国际地位
D.对德宣战不利于一战的尽快结束
4.瑞士著名的国际法学者瓦特尔在1758年发表的《国际法》中说:“均势的核心意义是妥协安排国际事务,没有一个国家能居于至高无上的主宰、支配他国的地位。”1907年,英国外交部在克劳备忘录中谈到:“英国的政策是维持均势,把自己的力量加在这一边或那一边,但是总是加在一边以抵制某一时期内最强大的国家或集团的政治霸权。这几乎成为一个历史上的真理。”英国“均势”政策的表现不包括
A.参加反法同盟, B.巴黎和会上反对法国过分削弱德国
C.英法俄组成协约国 D.与法国联合,与美国争夺国联领导权
3.一战中,德军参谋长毛奇对威廉二世说:“陛下,我们输掉了战争!”毛奇的这句话应该说于
A.马恩河战役后 B.凡尔登战役后
C.索姆河战役后 D.日德兰海战后
2.1896年德皇威廉二世说:“我们十年前开始实行殖民政策而未有舰队……我们现在有了大量的殖民属地……因为这些殖民属地与英国继续不断地发生或大或小的纠纷……我们的贸易正和英国作生死的斗争……但是在各大洋上航行的挂着我们旗帜的大批商船,在130只英国巡洋舰的面前而我们只有4只来对抗的情形下,是十分不保险的。”对上述的认识,不正确的是
A.英德矛盾逐渐成为帝国主义间的主要矛盾
B.德国打算与英国进行海军军备竞赛
C.赢得争夺的焦点是殖民地和贸易问题
D.德国力图与英国成为海上贸易伙伴
1.“20世纪初,帝国主义的殖民体系形成但又过时。”导致这种“过时”的最主要原因是:
A.资本主义经济的发展 B.民族解放运动的兴起
C.列强力量对比的变化 D.局部战争的不断变化
29.(12分)A、B、C、D、E均为可溶于水的固体,组成它们的离子有
|
阳离子 |
Na+ Mg2+ Al3+
Ba2+ |
|
阴离子 |
OH
Cl CO32-
HSO-4 |
分别取它们的水溶液进行实验。结果如下:
①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生白色沉淀,沉淀可溶于E溶液;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。据此推断它们是A ;B ;C ;D
河北省正定中学2010高一第二学期第一次考试
28.(21分)有A、B、C、D、E五种短周期元素,A元素的一种同位素原子核内不含中子,其单质为气体;B原子最外层电子数是次外层电子数的3倍,C 2+与B元素的离子具有相同的电子层结构;D与E原子具有相同的电子层数,且次外层电子数均为8;在同周期主族元素中原子半径E最大,D最小。回答下列问题:
(1)C 2+离子与D原子的结构示意图分别为: 、 。
(2)B和E形成的两种化合物的电子式是: 、
其中之一可与A 和B形成的化合物反应得到游离态B,写出该反应的化学方程式:
。
(3)由这五种元素中的几种形成的化合物中碱性最强的是 (化学式),
含氧酸酸性最强的是 (化学式)。
27.(12分)(1)已知20.0gNaOH稀溶液跟足量稀盐酸反应,放出28.68kJ热量,那么此反应数据表明:如果NaOH稀溶液跟稀盐酸中和生成18g水时,该反应放出热量_________________kJ,由此测得的中和热为___________kJ/mol
(2)已知断开1 molH-H键、1mol Br-Br键、1mol H-Br键分别需要吸收的能量为436kJ、193kJ、366kJ.。 计算H2和Br2反应生成1mol HBr需_______(填“吸收”或“放出”)能量_______kJ。
26.(15分)(1)分别用电子式表示HClO、MgCl2的形成过程
(2)已知下列原电池的总反应式:Cu+2FeCl3==CuCl2+2FeCl2,请写出电极反应式:
 正极反应式为:
正极反应式为:
负极反应式为:
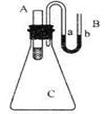
(3) 如图所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面高于b端液面的是____________。(填序号)
25. 在25 ℃,101 kPa下,1 mol的白磷(化学式为P4)完全燃烧放出的热量比4 mol的红磷(化学式为P)完全燃烧放出的热量多。反应方程式分别为:
P4 (s) + 5O2 (g) = P4O10 (s) 4P (s)+ 5O2 (g) = P4O10 (s)
由此判断,下列说法正确的是( )
A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高
B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低
C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高
D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低
第Ⅱ卷(非选择题,共60分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com