
31.(15分)[化学-选修物质结构与性质]
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
|
Z |
Z和Y同周期,Z的电负性大于Y |
|
W |
W的一种核素的质量数为63,中子数为34 |
(1)Y元素位于周期表中 区,该元素原子核外共有 种不同运动状态的电子。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键,该分子中中心原子的杂化类型为 。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子外围电子排布式是 。
(4)请写出元素W的单质与元素Y的最高价氧化物对应水化物的浓溶液在一定条件下发生反应的化学方程 。
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:XO(g)+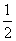 O2(g)=XO2(g)
O2(g)=XO2(g)  H =-283.0
kJ·mol-2
H =-283.0
kJ·mol-2
Y(s)+ O2(g)=YO2(g)  H =-296.0 kJ·mol-1
H =-296.0 kJ·mol-1
此反应的热化学方程式是 。
30.(10分)[化学-选修有机化学基础]
下表是A、B、C、D、E五种有机物的有关信息;
|
A |
B |
C |
D |
E |
|
①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与水在一定条件下反应生成C |
①由C、H两种元素组成; ②球棍模型为: 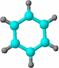 |
①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯。 |
①相对分子质量比C少2; ②能由C氧化而成; |
①由C、H、O三种元素组成; ②球棍模型为: 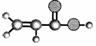 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为 ;写出在一定条件下,A生成高分子化合物的化学反应方程式 。
(2)写出B在浓硫酸作用下,与浓硝酸反应的化学方程式 。
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为 。
(4)写出由C氧化生成D的化学反应方程式 。
II.(第31题-第32题2小题任选一题作答,得分计入总分;若两题都做,则按顺序将第1小题即31题所得分数计入总分,直接将正确答案填在答题纸的相应空格内)
I.(第29题-第30题2小题任选一题作答,得分计入总分;若两题都做,则按顺序将第1小题即29题所得分数计入总分,直接将正确答案填在答题纸的相应空格内)
29.(10分)[化学-选修物质结构与性质]
现有A、B、C、D四种短周期元素(零族除外),请根据信息回答下列问题。
|
元素 |
A |
B |
C |
D |
|
性质或结构信息 |
元素非金属性较强,其最高价氧化物对应的水化物为强酸,但其单质稳定,常作保护气。 |
原子核外电子占了4个轨道 |
原子半径仅比氢原子大,其氢化物溶于水形成弱酸 |
原子核外有5种不同能量的电子,且s电子数比p电子数少1个 |
(1)A元素原子的核外电子排布式为: 。
(2)写出C元素的单质与水反应的化学方程式 ;A、C两元素的氢化物的稳定性强弱是 > (用化学式表示)。
(3)D元素最高价氧化物对应的水化物呈 (选填“酸性”、“碱性”或“两性”)。
(4)B元素最简单的氢化物分子为 分子(选填“极性”或“非极性”)。4g该氢化物在空气中完全燃烧生成液态水时,放出222.575kJ热量,写出表示该氢化物燃烧热的热化学方程式 。
28.(11分)元素推断题:
有短周期元素A、B、C、D、E,已知:
① 常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜;
② B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍;
③ E与A同周期,C、D、E三种元素形成的单质或化合物可发生如下图所示的反应。
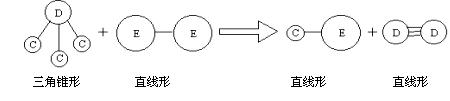
请回答下列问题:
(1) 写出A元素的单质与NaOH溶液反应的化学方程式 ;
(2)B元素在元素周期表第 周期第 族;
B的固态氧化物的晶体类型是 ;
(3)D元素的原子结构示意图是 ;
(4) B元素与E元素的最高价氧化物的水化物的酸性强弱 > (写化学式);
(5)写出元素E的单质与NaOH溶液反应的离子方程式 。
27.(15分)实验题:
I.(3分)下列实验不能成功的是______________(填字母代号)。
A.为了检验R-X是碘代烷,将R-X与NaOH水溶液共热,经充分反应后冷却,向冷却液中加稀HNO3酸化后,再加AgNO3溶液,观察沉淀颜色。
B.为检验淀粉是否水解,将淀粉与少量稀H2SO4共热一段时间,加入新制的Cu(OH)2 ,观察变化。
C.向银氨溶液中加入几滴乙醛后用酒精灯加热至沸制取银镜。
D.向混有乙酸的乙酸乙酯中加入NaOH溶液再分液,提纯乙酸乙酯。
E.无水乙醇与浓硫酸按1:3的体积比混合,迅速升温到170℃制取乙烯。
II.(12分)下图为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。图中:A处为无水乙醇(沸点为78℃);B处为绕成螺旋状的细铜丝或银丝;C处为无水CuSO4粉末;D处为碱石灰;F处为新制的碱性Cu(OH)2悬浊液。
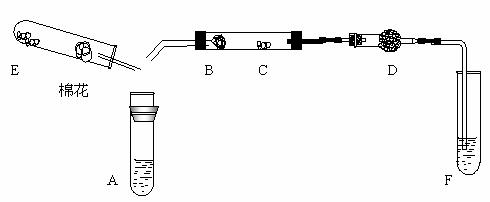
(1)在上述装置中,实验时需要加热的仪器按加热的先后顺序排列为(填序号)_________________,E处是一种纯净物,其发生反应的化学方程式为 。
(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是 ,D处使用碱石灰的作用是 。
(3) 能证明乙醇反应后所生成的产物的实验现象是 。
(4)本实验中若不加热E处,其他操作不变,则发现C处无明显变化,而F处现象与(3)相同,B处发生反应的化学方程式是 。
26.(9分)元素推断题:
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)M的元素符号为 ;X、Y、Z、L四种元素的原子半径从大到小的顺序是 (用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为 ,B的结构式为____________。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为 。 该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 kJ·mol-1 b.+29.7 kJ·mol-1 c.-20.6 kJ·mol-1 d.-241.8 kJ·mol-1
25.某有机化合物的结构简式如下,关于它的性质叙述中不正确的是( )
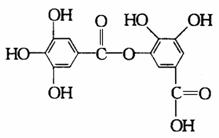
A.它有酸性,能与纯碱溶液反应
B.它在一定条件下可以水解只生成一种物质
C.1 mol该有机物最多能和7 mol NaOH反应
D.该有机物能发生取代反应
第Ⅱ卷(共60分)
第II卷非选择题分必考题和选考题两部分;第26题-第28题为必考题。第29题-第32题为选考题,请根据要求作答:
24. 描述 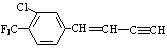 分子的下列叙述中,错误的是( )
分子的下列叙述中,错误的是( )
A. 与苯环直接相连的原子都在同一平面上
B. 分子中的碳原子分别采取sp、sp2、sp3杂化,分子中共有10个不饱和碳原子
C. 最多有18个原子可能处在同一个平面上
D. 分子式为C11H6ClF3
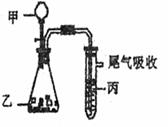
23. 用右图装置进行实验,下表中实验结果能说明结论的是( )
|
|
甲 |
乙 |
丙 |
结论 |
|
A. |
水 |
电石 |
溴水 |
稳定性:水>C2H2>Br2 |
|
B. |
盐酸 |
石灰石 |
苯酚钠溶液 |
酸性:HCl>H2CO3>苯酚 |
|
C. |
盐酸 |
FeS |
溴水 |
还原性:S2->Br->Cl- |
|
D. |
浓盐酸 |
KMnO4 |
KBr溶液 |
氧化性:Cl2> KMnO4
>Br2 |
22.元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测正确的是( )
 A.H2Z是含极性键的非极性分子
A.H2Z是含极性键的非极性分子
B.原子半径X>Y,离子半径X+>Z2-
C.同族元素中Z的氢化物沸点最低
D.XYZ3的晶体类型是离子晶体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com