
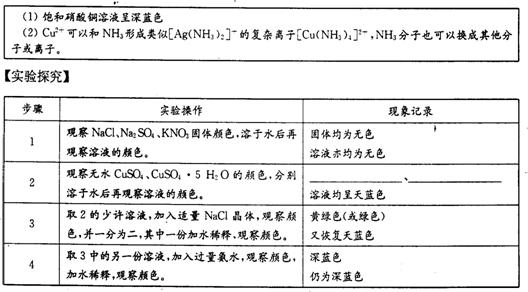
 【资料卡片】
【资料卡片】
【交流讨论】
(1)以上所得溶液或物质呈天蓝色的化学粒子符号是 (写化学式,下同);实验步骤4中呈深蓝色的化学粒子符号是 ;使饱和硝酸铜溶液呈深蓝色的化学粒子符号可能是 。
(2)请写出实验步骤3中“其中一份加水稀释”的反应离子的方程式: 。
(3)有资料上介绍浓硝酸与铜丝反应后得溶液颜色显蓝色,实验中得到却是绿色溶液,试写出显绿色的可能原因 ,设计两种不同的简单的实验方法证明你的解释:
方案① ;
方案② 。
17.下面是某化学学习小组的实验记录,请根据实验记录(部分需要补充)回答有关问题。
【研究课题】铜离子颜色的探究
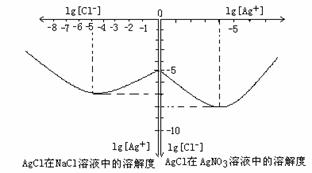
由以上信息可知:
(1)AgCl的溶度积常数的表达式为: ,由图知AgCl的溶度积常数为 。
(2)AgCl在NaCl溶液中的溶解出现如图所示情况(先变小后变大)的原因是:
。
(3)反应AgCl + KI== AgI + KCl能在水溶液中进行,是因为 。
(4)若在AgCl形成的浊液中滴加氨水有什么现象?
发生反应的离子方程式为 .
【解析】(1)KSP=c(Ag+)c(Cl-])(2分) ; 10―12 (2分)
(2)Cl―抑制了AgCl的溶解,但Cl―浓度的增大使AgCl形成络合物:
AgCl + Cl― ==[AgCl2]― (2分)
(3)AgI的溶解度小于AgCl的溶解度(2分)
(4)白色沉淀溶解,形成无色溶液(2分);AgCl+2NH3=Ag(NH3)2++ Cl―
16.沉淀物并非绝对不溶,其在水及各种不同的溶液中溶解有所不同,同离子效应、络合物的形成等都会使沉淀物的溶解度有所改变。下图是AgCl在NaCl、AgNO3 溶液中的溶解情况。
如:写成
[CuCl2]-(aq) CuCl(s) +
Cl-(aq)或[CuCl3]3-(aq)
CuCl(s) +
Cl-(aq)或[CuCl3]3-(aq) CuCl(s) +
2Cl-(aq)
CuCl(s) +
2Cl-(aq)
(5)溶液变蓝(1分)。4Cu++O2+4H+===4Cu2++2H2O(2分)
(4)(2分)[CuCl4]3-(aq) CuCl(s) +
3Cl-(aq)
CuCl(s) +
3Cl-(aq)
(其它合理答案也可给分)

 ①乙认为是溶解在溶液中的H2逸出,你认为是否有道理? ,理由是:
。
①乙认为是溶解在溶液中的H2逸出,你认为是否有道理? ,理由是:
。
②根据乙同学的实验甲同学作了如下猜想,是否成立,请你设计实验方案。
甲猜想
验证方法
预测现象及结论
甲认为铜片中
可能含有锌等杂质
(3)甲注意到乙的交流卡片记录的第(3)条现象中的白色沉淀。
分析:不可能是CuCl2,因为CuCl2溶液显蓝色或绿色,也不可能是氯化锌,因为稀释后溶液更稀,不会析出。并利用资料卡片中的①②大胆猜想,白色沉淀是生成的氯化亚铜。
请你帮他设计验证方案(若有多个只设计一个方案):
甲猜想
预计验证方法
预测的现象与结论
白色沉淀是
氯化亚铜
(4)乙的实验步骤(3)中,将反应后的溶液,隔绝空气,加入适量水,出现白色沉淀,实际上是一个平衡问题,请写出这一平衡关系:
(用离子方程式表示)。
(5)若乙同学在第三步实验中没有隔绝空气稀释,可能会出现什么现象?
如何解释?(用离子方程式表示) 。
【解析】 (本题共14分)
(1)铜、锌及浓盐酸一起组成了原电池,加快了反应速率(1分)
(2)①没有道理,(1分)因为氢气本身难溶于水(1分)
②(3分)(验证方法1分,现象和结论2分下同)
将铜片加入稀硫酸(或稀盐酸)中
若无气体放出,则不含锌等活泼金属杂质;
若有气体则有锌等杂质
(3)(3分)(其他答案合理也可给分)
乙
预计验证方法
预测的现象与结论
方案:向氯化亚铜悬浊液中加入氯化钾浓溶液中。
若白色沉淀消失且得无色溶液,则原白色沉淀为氯化亚铜,否则不是。
① R-CHO + 2Cu(OH)2 Cu2O(红色) + R-COOH + 2H2O
Cu2O(红色) + R-COOH + 2H2O
② Cu2+ + 4I-=2CuI(白色)↓+ I2
③ 氯化亚铜在不同浓度的KCl溶液中可形成[CuCl2]-、[CuCl3]2- 、[CuCl4]3-等离子,且它们在溶液中均为无色。
实验过程:
甲:将锌放入浓盐酸中,反应速率较快;
乙:将实验过程记录下来,交流并讨论:
|