
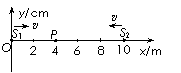
18. 如图所示,均匀介质中两波源S1、S2,分别位于x轴上x1=0、x2=10m处,在t=0时刻同时从各自平衡位置开始沿y轴正方向做简谐运动,周期均为T=1s,产生的机械波的传播速度均为v=4 m/s,振幅均为A=2 cm。质点P位于x轴上xp=4m处,设质点P从t=0到t=2.5s内通过的路程为L,在t=3.25 s时刻的位置为y,则
 A.L=4 cm
A.L=4 cm
B.L=12 cm
C.y=2 cm
D.y=-2 cm
17.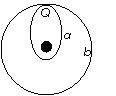 发射地球同步通信卫星的基本方法是,先用火箭将卫星送入一近地椭圆轨道a运行,然后开动星载火箭变轨,将其送入与地球自转同步的轨道b,变轨点选在轨道a与轨道b内切的Q点,如图所示。下列说法正确的是
发射地球同步通信卫星的基本方法是,先用火箭将卫星送入一近地椭圆轨道a运行,然后开动星载火箭变轨,将其送入与地球自转同步的轨道b,变轨点选在轨道a与轨道b内切的Q点,如图所示。下列说法正确的是


A.卫星在Q点变轨时加速度变小
B.卫星变轨后在Q点的机械能比变轨前的大
C.卫星在轨道b运行速度小于在轨道a运行时的最小速度
D.卫星在Q点变轨时星载火箭喷射气体的方向与卫星线速度方向相同
16. 氢原子从n=3的能级跃迁到n=2的能级辐射出a光,从n=4的能级跃迁到n=2的能级辐射出b光。则
A.在同一双缝干涉装置进行实验,用a光照射时相邻亮纹间的距离比用b光照射时的大
B.若用a光照某金属不能发生光电效应,则用b光照该金属也不能发生光电效应
C.在同一种玻璃介质中,a光发生全反射的临界角比b光的小
D.在同一种玻璃介质中,a光传播速度比b光的小
15. 用α粒子轰击某原子核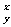 Z,产生一个
Z,产生一个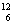 C和一个中子。由此可知
C和一个中子。由此可知
A.x=8,y=3 B.x=9,y=5 C.x=8,y=5 D.x=9,y=4
14. 下列说法正确的是


A.气体能充满任何容器是因为分子间的排斥力大于吸引力
B.可以将流散到周围环境中的内能重新收集起来加以利用而不引起其他变化
C.测出油酸分子的大小,并已知油酸的摩尔体积,就可以估算出阿伏伽德罗常数
D.一定质量的气体,温度升高时,压强一定变大
29.(14分)以工业废铁屑为原料生产氧化铁红颜料并进行适当的综合利用,其主要流程如下:
已知:FeSO4溶液与稍过量的NH4HCO3溶液混合,得到含FeCO3的悬浊液。


请回答下列问题:
(1)用5 % 的Na2CO3热溶液去油污(主要成分是油脂)时,反应生成的有机产物是(写名称): 。
(2)反应Ⅰ需要控制在50 ℃-80 ℃以提高反应速率,如果硫酸过量,反应混合液与空气接触会发生副反应,如何检验副反应的产物?
。
(3)写出在空气中煅烧沉淀的化学反应方程式: 。
(4)本流程中产生的CO2和H2,在催化剂作用下按体积比1∶1合成一种重要的有机化工原料R,该合成符合绿色化学要求。上述合成反应∆H=+14.9 kJ/mol,则加压、降温可以使平衡分别向 、 方向移动。已知液体R的燃烧热为254.6 kJ/mol,则R完全燃烧的热化学方程式为 。
(5)摩尔盐常用于定量分析并用于医药、电镀方面。已知摩尔盐中结晶水的含量为27.6 %,n(Fe2+)∶n(SO2-4 )=1∶2,则摩尔盐的化学式中,结晶水数目x的计算式为:
x= 。
绵阳市高2010级第三次诊断性考试
28.(16分)烃A的相对分子质量为42,B与新制的Cu(OH)2加热至沸腾产生红色沉淀,E可作隐形眼镜材料。下列各物质的转化关系如下图所示:


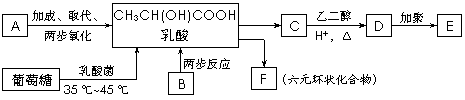
已知: HCN--→
HCN--→  H2O,H+----→
H2O,H+----→  ,请回答下列问题:
,请回答下列问题:
(1)多羟基醛、多羟基酮以及水解能生成它们的有机物都属于糖类,写出乳酸的同分异
构体中,属于糖的一种有机物的结构简式 。
(2)写出以下物质的结构简式:A ,E ,F 。
(3)B的名称是 ,由B合成乳酸的第一步反应属于 反应。
(4)由A合成乳酸的第二步反应化学方程式是(自选合适的无机试剂):
;
(5) C转化为D的化学方程式是 。
27.(14分)用A-M分别代表一种物质,它们之间的转化关系如下图所示(部分生成物略去)。其中A为紫色晶体,B、H、J均为常见的单质气体,单质E在浓硝酸中钝化。
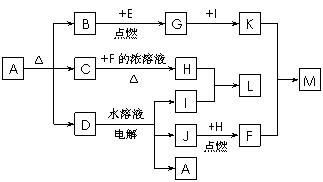 请回答下列问题:
请回答下列问题:
(1)D的化学式是 ,L由3种元素组成,其电子式是
。
(2)E元素在周期表中的位置是 。工业上可利用C与E在高温下反应冶炼金属,该反应的化学方程式是
。
 (3)用C与F溶液制H气体时,发生反应的化学方程式是
。
(3)用C与F溶液制H气体时,发生反应的化学方程式是
。
(4)用石墨电极电解D的水溶液时,阳极的电极反应式是 。
(5)在500 mL 0.2 mol/L K物质的水溶液中逐滴加入F的水溶液并不断搅拌,溶液中析出沉淀的质量发生变化,在右图中画出沉淀质量随加入F的物质的量的变化曲线。
26.(16分)某化学兴趣小组用铜和浓硫酸制取SO2,并依次检验SO2具有酸性氧化物的性质和还原性、漂白性、氧化性,所用仪器如下图所示(图中连接胶管、夹持和加热装置省略):


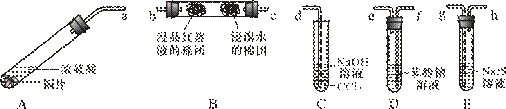
查阅资料可知,HSO-3 的酸性强弱与H2CO3相近。请回答下列问题:
(1)上述装置的接口连接顺序依次是 (填导管接口字母)。
(2)装置A、D中发生反应的化学方程式是:A , D 。
(3)证明SO2具有氧化性的现象是 ;证明SO2具有还原性的实验中,反应的离子方程式是 。
(4)C试管中NaOH溶液的作用是 ,CCl4的作用是 。
(5)实验过程中还观察到A试管内产生黑色沉淀,查资料可知,该黑色沉淀是副反应产生的CuS和Cu2S。收集黑色沉淀经过滤、洗净、干燥后放入氧气流中加热,然后冷却,用电子天平称重发现黑色固体质量减少a %,则a值范围是 。
13. 将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH===NaNO2+NaNO3+H2O、NO+NO2+2NaOH===2NaNO2+H2O
则生成的盐溶液中NaNO3的物质的量为


A. 0.2 mol B. 0.4 mol C. 0.6 mol D. 0.8 mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com