
21.(6分) , , 。
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
|
|
|
|
|
|
|
|
|
|
第Ⅱ卷(非选择题 共50分)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
78.5℃、118℃、77.1℃)
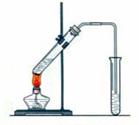
(1)在左侧试管中除了加入乙醇和乙酸外,还应加入的试剂是
该试剂的作用是:①_____ _ __ ②_____________ 。
(2)反应结束后将右侧的试管取下,振荡、静置,观察到的现象是
。
(3)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作流程,
请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
试剂a是__________,b是_______________;
分离方法①是__________,②是______________,③是_______________。
写出C → D 反应的化学方程式 。
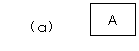
|
|

|
 高一学年化学学科试题答题卡
高一学年化学学科试题答题卡
第Ⅰ卷(选择题 共50分)
26.(10分)实验室合成乙酸乙酯如(右图所示),得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:(已知:乙醇、乙酸、乙酸乙酯的沸点依次是
25.(10分)
某同学在用稀硫酸与锌粒(黄豆粒大小)制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有 ;
(2)硫酸铜溶液可以加快氢气生成速率的原因是 ;
(3)要加快上述实验中气体产生的速率,还可采取的措施有
、 、 。
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
请完成此实验设计,其中:V1= ,V6= ,V9= ;
|
实 验 混合溶液 |
A |
B |
C |
D |
E |
F |
|
|
4mol/LH2SO4/mL |
40 |
V1 |
V2 |
V3 |
V4 |
V5 |
|
|
CuSO4/mL |
0 |
1 |
5 |
10 |
V6 |
40 |
|
|
H2O/mL |
V7 |
V8 |
V9 |
V10 |
15 |
0 |
该同学最后得出的结论为:当加入少量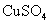 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的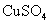 溶液超过一定量时,生成氢气的速率反而会下降。
溶液超过一定量时,生成氢气的速率反而会下降。
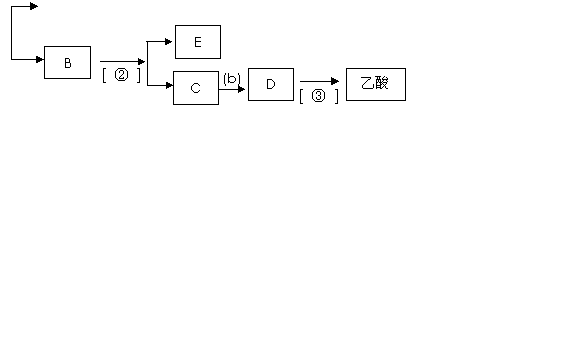
24.(10分)某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高经济效益,而且还能防止环境污染,现按以下方式进行:
|
|
|
①
|
|
|
|
|
|
|
|
|
|
|||||
|
|||||
|
|||||
(1)写出A、B、F的名称分别为 、 、 。
(2)E的结构简式为 。
(3)写出反应③和反应⑤的化学方程式。
反应③ 。
反应⑤ 。
(4)写出比E多一个碳的同系物发生加聚反应的化学方程式 。
23.(10分)
I.在某体积为2L的密闭容器中充入1.5mol NO2和2mol CO,一定条件下发生反应:NO2+CO===CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,
①该段时间内,用CO2表示的平均反应速率为
②2 min时,容器内气体的总物质的量为 。
③假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量 (填“大于”、“小于”或“等于”)2 min时容器内气体的总物质的量。
II.将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先处理好),并架在铁架台上,下面放置一个盛有沙子的蒸发皿。请写出引发铝热反应的操作及该反应的化学方程式:
操作
化学方程式 。
22.(4分)下列反应中属于取代反应的是 ,属于加成反应的是 。
①甲烷在光照下与氯气反应 ②乙烯使溴水褪色 ③乙烯使酸性高锰酸钾溶液褪色 ④苯与液溴反应 ⑤乙醇与乙酸酯化 ⑥苯与浓硝酸和浓硫酸的混酸反应
21.(6分)下面列出了几组物质,请将物质的合适序号填写在空格上。
互为同位素的是 ,互为同系物的是 ,互为同分异构体的是 。
①金刚石与“足球烯”C60; ②D与T; ③16O、17O和18O;
④氧气(O2)与臭氧(O3); ⑤CH4和CH3CH2CH3;
⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);
|
⑦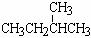 和 CH3-C-CH3
和 CH3-C-CH3
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com