
27.(12分)(1)已知20.0gNaOH稀溶液跟足量稀盐酸反应,放出28.68kJ热量,那么此反应数据表明:如果NaOH稀溶液跟稀盐酸中和生成18g水时,该反应放出热量_________________kJ,由此测得的中和热为___________kJ/mol
(2)已知断开1 molH-H键、1mol Br-Br键、1mol H-Br键分别需要吸收的能量为436kJ、193kJ、366kJ.。 计算H2和Br2反应生成1mol HBr需_______(填“吸收”或“放出”)能量_______kJ。
26.(15分)(1)分别用电子式表示HClO、MgCl2的形成过程
(2)已知下列原电池的总反应式:Cu+2FeCl3==CuCl2+2FeCl2,请写出电极反应式:
正极反应式为:
负极反应式为:
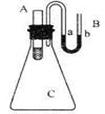 (3) 如图所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面高于b端液面的是____________。(填序号)
(3) 如图所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面高于b端液面的是____________。(填序号)
25. 在25 ℃,101 kPa下,1 mol的白磷(化学式为P4)完全燃烧放出的热量比4 mol的红磷(化学式为P)完全燃烧放出的热量多。反应方程式分别为:
P4 (s) + 5O2 (g) = P4O10 (s) 4P (s)+ 5O2 (g) = P4O10 (s)
由此判断,下列说法正确的是( )
A.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷高
B.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷低
C.由红磷转化为白磷是放热反应,等质量时红磷能量比白磷高
D.由红磷转化为白磷是吸热反应,等质量时红磷能量比白磷低
第Ⅱ卷(非选择题,共60分)
24.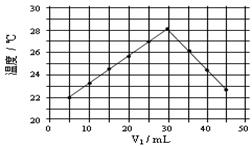 将V1mL1.0mol·L-1
HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )
将V1mL1.0mol·L-1
HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )
A.做该实验时环境温度为22℃
B.该实验表明化学能可能转化为热能
C.NaOH溶液的浓度约为1.0mol/L·L-1
D.该实验表明有水生成的反应都是放热反应
23. 下列物质中,既含有极性共价键又含有非极性共价键的是( )
A.NH4Cl B.Na2O2 C.H2O2 D.CH4
22.有a、b、c、d四种金属。将a与b用导线连接起来,浸入电解质溶液中,外电路电流从b流向a。将a、d分别投入等浓度盐酸中,d比a反应剧烈。将铜浸入b的盐溶液里,无明显变化。如果把铜浸入c的盐溶液里,有金属c析出。据此判断它们的活动性由强到弱的顺序是( )
A. dcab B. dabc C. dbac D. badc
21. 将足量的CO2通入KOH和Ca(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(v)的关系正确的是( )

A B C D
20. 已知2H→H2并放出437.6kJ的热量,下列说法正确的是( )
A.氢气分子内每个氢原子都达到8电子稳定结构
B.氢气分子的能量比氢原子的能量低
C.1molH2离解成2molH 要放出437.6kJ 热量
D.氢原子比氢气分子稳定
19. 短周期元素X和Y,X原子的电子层数为n,最外层电子数为(2n+1),Y原子最外层电子数是次外层电子数的3倍。下列说法一定正确的是( ) A.X和Y都是非金属元素,其中X的最高化合价为+5价 B.X与Y所能形成的化合物都是共价化合物 C.元素X可形成化学式为KXO3的盐
D.X的氢化物不溶于水
18. 下列关于元素周期表和元素周期律的说法不正确的是( ) A.从氟到碘,其氢化物的稳定性逐渐减弱 B.因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强 C.第三周期从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强 D.氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性弱
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com