
25、(6分)某烃能使酸性KMnO4溶液褪色但不能使Br2的CCl4溶液褪色。相同条件下该烃的蒸气对H2的相对密度为60,且12.0 g该烃完全燃烧后生成10.8 g水和39.6 g CO2,又知该烃的一氯代物只有两种同分异构体,试确定该烃的结构简式。
24、(6分)(1)下列ΔH表示物质燃烧热的是 __ ,表示物质中和热的是 (填ΔH1、ΔH2、ΔH3等)。
A.2H2(g)+O2(g)===2H2O(l);ΔH1
B.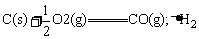
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g);ΔH3 D.C(s)+O2(g)===CO2(g);ΔH4
E.C6H12O6(s)+6O2(g)===6CO2(g) + 6H2O(l);ΔH5
F.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l);ΔH6
G.2NaOH(aq)+H2SO4(aq)===Na2SO4(aq)+2H2O(l);ΔH7
H.CH3COOH(aq)+NaOH(aq)===CH3COONa(aq)+H2O(l);ΔH8
(2)2.00 g C2H2气体完全燃烧生成液态水和CO2气体,放出99.6 kJ的热量,写出该反应的燃 烧热化学反应方程式 ;
(3)充分燃烧一定量的丁烷放出的热量大小为QkJ,生成的CO2恰好与5mol/L 100ml KOH溶液完全反应生成酸式盐,则完全燃烧1mol丁烷的反应热ΔH为 。
23、(7分)下图中A为直流电源,B为浸透饱和食盐水溶液和酚酞试液的滤纸,C为盛有CuSO4溶液的电解槽,e为铜电极,f为铁电极。接通电路后,发现e电极质量增加,则:
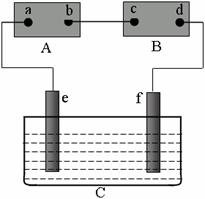
⑴电源A上b为 极;
⑵电解过程中,d点出现的现象是 ,c点的电极反为 ,B上的总反应为 ;
⑶电解过程中,c的溶液中可观察到的现象是 ,e电极上的电极反应式为 _____ ,f电极上的电极反应式为 。
22、(7分)根据下图转化关系填空:
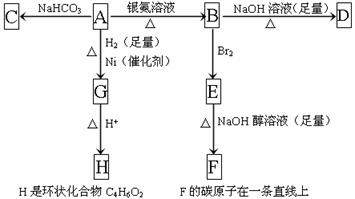
⑴化合物A含有的官能团是 。
⑵B在酸性条件下与Br2反应得到E,E在足量NaOH醇溶液作用下转变成F时发生两种反应,此两种反应类型分别是 。
⑶D的结构简式是 。
⑷1mol A与2 mol H2反应生成1 mol G,其反应方程式是 。
⑸与A有相同官能团的A的同分异构体的结构简式是 。
21、(6分)有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、Cl-和I-。取该溶液进行以下实验:
⑴用pH试纸检验,表明溶液呈强酸性;
⑵取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色;
⑶另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
⑷取部分上述碱性溶液加热,加Na2CO3溶液,有白色沉淀生成;
⑸将⑶得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实判断:在该溶液中肯定存在的离子是 ,肯定不存在的离子是 ,不能确定是否存在的离子是 。
20、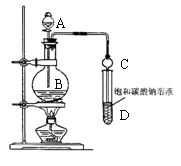 (7分)某课外实验小组设计的制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。请回答:
(7分)某课外实验小组设计的制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。请回答:
⑴浓硫酸的作用是 ;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学反应方程式 ;
⑵球形漏斗C的作用是 。若反应前向D中加入几滴酚酞试液,溶液呈红色,产生此现象的原因是(用离子方程式表示) ;反应结束后D中的现象是 。
19、(5分)在Fe(OH)3胶体中逐滴加入HI稀溶液,会出现一系列变化:
⑴先出现红褐色沉淀,原因是: ;
⑵随后沉淀溶解,溶液呈黄色,写出此过程反应的离子方程式: ;
⑶最后溶液颜色加深,原因是: ,此过程的离子方程式是: ;
⑷如用稀盐酸代替HI稀溶液,能出现上述哪些相同的实验现象:__________(写序号)。
18、分析化学中常用X射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上。其晶体中的阴离子晶胞结构如图示,下列说法不正确的是( )
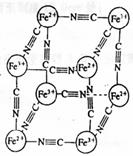 A.该晶体是离子晶体
A.该晶体是离子晶体
B.M的离子位于上述晶胞面心,呈+2价
C.晶体的化学式可表示为MFe2(CN)6,且M为+1价
D.M的离子位于上述晶胞体心,呈+2价
第Ⅱ卷(非选择题,共52分)
17、下列离子方程式书写不正确的是( )
A.少量铁粉加入稀硝酸中:3Fe + 8H+ + 2NO3-=3Fe2+ + 2NO↑+ 4H2O
B.Ca(HCO3)2溶液与过量Ca(OH)2溶液反应:Ca2+ + HCO3- + OH-=CaCO3↓+ H2O
C.NH4HCO3溶液和过量Ba(OH)2溶液共热:2HCO3-+2OH- + Ba2+=BaCO3↓+ CO32- +2H2O
D.Na2S溶液中通入足量H2S:S2- + H2S=2HS-
16、用含有少量银和锌的粗铜做阳极,纯铜片做阴极,CuSO4溶液做电解液,电解一段时间后,阳极质量减少了mg,则( )
A.电解液质量增加mg B.阴极质量增加xg,xx>m
C.阴极质量增加mg D.阴极质量增加yg,y<m
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com