
27.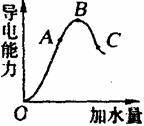 (6分)在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如右图所示。请回答:
(6分)在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如右图所示。请回答:
(1)“O”点导电能力为“0”的理由是
_______________________。
(2)A、B、C三点pH值由大到小的顺序是
_______________________。
(3)A、B、C三点电离度最大的是____________________。
26.(4分)在95℃时,纯水的pH (填“大于”“小于”“等于”)7,所选择的
理由是 。
25.水的电离过程为H2O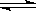 H++OH-,在不同温度下其平衡常数为
H++OH-,在不同温度下其平衡常数为
K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述正确的是
A.C(H+)随着温度升高而降低
B.在35℃时,C(H+)>C(OH-)
C.水的电离度?(25℃)>?(35℃)
D.水的电离是吸热的
24.将pH= l的盐酸平均分成 2份,l份加适量水,另1份加入与该盐酸物质的量浓度
相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为( )
A. 9 B.10 C.11 D.12
23.在相同温度时100mL 0.01mol/L的醋酸溶液与10mL 0.01mol/L的醋酸溶液相比较,
下列数值前者大于后者的是 ( )
A.中和时所需NaOH的量 B.电离度
C.对的物质的量 D.CH3COOH的物质的量
22.某强酸溶液pH=a,强碱溶液pH=b,已知a+b=12,酸碱溶液混合pH=7,则酸溶
液体积V(酸)和碱溶液体积V(碱)的正确关系为 ( )
A.V(酸)=102V(碱) B.V(碱)=102V(酸).
C.V(酸)=2V(碱) D.V(碱)=2V(酸)
21.pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=11,则强碱与强酸的
体积比是 ( ).
A.11∶1 B.9∶1 C.1∶11 D.1∶9.
20.pH=9 的Ba(OH)2溶液与pH=12的KOH溶液,按4︰1的体积比混合,则混合溶
液中H+浓度为(单位:mol·L-1) ( )
A.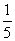 ×(4×10-9+1×10-12)
B.
×(4×10-9+1×10-12)
B.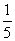 ×(8×10-9+1×10-12)
×(8×10-9+1×10-12)
C.5×10-10 D.5×10-12
19.有人曾建议用AG表示溶液的酸度(acidity arede),AG的定义为 ( )
AG=lg([H+]/[OH-])。下列表述正确的是
A.在25℃时,若溶液呈中性,则pH=7,AG=1
B.在25℃时,若溶液呈酸性,则pH<7,AG<0
C.在25℃时,岩溶液呈碱性,则pH>7,AG>0
D.在25℃时,溶液的pH与AG的换算公式为AG=2(7-pH)
18.某温度下,重水D2O的离子积为1.6×10-15,若用pH一样的定义来规定
pD=-lgc(D+),以下关于pD的叙述正确的是 ( )
A.中性溶液的pD=7.0.
B.含0.01 mol的NaOD的D2O溶液1L,其pD=12.0.
C.溶解0.01 mol的DCl的D2O溶液1L,其pD=2.0.
D.在100 mL 0.25 mol·L-1的DCl重水溶液中,加入50 mL 0.2mol·L-1的NaOD的
重水溶液,其pD=1.0.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com