
3.匀变速直线运动的位移公式是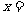 ,其中是矢量的物理量有
,是标量的物理量有
。
,其中是矢量的物理量有
,是标量的物理量有
。
2.采用 的思想我们可推导出匀变速直线运动的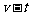 图线与时间轴所围的“面积”表示
。时间轴上方所围的“面积”表示 ,时间轴下方所围的面积表示 。
图线与时间轴所围的“面积”表示
。时间轴上方所围的“面积”表示 ,时间轴下方所围的面积表示 。
1.匀速直线运动的速度-时间图线与时间轴所围的“面积”表示
,其位移公式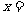
。
31.氢氧化镁难溶于水,但它所溶解的部分全部电离。t℃时,饱和Mg(OH)2溶液的pH=11,
若不考虑KW的变化,则该温度下Mg(OH)2的溶解度为?
30.(11分)已知氨水的电离度与醋酸的电离度在同温同浓度下相等,溶有一定量氨的氯化铵溶液呈碱性。现向少量的Mg(OH)2悬浊液中,加入适量的饱和氯化铵溶液,固体完全溶解。甲同学的解释是.
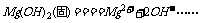 ①
①
NH4++H2O===NH3·H2O+H+……②
H++OH-===H2O……③
由于NH4+水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;乙同学的解释是.
Mg(OH)2(固)====Mg2++2OH-……①
NH4++OH-===NH3·H2O……②
由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确,他选用的试剂是___________(填写编号)。
A.NH4NO3 B.CH3COONH4 C.Na2CO3 D.NH3·H2O
(2)请你说明丙同学作出该选择的理由_________________________________。
(3)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理___________(填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊溶解的离子方程式_________________。
29.(4分)配制氯化铁溶液常出现浑浊现象,其原因是___________________________。
如何操作既可得到透明溶液而又不引进杂质离子____________________________
_______________________________________
28.(3分)将0.2 mol·L-1的CH3COONa溶液与0.1mol·L-1 HCl等体积混合后,溶液
中各种离子的浓度按其从大到小的顺序应为 。
27.(6分)在1 mol·L-1 Na2CO3溶液中,欲使CO32-的浓度尽量接近1mol·L-1,则应向
溶液中加入少量的_______________________或______________________________
原因是 。
26.某元素X的相对原子质量为a,它的最高氧化物的水化物的分子式为HmXOn(m>1)。
下列有关叙述中一定正确的是 ( )
A.该酸的水溶液中,c(H+)∶c(XO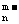 )=n∶1
)=n∶1
B.该酸的摩尔质量为(m+a+16n)g
C.100 mL该酸溶液,能中和4g NaOH
D.若0.1molL-1该酸溶液的pH=1,则NamXOn的水溶液的pH>7
25.下列说法正确的是 ( )
A.水解反应是吸热反应 B.升高温度可以抑制盐类的水解
C.正盐水溶液pH均为7 D.硫酸钠水溶液pH小于7
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com