
15、下列分子中,所有原子的最外层均为8电子结构的是( )
A.BeCl2 B.HClO C.PCl5 D.P4
14.下列离子方程式书写正确的是( )
A.溴乙烷与6mol/L的氢氧化钠水溶液共热:
C2H5Br+OH-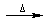 CH2=CH2↑+Br-+H2O
CH2=CH2↑+Br-+H2O
B.等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合:
Ca2++2HCO3-+2OH- CaCO3↓+CO32-+2H2O
CaCO3↓+CO32-+2H2O
C.在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入1~2滴盐酸:
3Fe2++4H++NO3- 3Fe3++NO↑+2H2O
3Fe3++NO↑+2H2O
D.在H2O2中加入酸性高锰酸钾溶液:
2MnO4-+6H++5H2O2 2Mn2++5O2↑+8H2O
2Mn2++5O2↑+8H2O
13.在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.无色溶液:Ca2+、H+、Cl-、HSO3-
B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C.FeCl2溶液:K+、Na+、SO42-、AlO2-
D.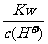 =0.1 mol/L的溶液:Na+、K+、SiO32-、NO3-
=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3-
12.下列有关实验操作的说法正确的是( )
A.可用25 mL碱式滴定管量取20.00 mL KMnO4 溶液
B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干
D.将金属钠在研体中研成粉末,使钠与水反应的实验更安全
11、从下列事实所列出的相应结论正确的是( )
|
|
实
验 事 实 |
结 论 |
|
A |
Cl2的水溶液可以导电 |
Cl2是电解质 |
|
B |
SO2通入硝酸钡溶液出现白色沉淀 |
BaSO3不溶于强酸 |
|
C |
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 |
结合H+的能力:CO32-<
AlO2- |
|
D |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
10、下列反应的离子方程式正确的是( )
A.NaHS水解:HS-+H2O H3O++S2-
H3O++S2-
B.钠与CuSO4溶液反应:2Na+Cu2+=Cu+2Na+
C.向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+
D.澄清石灰水跟盐酸反应:H++OH-=H2O
9、 短周期元素X、Y的原子序数相差2,下列叙述正确的是( )
A.X与Y不可能位于同一周期
B.X与Y不可能形成原子个数比为1:1型离子化合物
C.X离子与Y离子电子层结构可以相同,也可以不同
D.X与Y形成的共价化合物中,各原子最外层一定满足8电子的稳定结构
8、A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )
A. B、A、D、C、E B. E、C、D、B、A
C. A、B、C、D、E D. C、D、A、B、E
7、下列各组物质相互混合反应,既有气体生成最终又有沉淀生成的是( )
①金属钠投入FeCl3溶液中 ②过量的NaOH溶液和明矾溶液
③少量的电石加到过量的NaHCO3溶液中 ④ Na2O2投入FeCl2溶液中
⑤浓硫酸铵溶液加入到浓氢氧化钡中
A.①④ B.②③ C.①③④⑤ D.①③④
6、高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。
湿法制备的主要反应方程为:2Fe(OH)3+3ClO―+4OH―=2FeO42-+3Cl―+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4 +2Na2SO4
下列有关说法不正确的是( )
A.高铁酸钾中铁显+3价
B.湿法中每生成1mol Na2FeO4转移3 mol电子
C.干法中每生成1mol Na2FeO4转移4 mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能吸附水中的悬浮杂质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com