
4、徒有万般“羡鱼”心,而无一丝“结网”意,结果定会一事无成。这道理虽然浅显,但实际上却不是每个人都能清楚认识到的。有的人希望成为爱迪生式的“发明大王”,可是却畏于钻研科学知识之难;有的人想继莫泊桑之后,再夺“短篇小说之王”的桂冠,但又慑于常年练笔之艰辛;有的人想一鸣惊人成为“音乐巨匠”,却惰于在五线谱的田地上埋首耕耘;有的人愿自己成为体育明星,却怠于“闻鸡起舞”进行训练。如此心怀鸿鹄之志,而身属燕雀之行,连一条小小的鱼都会捉不到,更何况要实现那恢宏的大志呢!
3、苦难,对于天才是一块垫脚石,对于能干的人是一笔财富,对于弱者是一个万丈深渊成功,对于永不懈怠的人是一座里程碑,对于骄傲自满的人是一个包袱,对于不求进取的人是一桩祸患。对于志向远大的人是向上攀登的阶梯,对于心有小志的人是一生荣耀;对于胸无大志的人,无底深渊;对于努力者,奖励;对于耕耘者,收获;对于骄傲者,过眼云烟;对于目标远大者,小的驿站;对于奋斗者,一座灯塔;对于懒惰者,一个美丽的梦;对于奋进的人,另一段艰难跋涉的开端;对于知足的人,幸福的顶峰;对于失败者,遥不可及的梦想。
2、如果有人问,“春天是怎样的?”丘迟会说“草长莺飞,杂花生树”;白居易说是“日出江花红胜火,春来江水绿如蓝”;苏轼说是“蒌蒿满地芦芽短,正是河豚欲上时”;李白说是“燕草如碧丝,秦桑低绿枝”;杜牧说是“千里莺啼绿映红,水村山郭酒旗风”……”
1、屈原在其“联齐抗秦”的政治主张未被采纳却“忠而被谤”的苦难中,仍能“哀怨托离骚,孤忠报楚国”;司马迁因秉笔直书,“不溢美”“不隐恶”而遭受腐刑,却能“忧愁发愤,著成信史照尘寰”;杜甫虽“长夜沾湿”“布衾似铁”却依然“民间疾苦,笔底波澜”,吟诵出“大庇天下寒士”的千古绝唱。他们不是在时光的流逝中淡化苦难,而是用全部的热情和才智与命运进行了不屈的抗争,升华了自己也点缀了历史。
1吸热反应和放热反应
旧化学键断裂需要 ____ 能量,形成化学键要 __ 能量(化学反应的实质)
⑴若为吸热反应,此时反应物总能量 _ 生成物总能量,反应过程中__________能量
⑵若为放热反应,此时反应物总能量 _ 生成物总能量,反应过程中__________能量2.吸热反应与放热反应的判断
|
|
吸热反应 |
放热反应 |
|
△H |
△H 0 |
△H 0 |
|
能量变化 |
反应物总能量 生成物的总能量(填“大于”或“小于”) |
反应物总能量 生成物的总能量(填“大于”或“小于”) |
2常见的放热反应
如:燃料的燃烧、中和反应、金属与酸、大多数化合反应……
3常见的吸热反应
如:①大多数分解反应 ;②C、H2、CO等热还原反应;③铵盐和碱的反应
例2.下列说法不正确的是( )
A.化学反应除了生成新物质外,还伴随着能量的变化
B.放热反应可能需要加热才可以发生 C.反应条件是加热的反应都是吸热反应
D.化学反应放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量
4热化学方程式
已知2H2(g)+O2(g)=2H2O(l)
△H=-571.6KJ/mol
H2(g)+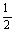 O2(g)=H2O(g) △H=-241.8KJ/mol
O2(g)=H2O(g) △H=-241.8KJ/mol
则, H2(g)+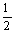 O2(g)=H2O(l) △H= KJ/mol 2H2(g)+O2(g)=2H2O(g)△H= KJ/mol
O2(g)=H2O(l) △H= KJ/mol 2H2(g)+O2(g)=2H2O(g)△H= KJ/mol
练习:1mol甲烷燃烧时,生成液态水和二氧化碳,同时放出890.3kJ的能量。
请写出该反应的热化学方程式。
(二)化学反应限度(化学平衡)
1.研究对象---- 反应
可逆反应:___________________________________________________________________
可逆反应的特点:_____________________________________________________________
2.化学平衡状态
可逆反应在一定条件下进行到一定程度时, 和 相等,反应物和生成物的 _____________ 不再发生变化,称为化学平衡状态。
注:化学平衡状态的判断
①各组分的含量(如:质量、物质的量、体积、浓度、质量分数等)保持不变;
②正逆反应速率相等(包括反应方向相对和反应速率对应相等)
练习 使反应4NH3(g)+3O2(g)  2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均速率v(X)为
2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均速率v(X)为
A. v(NH3)=0.02mol·L-1·s-1 B. v(O2)=0.003mol·L-1·s-1
C. v(N2)=0.02mol·L-1·s-1 D. v(H2O)=0.02mol·L-1·s-1
★3.关于化学平衡的计算“三段式”
aA + bB = cC + dD
起始量(浓度或物质的量)
转化量(浓度或物质的量)
平衡量(浓度或物质的量)
例6恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13mol ; nt(NH3)=6 mol,计算a的值。
(2)反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(一) 化学反应速率___________________________________________________________
1. 表示方法:V= 2.单位: 或
3.特点
⑴均取正值 ⑵同一反应用不同物质表示数值不一定相同
⑶同一反应,各物质表示的速率比等于化学计量数之比(等于各物质的变化量之比)
如:mA(g)+nB(g) pC(g)+ q(g)则有m:n:p:q=____________________________
pC(g)+ q(g)则有m:n:p:q=____________________________
例:反应4A(s)+3B(g) 2C(g)+ D(g),经2min,B的浓度减少0.6mol/L。对此反应速率的表示正确的是( )
2C(g)+ D(g),经2min,B的浓度减少0.6mol/L。对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol·(L·min)-1
B.分别用B、C、D表示的反应速率其比值是3:2:1
C.此2min内的反应速率,用B表示是0.6 mol·(L·min)-1
D.在这2min内用B和C表示的反应速率的值是相等的
4.反应速率的影响因素
⑴内因-- _______(决定因素)
⑵外因--① ② ③ ④ ⑤_________________其它因素
外界条件对化学反应速率的影响
|
外界条件 |
措施 |
化学反应速率变化 |
外界条件 |
措施 |
外界条件 |
|
温度 |
升温 |
|
压强 |
增大 |
|
|
降温 |
|
降低 |
|
||
|
浓度 |
增大 |
|
催化剂 |
使用催化剂 |
|
|
减小 |
|
接触面积 |
增大接触面积 |
|
14、写出下列物质的电子式
氟化钙 Na2O 硫化钾
HCl H2O NaOH
CH4 C2H4 氯化钠 _____________________
第十讲(下) 化学反应速率与能量
[知识梳理]
13、在下列物质中:①氨气 ②氯化氢 ③氯化铵 ④干冰 ⑤苛性钠 ⑥食盐 ⑦冰 ⑧氩气 ⑨氧化钠 ⑩双氧水 11氢气 12甲烷 13H2SO4 14Cl2 15CH3COOH
(1)只有共价键的是 (2)只有离子键的是
(3)既有离子键又有共价键的是 (4)共价化合物有_____________________
12、最近,科学家研制得一种新的分子,它具有空心的类似足球状的结构,化学式为C60。下列说法正确的是
A、C60是一种新型的化合物 B、C60和石墨都是含碳元素的单质
C、C60中含离子键 D、C60与12C互为同素异形体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com