
10.[答案]
评分标准:答对试剂给2分,答对现象者给1分,如有其他合理答案,参照上列标准给分。
[相应知识点归纳]
(1)共性归纳:氯化钠和氯化铵都是盐酸盐;氮气和二氧化碳都是空气的成分,通常情况下都不支持燃烧;硫酸钠和碳酸钠都是可溶性钠盐;氯化铁和氯化亚铁都是铁元素的盐酸盐;乙烯和乙烷都是含有两个碳原子的烃分子。
(2)物质的鉴别根据物理性质鉴别:颜色、气味、密度、溶解性、熔沸点、硬度、特性等。本题中根据焰色反应可以鉴别氯化钠和氯化铵,根据溶解性鉴别氮气和二氧化碳,根据溶液颜色鉴别氯化铁溶液(黄色)和氯化亚铁溶液(浅绿色)。
(3)物质的鉴别根据化学性质鉴别:酸碱性、氧化还原性、络合性、热稳定性、饱和性和不饱和性等。
①.酸碱性:可以鉴别氯化钠和氯化铵、硫酸钠和碳酸钠。
方法:将固体溶于水,用pH 试纸检验,pH=7的溶液是氯化钠溶液和硫酸钠溶液,pH<7的是氯化铵溶液,pH>7的是碳酸钠溶液。
说明:强酸强碱盐不水解溶液呈中性,强酸弱碱盐水解溶液呈酸性,例如:氯化铵(pH<7);强碱弱酸盐水解溶液呈碱性,例如:碳酸钠(pH>7)。
②.加酸可以鉴别硫酸钠和碳酸钠。
方法:在固体中加入盐酸,有气泡产生的是碳酸钠。
③.加碱可以鉴别的是氯化钠和氯化铵、氮气和二氧化碳、氯化铁和氯化亚铁。
方法:在固体中加入强碱混合研磨,有刺激性气味产生是氯化铵;将气体通入澄清石灰水,石灰水变浑浊的是二氧化碳气体;将固体溶于水再加入碱溶液,产生白色沉淀变成灰绿色最终变成红褐色的是氯化亚铁溶液,直接产生红褐色沉淀的是氯化铁溶液。
④.氧化还原性:鉴别氯化铁和氯化亚铁
ⅰ、能溶解铜粉的是氯化铁溶液:2FeCl3+Cu=2FeCl2+CuCl2
ⅱ、能使润湿的碘化钾淀粉试纸变蓝色的是氯化铁溶液:2FeCl3+2KI=2FeCl2+I2+2KCl ,碘遇淀粉变蓝色。
⑤.络合性:鉴别氯化铁和氯化亚铁。
方法:将固体溶于水,加入硫氰化钾溶液,溶液呈红色的是鉴别氯化铁溶液。
⑥.热稳定性:鉴别氯化钠和氯化铵。
方法:将固体置于试管中加热,固体质量不变的是氯化纳,质量减少以至消失的是氯化铵。
⑦.饱和性和不饱和性:鉴别乙烯和乙烷
方法1:加成反应鉴别法:使溴水(黄色或橙色)褪色的是乙烯。
方法2:氧化反应鉴别法:使酸性高锰酸钾溶液(紫色)褪色的是乙烯。
10.(1956年全国高考题第4题).(15分)加一种什么试剂并根据什么现象,来鉴别下列各对物质(不要求写反应式)
(1)氯化钠和氯化铵;(2)氮气和二氧化碳;(3)硫酸钠和碳酸钠;(4)氯化铁和氯化亚铁;(5)乙烯和乙烷
9.[评分标准]盐酸溶液以石蕊试纸试之呈红色(2分),加入氯化钡溶液无反应(2分);硫酸钠溶液以石蕊试纸试之不变色(2分),加入氯化钡溶液生成白色沉淀(2分);硫酸溶液以石蕊试纸试之呈红色(2分),加入氯化钡溶液生成白色沉淀(2分).(如果只答沉淀,没有说出白色或说错颜色,仅给1分)。
[相应知识点归纳]
(1)遇到紫色石蕊变红的酸性溶液分类:酸(盐酸、稀硫酸)、酸式盐(硫酸氢钠)溶液、强酸弱碱盐溶液。
(2)遇到紫色石蕊变蓝的碱性溶液分类:可溶性碱溶液、强碱弱酸盐(碳酸钠)溶液。
(3)遇到紫色石蕊不变色的中性盐溶液分类:强酸强碱盐溶液(氯化钠)和弱酸弱碱盐溶液(醋酸铵)盐。
(4)与氯化钡溶液中的Ba2+产生沉淀的物质分类:硫酸和硫酸盐、可溶性碳酸盐、可溶性硅酸盐、可溶性磷酸盐、可溶性亚硫酸盐。
(5)与氯化钡溶液中的Cl- 产生沉淀的物质分类:硝酸银溶液和硝酸亚汞溶液。
※某溶液中加入BaCl2溶液产生白色沉淀,再加入硝酸,沉淀不溶,说明原溶液中一定含有SO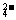 (×)。
(×)。
※某溶液中加入BaCl2溶液产生白色沉淀,再加入硝酸,沉淀不溶,说明原溶液中可能含有SO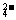 或Ag+(√)。
或Ag+(√)。
9.(1955年全国高考第3题)(12分)今有盐酸、硫酸钠和硫酸三种水溶液.问石蕊试纸及氯化钡溶液对它们各产生什么现象?
8.[答案]结构式略,名称依次为:1-丙醇,2-丙醇,甲基乙基醚。
[解析] 符合C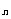 H
H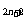 O的含氧衍生物,同分异构体分为醚类和醇类两种类别异构,醇类又分为官能团(羟基)的位置异构,本题中碳原子个数只有3个,没有碳干异构;本题分为醚类异构体:甲基乙基醚和醇类异构体:1-丙醇,2-丙醇。
O的含氧衍生物,同分异构体分为醚类和醇类两种类别异构,醇类又分为官能团(羟基)的位置异构,本题中碳原子个数只有3个,没有碳干异构;本题分为醚类异构体:甲基乙基醚和醇类异构体:1-丙醇,2-丙醇。
[相应知识点归纳]
(1)同分异构体分为类别异构、官能团位置异构和碳干异构、平面异构。
(2)常见的类别异构有:①烯烃和环烷烃;②炔烃和二烯烃;③醇和醚;④醛和酮;⑤羧酸、酯、羟基醛、羟基酮;⑥葡萄糖和果糖;⑦麦芽糖和蔗糖;⑧氨基酸和硝基烷。
8.(1954年全国高考试题第5题)(15分)今有三种有机化合物,它们的分子式都是C3H8O,试写出它们的结构式和化学名称来。
7.[评分标准]1.混合物(2分);理由:①成份不固定,②氧氮不化合,③溶于水的空气的氧氮比例与空气中不同,
④液化空气蒸发时,氮先出(任答其二,各给4分)。
[相应知识点归纳] ①空气的主要成分是氮气和氧气,还含有少量的二氧化碳、水蒸气以及稀有气体等,并随各地空气污染指数不同含有不同的大气污染物。②混合物是由不同物质组成的,没有固定的熔沸点;化合物是纯净物,有固定不变的组成,有固定的熔沸点。③分离液态空气时沸点低的氮气先出来,氧气后出来;说明空气的沸点不同是混合物,同时也说明空气是由多种物质组成的是混合物。
7.(1953年全国高考试题第1题)(10分)空气是混合物,还是化合物?用两个理由说明.
6.[答案]E。
[解析] 根据溶解性将硫化物分为可溶性硫化物和不溶性硫化物;绝大多数硫化物不溶于水,只有K2S 、Na2S 、(NH4)2S溶于水。
[相应知识点归纳]
酸碱盐溶解性口诀:
①.钾钠钡铵碱都溶,含义:可溶性碱有:KOH、NaOH、Ba(OH)2、NH3 ·H2O都溶于水,澄清石灰水溶。
②.硝酸盐类也相同,含义:硝酸盐都溶于水,象可溶性碱一样溶于水。
③.氯化银汞要沉淀,含义:AgCl 、Hg2Cl2不溶于水。
④.硫酸钡铅还不溶,含义:BaSO4 、PbSO4也不溶于水。
⑤.碳磷硅酸亚硫酸,钾钠铵盐溶水中,含义:碳酸盐、磷酸盐、硅酸盐、亚硫酸盐中只溶解对应的钾盐、钠盐、铵盐。
⑥.硫化钡镁钾钠铵,定要溶解要记全,含义:硫化物质溶解BaS 、MgS 、K2S 、Na2S 、(NH4)2S。
6.(1952年全国高考题第7题)哪一种硫化物能溶于水? ( )
(A)FeS (B)PbS (C)CuS (D)ZnS (E)Na2S
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com