
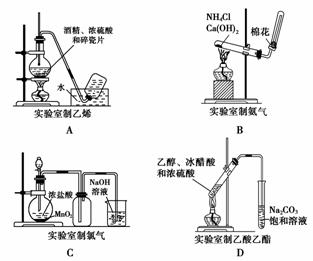
4.(2008年重庆卷)下列实验装置图正确的是( )
3.实验室里可按如下图所示的装置来干燥、收集气体R,多余的气体R可用水吸收,则( )
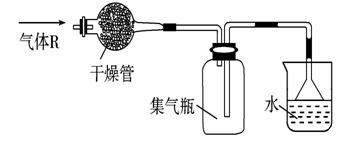
A.HCl
B.Cl2
C.CO
D.NH3
2.为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置应分别装入 ( )
A.饱和Na2CO3溶液;无水CaCl2
B.饱和NaHCO3溶液;浓H2SO4
C.浓H2SO4;饱和NaHCO3溶液
D.饱和NaHCO3溶液;稀H2SO4
1.(2009年长春模拟)下列关于实验室制取气体所用试剂的组合中不合理的是 ( )A.制Cl2:MnO2、HCl(浓)
B.制NH3:浓氨水、生石灰
C.制NO:HNO3(稀)、Cu
D.制CO2:H2SO4(稀)、大理石
14.(16分)各方监测数据显示:无锡市区域内的太湖水位出现50年
以来的最低水位,加上天气连续高温少雨,太湖水突然变质,且富营养化较重,诸
多因素导致蓝藻爆发,影响了自来水水源的水质.
六价铬对人体有毒,含铬废水要经过化学处理后才能排放.
工业上为处理含有Cr2O的酸性废水采用如下方法:在工业废水中加入适量
NaCl,然后以铁为电极电解,鼓入空气,最后将Cr2O以Cr(OH)3形式沉淀下来
而除去,且还生成Fe(OH)3沉淀,这种处理方法可使工业废水中的Cr2O含量达
到国家规定的排放标准.试回答:
(1)在工业废水中加入NaCl的作用是____________________________________.
(2)有关电极反应方程式是_____________________________________________.
(3)由Cr2O转化为Cr3+的离子方程式是__________________________________
____________________________________________________________________.
(4)电解过程中工业废水由酸性变碱性的原因是
___________________________________________________________________
___________________________________________________________________.
(5)另一种处理含铬废水的方法是用绿矾[FeSO4·7H2O]把废水中的六价铬还原成铬
离子,再加入过量石灰水,使铬离子转为氢氧化铬[Cr(OH)3]沉淀,其主要化学反
应的化学方程式如下:
H2Cr2O7+6FeSO4===3Fe2(SO4)3+Cr2(SO4)3+2H2O
现用上法处理1×104 L 含铬(+6价)78 mg/L的废水(Cr的相对原子质量为52),试
回答:
①处理后沉淀除Cr(OH)3外,还有________(填化学式来表示).
②需用绿矾________.
解析:Cr2O有强氧化性,电解Fe能产生Fe2+,发生氧化还原反应,达到除去
Cr2O的目的,同时还考查到水的电离平衡的问题.
答案:(1)增强废水的导电能力
(2)阳极:Fe-2e-===Fe2+
2H++2e-===H2↑
(3)Cr2O+6Fe2++14H+===2Cr3++7H2O+6Fe3+
(4)电解过程中,由于H+放电,因而破坏了水的电离平衡,导致溶液中c(OH-)>
c(H+),因而废水由酸性变为碱性.
(5)①Fe(OH)3和CaSO4·2H2O ②12.51 kg
13.(11分)汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源.治理的
方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它
的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃
类(C、H化合物)充分燃烧及SO2的转化.
(1)写出CO与NO反应的化学方程式_______________________________________
______________________________________________________________________.
(2)“催化转换器”的缺点是在一定程度上提高空气的酸度,其原因是
_____________________________________________________________________.
(3)控制城市空气污染源的方法可以有________.
A.开发氢能源 B.使用电动车
C.植树造林 D.戴上呼吸面具
解析:(1)CO、NO在催化剂的作用下转化为参与大气生态环境循环的无毒气体,
由此可得出,反应的产物是CO2和N2,反应的化学方程式为2CO+2NO N2
+2CO2.
(2)“催化转换器”促使SO2转化,由题给信息:能提高空气酸度,可判断SO2转化
成了SO3,即2SO2+O2 2SO3,SO3的形成,在一定程度上提高了空气的
2SO3,SO3的形成,在一定程度上提高了空气的
酸度.
(3)控制城市空气污染源的根本方法是开发无污染的氢能源和使用电动车等.
答案:(1)2CO+2NO N2+2CO2
(2)2SO2+O2
 2SO3,增加了SO3酸性气体
2SO3,增加了SO3酸性气体
(3)AB

12.(11分)当都市里的人们陶醉在繁华的城市生活中时,是否意识到有一支“大军”正
向我们逼近,影响我们的生活,危害我们的健康.
(1)在意大利,人们家里的咖啡壶大多是用回收的可乐罐制得.请再列举一种生活
垃圾回收利用的事例:
____________________________________________________________________
_____________________________________________________________________.
(2)回收利用垃圾,首先要对垃圾进行分类.一群环保志愿者在某社区推广垃圾分
类,他们在垃圾房放置了一些有分类标志的垃圾回收箱,结果却发现仍然有许多
居民并没有分类放置.造成这种现象可以排除的原因是 ( )
A.居民嫌麻烦,没有垃圾分类的习惯
B.居民每天产生的生活垃圾量多
C.居民的环保意识不强
D.居民不清楚垃圾分类的标准
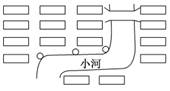
(3)上图是某居民小区中垃圾收集点(小圆圈)的布局,它在选址上存在的问题有
____________________________________________________________________.
垃圾收集点选址应考虑的因素包括
___________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________.
解析:(1)生活中使用过的废旧的纸制品、塑料制品、玻璃制品等,都属于生活垃
圾.
(2)注意这里要求判断“可以排除的原因”.
答案:(1)废塑料制取燃料油(或废纸、废塑料制造复合板;废玻璃瓶制造玻璃丝)
(2)B
(3)垃圾收集点分布不均匀;垃圾收集点沿河设置,污染水源 是否便于居民投放垃
圾;是否影响居民的生活;是否影响居民区的景观;是否造成再次污染;是否有利
于垃圾的运输
10.下列行为与加强能源资源节约和生态环境保护,增强可持续发展能力不相符的是( )
A.大量使用化学肥料,提高农作物的产量和质量
B.将农作物秸秆通过化学反应转化为乙醇用作汽车燃料
C.使用资源节约型、环境友好型的生物降解塑料包装
D.推广煤炭脱硫技术、减少直接燃煤,防止酸雨发生
解析:A项中大量使用化学肥料,会使地下水污染;B项中秸秆(纤维素)葡萄糖―→乙醇,方法可行;C项为防止“白色污染”,2008年6月1日我国“限塑令”建议使用可降解塑料;D项属于“钙基固硫”,往煤中加入少量生石灰,其反应为S+O2 SO2,CaO+SO2===CaSO3,2CaSO3+O2=== 2CaSO4,可以减少SO2排放,防止酸雨发生.
答案:A
9.下列有关环境问题的说法正确的是 ( )
A.燃烧煤时加入适量石灰石,可减少废气中SO2的量
B.臭氧的体积分数超过10-4%的空气有利于人体健康
C.pH在5.6-7.0之间的降水通常称为酸雨
D.含磷的合成洗涤剂易于被细菌分解,故不会导致水体污染
解析:A项,因发生反应CaCO3 CaO+CO2↑,CaO+SO2=== CaSO3,2CaSO3+O2===2CaSO4,可减少SO2的排放量;B项,臭氧浓度大时损害人体健康;C项,pH小于5.6的降水称为酸雨;D项,会导致水体富营养化.
答案:A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com