
(二)非选择题
13.美籍埃及人泽维尔用激光闪烁照相机拍摄到化学反应中化学键断裂和形成的过程,因而 获得1999年诺贝尔化学奖。激光有很多用途,例如波长为10.3微米的红外激光能切断B(CH3)3分子中的一个B-C键,使之与HBr发生取代反应:
B(CH3)3+HBr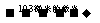 B(CH3)2Br+CH4
B(CH3)2Br+CH4
而利用9.6微米的红外激光却能切断两个B-C键,并与HBr发生二元取代反应。
(1)试写出二元取代的化学方程式: 。
(2)现用5.6gB(CH3)3和9.72gHBr正好完全反应,则生成物中除了甲烷外,其他两种产物的物质的量之比为多少?
14.A、B都是芳香族化合物,1molA水解得到1molB和1mol醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。且B分子中碳和氢元素总的质量分数为65.2%。A溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B的相对分子质量之差为 。
(2)1个B分子中应该有 个氧原子。
(3)A的分子式是 。
(4)B可能的三种结构简式是 。
15.有机物E和F可用作塑料增塑剂或涂料中的溶剂。它们的分子量相等,可用以下方法合成
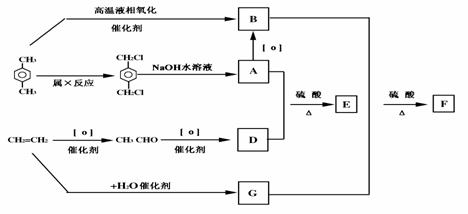
请写出:有机物的名称A 、B 化学方程式:
A+D E
E
B+G F
F
X反应的类型及条件:类型 条件
E和F的相互关系属 (多选扣分)
①同系物 ②同分异构体 ③同一种物质 ④同一类物质
16.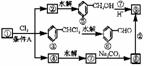 通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:
通常情况下,多个羟基连在同一个碳原子上的分子结构是不稳定的,容易自动失水,生成碳氧双键的结构:
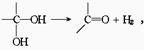
右图是9个化合物的转变关系。
(1)化合物①是 ,它跟氯气发生反应的条件是 。
(2)化合物⑤跟⑦可在酸的催化下去水生成化合物⑨,⑨的结构简式是 ,名称是 。
(3)化合物⑨是重要的定香剂,香料工业上常用化合物②和⑧直接合成它。此反应的化学方 程式是 。
(一)选择题
1.现有一系列稠环芳香烃,按如下特点排列:
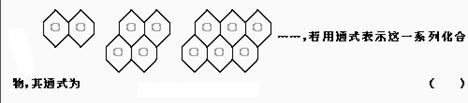
A.CnH2n-6? B.C4n-6H2n+6
C.C2n+4H6n+6? D.C6n+4H2n+6
2.分别燃烧下列各组物质中的两种化合物,所得CO2和H2O的物质的量之比相同的有( )
A.乙烯、丁二烯 B.乙醇、乙醚
C.苯和苯酚 D.醋酸、葡萄糖
3.下列有机物各1 mol,完全燃烧需氧气最多的是( )
A.C3H6 B.C3H8O
C.C3H6O2 D.C4H8O2
4.对于结构简式为:
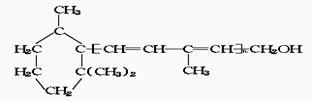
的维生素A,有如下各种说法:①维生素A是一种醇,②1摩维生素A在催化剂作用下,可与5 摩H2加成,③维生素A的分子中有苯环结构,④维生素A具有环己烷的结构,⑤维生素A的分子 式为C20H30O,⑥维生素A有异戊二烯的结构单元。上述各说法中正确的是
A.①③④⑤ B.②④⑤⑥ C.①②③④ D.①②⑤⑥
5.在灼热铜丝网的作用下,1-丙醇跟空气中氧气反应生成一种化合物。与该化合物互为同分异构体的有( )


其中一氯取代物的同分异构体数目相同的是( )
 A.①和④ B.②和③ C.①和③ D.②和④
A.①和④ B.②和③ C.①和③ D.②和④
7.白黎芦醇 广泛存在于食物(例如桑椹、花生、尤其是葡萄酒)中,它可能具有抗癌性。能够使1 mol该化合物起反应的Br2和H2的最大用量分别为( )
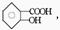 A.1mol,1mol
B.3.5mol,7mol
C.3.5mol,6mol D.6mol,7mol
A.1mol,1mol
B.3.5mol,7mol
C.3.5mol,6mol D.6mol,7mol
8.邻羟基苯甲酸,俗名水杨酸,其结构简式为 当与物质A的溶液反应生成化学式为C7H5O3Na的盐,A可以是下列中的( )
A.NaCl B.Na2SO4 C.NaOH D.NaHCO3
9.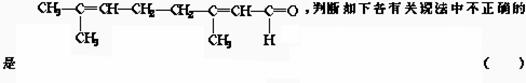 根据柠醛的结构简式为
根据柠醛的结构简式为
A.它可以使KMnO4酸性溶液褪色。
B.它可以使溴水褪色
C.它可以与银氨溶液发生银镜反应
D.它的催化加氢反应产物的分子式为C10H20O
10.下列各组物质,只用一种试剂就可鉴别的是( )
A.CH4、CH2 CH2、CH
CH2、CH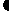 CH、CH2
CH、CH2 CH-CH
CH-CH CH2
CH2
B.CH3OH、HCOOH、CH3CHO、CH3COOH
C.HCOOCH3、CH3CHO、C6H5OH、C2H5OH
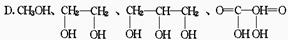
11.若1摩气态烃能跟2摩HCl加成,而加成产物又可以和6摩Cl2完全取代,则该烃是 ( )
A.2-甲基丙烯 B.乙炔 C.1,3-丁二烯 D.丙炔
12.歪状化合物COOCH2 是一种重要的有机试剂,它可由有机化工原料R和其它无机原料
 COOCH2
COOCH2
发生加成、水解、氧化、酯化反应制 得,R是( )
A.1-丁烯 B.乙炔 C.1,3-丁二烯 D.乙烯
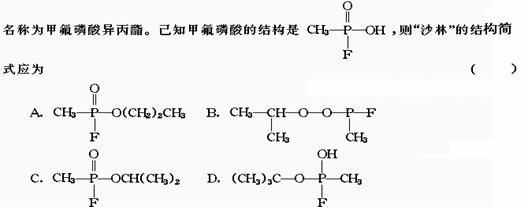
13.1995年3月20日在日本东京地铁发生了震惊世界的“沙林毒气袭击事件”,造成11人死亡,5500多人中毒,恐怖分子使用的“沙林”是剧毒的神经毒剂,它的化学
(五)正确利用新信息迁移题,培养分析问题,解决问题的能力。
新信息迁移题,其特点是在题中联系社会实践和科学发展给予一定量的新的问题情境或有关信息,结合教材中所学知识而构成的一类新题型。在解题过程中,可体会到一些科学、社会的发展与化学学科间的重要性质,接触并学习一些新知识,从而提高自身的科学素养和文化素质,同时达到培养自学能力、信息接受和处理能力、问题的分析和解决能力。
在解新信息迁移题时,首先是全面地、认真地分析题中给予的信息内容、要点和规律,然后迁移到教材中有关的知识内容上,解决题中要求的问题。
(四)定量认识有机物之间的相互反应。
在学习有机物的化学性质、制备和检验时,都要涉及有关的反应,对待反应的化学方程式, 除了明确反应物,生成物的组成和结构以及反应条件等定性内容之外,还必须同时明确各 物质之间的定量关系,不断强化理解学习的定量意识,现通过一些具体反应,举例说明如下:
(1)在烷烃和芳香烃与卤素(X2)的一卤取代反应中,被取代的H原子和卤素单质及生成的卤代烃物质的量之比为1∶1∶1。
 (2)在不饱和烃与氢气或卤素的加成反应中, C C双键与氢气或卤素单质的量之比都是1∶1,若是C
(2)在不饱和烃与氢气或卤素的加成反应中, C C双键与氢气或卤素单质的量之比都是1∶1,若是C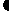 C叁键,则为1∶2
C叁键,则为1∶2
(3)当醇与金属钠反应时,醇羟基和反应消耗的Na及生成氢气物质的量之比为2∶2∶1。若醇羟基换成酚羟基或羰基,与金属钠反应时,也有同样的量关系。
 (4)当醇被氧化成醛或酮时,反应中被氧化的醇羟基和消耗的O2与生成C O双键、H2O物质的量之比为2∶1;2∶2;若将氧化剂O2换成CuO,上述量关系 为1∶1∶1∶1。
(4)当醇被氧化成醛或酮时,反应中被氧化的醇羟基和消耗的O2与生成C O双键、H2O物质的量之比为2∶1;2∶2;若将氧化剂O2换成CuO,上述量关系 为1∶1∶1∶1。
(5)在银镜反应中,醛基和消耗的[Ag(NH3)2]+与生成的羟基,析出Ag物质的量之比为1∶2∶1∶2。
在醛和新制的Cu(OH)2悬浊液反应时,醛基、Cu(OH)2和生成的羰基、Cu2O物质的量之比为1∶2∶2∶1。
(6)在有机物(CxHyOz)完全燃烧的反应中,有机物和消耗的氧气、与生成的CO2、H2O物质的量之比为:
1∶(X+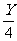 -
-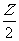 )∶X∶
)∶X∶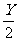 。
。
(三)重视各类物质性质的比较和分析,培养综合归纳的能力。
在有机化学的学习过程中,分别对各类有机物的主要性质,尤其是化学性质,有了比较系统的掌握之后,应注意,各类物质性质的横向比较,认识不同类的相关有机物在性质上的异同 。这本身也是对各种有机物性质的分析和归纳,见前面知识结构内容。
(二)通过分析、比较、综合、归纳掌握同分异构现象及其有关的知识内容。
在有机物中,经常出现由于分子中各原子的可能排列顺序和方式的变化,形成分子式虽然相同,但结构不同的化合物,而出现同分异构现象,这些具有同分异构现象的化合物互称为同分异构体。这就是有机物种类繁多的原因所在。同分异构体的概念中,有两个突出的要点:一是同分异构体间的共性,即“分子式相同”或是“分子组成相同”;另一是同分异构体间的差异,即“结构不同”且两个要点必须同时具备。现将一些存在“相同”和“相异”的概念比较如下:
|
|
相同点 |
不同点 |
|
同分异构体 |
分子式 |
结构 |
|
同系物 |
性质相似 |
分子组成中相差1个或n个CH2基因 |
|
同位素 |
质子数 |
中子数 |
|
同素异形体 |
同种元素 |
不同单质 |
将同分异构体和同系物两概念相比较时,同分异构体概念中强调“分子式相同”,所以分子量必相等,而同系物强调“分子组成上相差一个或几个CH2原子团,所以分子量必不等。因此,在互为同分异构体的各物质中,不可能存在互为同系物的物质,在互为同系物的各物质中,也不可能存在同分异构现象。
根据分子组成判断各同分异构体的结构和总数,是有机化学学习的重点内容之一。同分异构现象可分为3类:
(1)碳链异构(或称碳骨架异构):如乙苯和二甲苯,丁酸和异丁酸。
(2)相同官能团的位置异构:如1-丁烯和2-丁烯。
(3)官能团的种类异构:如丙醛和丙酮,乙醇和甲醚。
官能团的异构列表如下:
|
官能团异构类型 |
分子组成通式 |
|
烯烃-环烷烃 |
CnH2n |
|
炔烃-二烯烃 |
CnH2n+2O |
|
醇类-醚类 |
CnH2n-6O |
|
酚类-芳香醇-芳香醚 |
CnH2n-6O |
|
醛类-酮类-烯醇类-环氧烷-环烷醇 |
CnH2nO |
|
羰酸-酯类-羟基醛 |
CnH2nO2 |
|
硝基化合物-氨基酸 |
CnH2n+1NO2 |
(一)根据结构掌握和运用各类有机化合物的分子组成通式。
学习有机化学的关键是认识有机化合物的结构,根据内在的物质结构去掌握有关的各种表象 和问题。在掌握和运用各类有机物的分子组成通式时,也是如此。
分子中碳原子个数为n的链状烷烃的结构和其中碳、氢原子个数可表示如下:

由此确定烷烃的分子组成通式为CnH2n+2。而且当分子中碳原子个数为n个,其中氢原子个数的最大数为2n+2,是氢原子个数上限值。除了链状烷烃之外的各类有机物分子组成通式中,氢原子的个数都不大于此数值。若给出的有机物分子中,氢原子和碳原子的个数比大于
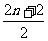 时,此分子组成肯定不正确。
时,此分子组成肯定不正确。

 以链状烷烃分子结构和分子组成通式(CnH2n+2)为基础进行分析和比较:在结构中 , 若增加一个双键,就要少2个氢原子;若增加一个C
以链状烷烃分子结构和分子组成通式(CnH2n+2)为基础进行分析和比较:在结构中 , 若增加一个双键,就要少2个氢原子;若增加一个C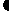 C叁键,要少4个氢原子,在结构中出现一个环状结构,也要少2个氢原子 。所以,烯烃和环烷烃的分子组成通式为CnH2n,炔烃和二烯烃的分子组成通式为CnH2n-2。苯和苯的同系物结构中有苯环结构,苯的结构用凯库勒式表示为,可看成是具有3个C
C双键和1个环 状结构,分子中碳原子个数为n时,氢原子个数应是在2n+1的基础上减去2×4,得到苯和苯
的同系物分子组成通式为CnH2n-6(n≥6),其他各类烃的分子组成通式,也可用同 样的方法进行确定。
C叁键,要少4个氢原子,在结构中出现一个环状结构,也要少2个氢原子 。所以,烯烃和环烷烃的分子组成通式为CnH2n,炔烃和二烯烃的分子组成通式为CnH2n-2。苯和苯的同系物结构中有苯环结构,苯的结构用凯库勒式表示为,可看成是具有3个C
C双键和1个环 状结构,分子中碳原子个数为n时,氢原子个数应是在2n+1的基础上减去2×4,得到苯和苯
的同系物分子组成通式为CnH2n-6(n≥6),其他各类烃的分子组成通式,也可用同 样的方法进行确定。
烃的衍生物中,卤代烃是饱和链烃基和卤素相结合,根据卤代烃的结构,分子组成通式为



 CnH2n+2-mxm,若其中的烃基不是烷烃基时,氢原子个数在此基础上, 按前面所述根据不饱和键和环状结构的数量而减少,烃的含氧衍生物中,分子中碳原子个数
为n个,每出现1个C O时,也同样减少2个氢原子,单纯氧原子的
个数多少,并不影响氢原子的个数,比如,1个碳原子与氢原子相连,或是与1个羟基相连,
氢原子个数都是1。因此,在醇的分子组成通式中,饱和一元醇和醚是CnH2n+2O多
元醇就是CnH2n+2Om,苯酚及其同系物、芳香醇是CnH2n-6O,醛酮的分子结构中存在C O键,分子组成通式为CnH2nO,羰酸或酯就是CnH2nO2。若醛、酮、羰酸和酯的分子结构中烃基也出现碳碳不饱和键和环状结构时,仍要在原烃的衍生物分子组成通式中,相应减少一定个数的氢原子。如某醛分子式为C3H6O,符合通式CnH2nO,可确定为丙醛,分子组成为C3H4O,与C3H6O相比较少2个氢原子,可知C3H4O为丙烯醛,若将结构中的C O键换成C C双键时,分子式为C3H6O的有机物还可 以是丙烯醇,从而可进一步确定:具有相同碳原子个数的醛、酮和烯醇互为同分异构体。
CnH2n+2-mxm,若其中的烃基不是烷烃基时,氢原子个数在此基础上, 按前面所述根据不饱和键和环状结构的数量而减少,烃的含氧衍生物中,分子中碳原子个数
为n个,每出现1个C O时,也同样减少2个氢原子,单纯氧原子的
个数多少,并不影响氢原子的个数,比如,1个碳原子与氢原子相连,或是与1个羟基相连,
氢原子个数都是1。因此,在醇的分子组成通式中,饱和一元醇和醚是CnH2n+2O多
元醇就是CnH2n+2Om,苯酚及其同系物、芳香醇是CnH2n-6O,醛酮的分子结构中存在C O键,分子组成通式为CnH2nO,羰酸或酯就是CnH2nO2。若醛、酮、羰酸和酯的分子结构中烃基也出现碳碳不饱和键和环状结构时,仍要在原烃的衍生物分子组成通式中,相应减少一定个数的氢原子。如某醛分子式为C3H6O,符合通式CnH2nO,可确定为丙醛,分子组成为C3H4O,与C3H6O相比较少2个氢原子,可知C3H4O为丙烯醛,若将结构中的C O键换成C C双键时,分子式为C3H6O的有机物还可 以是丙烯醇,从而可进一步确定:具有相同碳原子个数的醛、酮和烯醇互为同分异构体。
从上面的叙述和分析过程中,认识到:“分子结构是学好有机化学的关键”,对于“各类有 机物的分子组成通式的掌握不应靠单纯的记忆,也不宜完全依赖数学中的单一数字推导,如 苯的同系物看成由苯基和烷基结合而成,苯基为C6H5;烷基设为CmH2m+1,两 者结合后化学式为Cm+6H2m+6,即Cm+6H2(m+6)-6,设m+6=n时, 才最终得到苯和苯的同系物分子组成通式为CnH2n-6,这一推导过程明显过于呆滞 ,不利于对各类有机物分子组成通式的掌握,也不便于应用。
6.酯化反应与中和反应的比较
|
|
酯化反应 |
中和反应 |
|
反应的过程 |
酸脱-OH醇去-H结合生成水 |
酸中H+与碱中OH-结合生成水 |
|
反应的实质 |
分子间反应 |
离子反应 |
|
反应的速率 |
缓慢 |
迅速 |
|
反应的程序 |
可逆反应 |
可进行彻底的反应 |
|
是否需要催化剂 |
需浓硫酸催化 |
不需要催化剂 |
5.烃的羰基衍生物性质比较
|
物质 |
结构简式 |
羰基稳定性 |
与H2加成 |
其它性质 |
|
乙醛 |
CH3CHO |
不稳定 |
容易 |
醛基中C-H键易被氧化(成酸) |
|
乙酸 |
CH3COOH |
稳定 |
不易 |
羧基中C-O键易断裂(酯化) |
|
乙酸乙酯 |
CH3COOCH2CH3 |
稳定 |
不易 |
酯链中C-O键易断裂(水解) |
4.烃的羟基衍生物性质比较
|
物质 |
结构简式 |
羟基中氢原子活泼性 |
酸性 |
与钠反应 |
与NaOH的反应 |
与Na2CO3的反应 |
|
乙醇 苯酚 乙酸 |
CH3CH2OH C6H5OH CH3COOH |
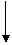 增 增强 |
中性 |
能 |
不能 |
不能 |
|
与H2CO3弱 |
能 |
能 |
能 |
|||
|
强于H2CO3 |
能 |
能 |
能 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com