
21. (6分) 在实验室中做小型实验:把物质A、B按一定比例充入一个表面积为300 cm2、容积为2 L的球形容器,使压强为p,然后将整个容器用加热器加热到280℃时,发生如下反应:
3A(g)+3B(g)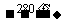 2C(g)+2D(g);ΔH=-180 kJ·mol-1
2C(g)+2D(g);ΔH=-180 kJ·mol-1
(1)若平均每分钟生成0.5 mol C,则此反应速率可表示为v(C)=________。
(2)若容器表面向外散热速率平衡为400 J·(min·cm2)-1,为了维持恒温280℃,平均每分钟需用加热器提供________kJ的热量。
(3)若将小型实验扩大为工业生产:将反应容器的容积扩大到原来的10倍,做成“相似体”,且将A、B按原比例向其中充入,并使压强仍为p,然后加热到280℃,则达到平衡时,C的体积分数与实验室的小型实验相比,将________(填“减小”“增大”或“不变”)。
20. (6分) 如下图所示,向A中充入1 mol X和1 mol Y,向B中充入2 mol X和2 mol Y,起始时,VA=VB=a L。在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:
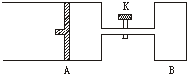
X+Y 2Z+W ΔH<0(X、Y、Z、W均为气体),达到平衡时,VA=1.2a L。
2Z+W ΔH<0(X、Y、Z、W均为气体),达到平衡时,VA=1.2a L。
试回答:
(1)A中X的转化率aA=________;
(2)A、B中X转化率的关系:aA_________aB(填“>”“=”或“<”);
(3)打开K,一段时间后又达平衡时,A的体积为________L(连通管中气体体积不计);
19、(5分)(07高考海南卷)PCl5的热分解反应如下:PCl5(g) 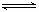 PCl3(g) + Cl2(g)。
PCl3(g) + Cl2(g)。
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150mol/L。计算该温度下的平衡常数。
18、(12分)影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过图1所示装置研究反应速率的有关问题。
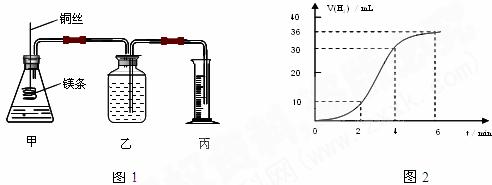 (1)(4分)取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内足量的稀盐酸中。足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图2所示。写出该反应的离子方程式___________________________________________,在前4min内,镁条与盐酸的反应速率逐渐加快,在4min之后,反应速率逐渐减慢,请简述其原因:____________________________________________ 。
(1)(4分)取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内足量的稀盐酸中。足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图2所示。写出该反应的离子方程式___________________________________________,在前4min内,镁条与盐酸的反应速率逐渐加快,在4min之后,反应速率逐渐减慢,请简述其原因:____________________________________________ 。
(2)某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
①(4分)该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没有影响;
原因Ⅱ:_______________________________________________________;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻碍作用;
原因Ⅳ:Cl-、SO42-均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:________________________________________________________。
②(4分)该同学设计并进行了两组实验,即得出了正确结论。他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体 ,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
若观察到实验a中____________,实验b中 ,则说明原因Ⅲ是正确的。依次类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用。
17、(12分)现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_______p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率_________
(4)若升高温度,则平衡时B、C的浓度之比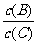 将______ ___。
将______ ___。
(5)若加入催化剂,平衡时气体混合物的总物质的量____ _____。
16、(4分)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为__________________。又已知:H2O(g)=H2O(l);△H2=-44.0kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_____________kJ。
15、已知在450℃时,反应 H2(g)+I2(g) 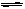 2HI(g)的化学平衡常数为50,由此推断出在450℃时,反应 2HI(g)
2HI(g)的化学平衡常数为50,由此推断出在450℃时,反应 2HI(g)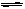 H2(g)+I2(g)的化学平衡常数为 ( )
H2(g)+I2(g)的化学平衡常数为 ( )
A、50 B、0.02 C、100 D、无法确定
14、下列对于反应C(s) + H2O(g) 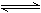 CO(g)
+ H2(g)的描述正确的是:( )
CO(g)
+ H2(g)的描述正确的是:( )
A. 达平衡时,各反应物和生成物浓度相同
B. 增大压强,对此反应速率无影响
C. 达平衡时,c(H2O):c(CO)=1:1
D.达平衡时,H2O转化为CO的速率等于CO转化为水的速率
13、在密闭容器中于一定条件下进行下列反应:2SO2 + O2 2SO3当到达平衡时通入18O2,再次平衡时,18O存在于( )
2SO3当到达平衡时通入18O2,再次平衡时,18O存在于( )
A、SO2 、O2 B、SO2 、SO3 C、SO2 、O2 、SO3 D、O2 、SO3
12、对某一可逆反应来说,使用催化剂的作用是 ( )
A. 提高反应物的平衡转化率 B. 以同样程度改变正逆反应速度
C. 增大正反应速率,降低逆反应速率 D. 改变平衡混合物的组成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com