
7.已知椭圆方程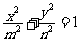 ,若在1,2,3,4,5,6这六个数字中任取两个作为
,若在1,2,3,4,5,6这六个数字中任取两个作为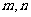 的值,则不同的椭圆个数为( )
的值,则不同的椭圆个数为( )
A.12 B.15 C.30 D.60
6. 已知点M是棱长为1的正方体
已知点M是棱长为1的正方体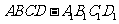 棱
棱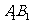 的中点,则点M到平面
的中点,则点M到平面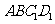 的距离是( )
的距离是( )
A.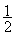 B.
B.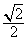 C.
C. D.
D.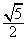
5.函数 ,若
,若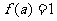 ,则
,则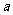 的所有可能值为( )
的所有可能值为( )
A.4 B.1或–1 C.–1或4 D.1,–1或4
4.已知双曲线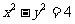 的右焦点为F,则点F到其中一条渐近线的距离为(
)
的右焦点为F,则点F到其中一条渐近线的距离为(
)
A.1
B.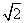 C.
C.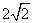 D. 2
D. 2
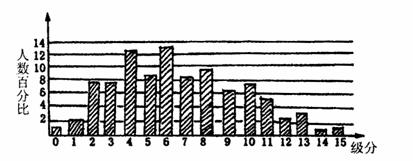
3.九二年度大学学科能力测验有12万名学生,各学科成绩采用15级分,数学学科能力测验成绩分布图如下图:请问有多少考生的数学成绩分高于11级分?选出最接近的数目( )
A.4000人 B.10000人 C.15000人 D.20000人
2.复数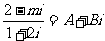 (m、A、B∈R),且A+B=0,则m的值是 ( )
(m、A、B∈R),且A+B=0,则m的值是 ( )
A.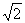 B.
B. C.-
C.- D.2
D.2
1.集合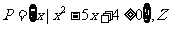 为整数集,则
为整数集,则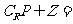 ( )
( )
A.{2,3} B.{1,2,3} C.{2,3,4} D.{1,2,3,4}
3.下列是某兴趣小组研究浓硫酸的氧化性的结论并进行了实验验证:
①一般认为1:1的硫酸浓度大于60%,就具有一定的氧化性,越浓氧化性越强,60%以下的H2SO4氧化性就不怎么强了。
②温度也影响氧化性,如铜放于冷的浓硫酸中反应不明显,如果加热就可以观察到明显现象。
③98%的浓硫酸物质的量浓度为18.4mol·L-1,密度为1.84g·cm-3
据以上信息回答:
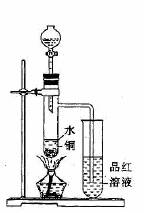 (1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓硫酸10-15滴(约0.5mL),加热至沸腾,该试管中液体是否有有明显变化______
___。试用数据解释原因__________________________________________。
(1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓硫酸10-15滴(约0.5mL),加热至沸腾,该试管中液体是否有有明显变化______
___。试用数据解释原因__________________________________________。
(2)甲同学再用分液漏斗加浓硫酸10mL再加热至沸腾,现象是____________________________________________________。
(3)乙同学利用所示装置直接从分液漏斗中加浓硫酸10mL与铜片反应。所观察到与甲不同的现象是 __________________原因是__________________________________。为了最终看到与甲类似的现象,乙同学需进行的操作是___________________。
(4)乙同学进行加热,还在带支管的试管中观察到有黑色物质出现,大胆假设此物质是_______________。
2.学习了元素周期律后,同学们对第四周期过渡元素氧化物产生了浓厚的兴趣。是否只有二氧化锰能催化氯酸钾受热分解?氧化铁、氧化铜、氧化铬等对氯酸钾的受热分解有没有催化作用?对此他们进行了实验探究。请你根据要求完成下列部分实验报告。
I 课题名称:____________________________________________________________
II实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、________、________、________等。
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
III 实验步骤:略
IV 实验数据:
|
实验 编号 |
KClO3(g) |
氧化物 |
产生气体(mL) |
耗时(s) |
||
|
化学式 |
质量(g) |
回收 |
(已折算到标况) |
|||
|
1 |
0.60 |
- |
- |
- |
10 |
480 |
|
2 |
0.60 |
MnO2 |
0.20 |
90% |
67.2 |
36.5 |
|
3 |
0.60 |
CuO |
0.20 |
90% |
67.2 |
79.5 |
|
4 |
0.60 |
Fe2O3 |
0.20 |
90% |
67.2 |
34.7 |
|
5 |
0.60 |
Cr2O3 |
0.20 |
异常 |
67.2 |
188.3 |
V 实验讨论:
(1)在氧化物的回收过程中,要进行过滤操作,所用的玻璃仪器是玻璃棒、_________、________
(2)实验编号3的实验中KClO3的分解率为_________%(保留一位小数)
(3)在用Cr2O3 做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色。该刺激性气体是________(填分子式),可用______________试纸检验。上述异常现象产生的原因是___________________________________。
VI 实验结论:_____________________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com