
8.所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,根据下列四种金属的熔沸点:
|
|
Na |
Cu |
Al |
Fe |
|
熔点(0C) |
97.5 |
1083 |
660 |
1535 |
|
沸点(0C) |
883 |
2595 |
2200 |
3000 |
其中不能形成合金的是 ( )
A.Cu和Al B.Fe和Cu
C.Fe和Na D.Al和Na
7.下列与实验相关的叙述正确的是 ( )
A.稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B.FeCl3溶液中混有少量CuCl2杂质,可以加入适量铁粉除杂
C.检验某溶液是否含有Fe2+时,应取少量该溶液,依次加入氯水、KSCN溶液
D.从碘水中提取碘时,不能用无水乙醇代替四氯化碳
6.常温下,下列各组离子在给定条件下一定能大量共存的是 ( )
A.在pH=0的溶液中:I-、Ca2+、NO3-、NH4+
B.存在大量Fe3+的溶液中:SCN-、Na+、SO42-、Cl-
C.存在大量Al3+的溶液中:AlO2-、Na+、SO42-、Cl-
D.在c(OH-)=1.0ⅹ10-3 mol·L-1的溶液中:Na+、S2-、AlO2-、SO32-
5.用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.常温常压下,22.4LCO2中含有NA个CO2分子
B.标准状况下,1molZn与含2molH2SO4的浓硫酸充分反应,生成气体分子数为NA
C.0.1mol/L的氯化铝溶液中含有的氯离子数为0.3NA
D.标准状况下,2.24L四氯化碳中含有C-Cl键数为0.4NA
4.化学在生产和日常生活中有着重要的应用。下列说法不正确的是 ( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.工业上可用铝热反应大规模炼铁
C.刚玉的主要成分是Al2O3,硬度大
D.电解熔融MgCl2,可制得金属镁
3.下列实验设计及其对应的离子方程式均正确的是 ( )
A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ = Cu2+ + 2Fe2+
B.F2与H2O反应制备O2 :F2 + 2H2O = 2H+ +2 F-+ O2↑
C.将氯气溶于水配置氯水:Cl2 + H2O = 2H+ + Cl- + ClO-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO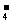 +
6H+ + 5H2O2 = 2Mn2+
+ 5O2↑ + 8H2O
+
6H+ + 5H2O2 = 2Mn2+
+ 5O2↑ + 8H2O
2.下列叙述中正确的是 ( )
A.稀有气体的晶体中不存在分子间作用力
B.次氯酸分子的结构式为H-O-Cl
C.Na2O和Na2O2所含化学键类型完全相同
D.Br2蒸气被木炭吸附时共价键被破坏
1.化学与生活、社会密切相关。下列说法不正确的是 ( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.垃圾是放错地方的资源,应分类回收利用
12.在Fe(OH)3胶体中,逐滴加入HI稀溶液,会出现一系列变化。先出现红褐色沉淀,原因是____________ 。
(2)随后沉淀溶解,溶液呈黄色,写出此反应的离子方程式____________ 。
(3)最后溶液颜色加深,原因是____________,此反应的离子方程式是____________ 。
(4)若用稀盐酸代替HI稀溶液,能出现上述哪些相同的变化现象?____________。(写序号)
11.请按要求回答下列问题。
(1)请分别写出中学所学常见的强酸和强碱(各不少于3种)
强酸:____________ 。
强碱:____________ 。
(2)请写出中学所学常见的强氧化剂,其中属于单质的有____________(不少于3种);属于化合物的有____________________(不少于4种)。
(3)请观察分析下列各组物质,指出各组物质具有的共同化学性质,每组各举一例,用化学方程式或离子方程式说明:
①H2SO4,H2SO3,H2S,SO2,CO2,Cl2,NH4Cl,FeCl3
共性____________ ;
举例____________ 。
②NaOH,Na2O,CaO,Na,Fe,Na2CO3,Na2S,Na2SO3
共性____________ ;
举例____________ 。
③Al,Al2O3,Al(OH)3,NaHCO3,NaHSO23,NaHS,(NH4)2S
共性____________ ;
举例____________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com