
7.下列各组物质中,按熔点由低到高排列正确的是
A.O2、 I2、 Hg B.CO2、 KCl、 SiO2
C.H2S 、H2As、H2O D.SiC、 NaCl 、 SO2
6. 金属具有延展性的原因
A.金属原子半径都比较大,价电子较少
B.自由电子受外力作用时能迅速传递能量
C.金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈的作用
D.金属受外力作用变形时,金属阳离子与自由电子间强烈的作用被破坏
5. 下列关于只含非金属元素的化合物的说法中,正确的是
A.一定是共价化合物 B.其晶体有可能是离子晶体
C.其晶体不可能是离子晶体 D.其晶体不可能是原子晶体
4. 下列分子中,所有原子都满足最外层8电子结构的是
A.乙炔 B.三氟化硼 C.五氯化磷 D.二硫化碳
3. 下列物质中含有离子键的是
A.氯化铝 B.乙醇 C.硫酸 D.苛性钠
2. 下列各组中的两种固态物质熔化(或升华)时,克服的微粒间相互作用力属于同种类型的是
A.碘和氯化钾 B.金刚石和重晶石
C.二氧化硅和干冰 D.软脂酸甘油酯和冰醋酸
1. 在单质的晶体中,一定不存在
A.离子键 B.分子间作用力
C.共价键 D.金属离子与自由电子间的作用
20.(8分)制造普通玻璃的原料是纯碱(Na2CO3)、石灰石(CaCO3)和石英(SiO2),这种玻璃的成分可以认为是由Na2O、CaO和SiO2所组成的混合物,而钾玻璃是将原料中的Na2CO3由K2CO3替代而制得的。今测得某钾玻璃中各成分的质量分数为:18.4%的K2O、11.0%的CaO和70.6%的SiO2。求生产制取这种钾玻璃的原料的物质的量之比是多少?
19.(8分)用地壳中某主要元素生产的多种产品在现代高科技中占有重要位置,足见化学对现代物质文明的重要作用。例如:
(1)计算机芯片的主要成分是 ;
(2)光导纤维的主要成分是 :
(3)目前应用最多的太阳能电池的光电转化材料是 ;
(4)用作吸附剂、干燥剂、催化剂或催化剂载体的人造分子筛大多是一类称为 的化合物 ;
18.(14分)某学生兴趣小组想利用高岭土[其主要成分是Al2O3·2SiO2·2H2O]试验新型的净水剂。试验程序如下:
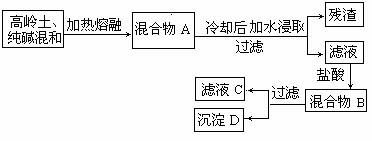
其中滤液E就是欲求的净水剂。试回答下列问题:
①写出混合物A、B,滤液C、D的主要成分
A: ;B: ;C: ;D: 。
②写出高岭土与纯碱熔融的两个化学方程式 ;
③该试验中,熔融高岭土可以选用的坩埚有
A.玻璃坩埚 B.瓷坩埚 C.氧化铝坩埚 D.铁坩埚
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com