
17.(14分)用下列10种物质的序号,填空回答问题
①N2 ②NH4NO3 ③Cl2 ④K2O2 ⑤Cu(OH)2
⑥CCl4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
|
由非极性键形成的非极性分子 |
|
|
由极性键形成的非极性分子 |
|
|
由极性键形成的极性分子 |
|
|
只有离子键形成的离子晶体是 |
|
|
既有离子键又有非极性键的离子晶体是 |
|
|
既有离子键又有极性键的离子晶体是 |
|
|
晶体中既有化学键,又有分子间作用力,还有氢键的是 |
|
16.据报道,科研人员应用电子计算机模拟出类似C60的物质N60,下列关于该物质的说法不正确的是
A.N60易溶于水 B.稳定性N60<N2
C.N60分子中每个氮原子与3个氮原子相连 D.熔点N60<N2
第II卷 非选择题
学号_____________姓名______________
15、据下列给出几种物质的熔点和沸点判断下列有关说法中错误的是
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCi4 |
单质B |
|
熔点 |
810℃ |
710℃ |
190℃ |
-68℃ |
2300℃ |
|
沸点 |
1465℃ |
1418℃ |
182.7℃ |
57℃ |
2500℃ |
A.SiCl4是分子晶体 B.单质B是原子晶体
C.AlCl3加热能升华 D.MgCl2所含离子键 的强度比NaCl大
14、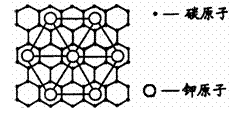 石墨能与熔融金属钾作用,形成石墨间隙化合物,
石墨能与熔融金属钾作用,形成石墨间隙化合物,
K原子填充在石墨各层面料原子中。比较常见的
石墨间隙化合物是青铜色的化合物,其化学式可
写作CxK,其平面图形见右图,则x值为
A.8 B.12 C.24 D.60
13、下列说法正确的是
A.极性分子可能是离子化合物,也可能是共价化合物。
B.晶体中只要有阳离子,就一定有阴离子,只要有阴离子,也一定有阳离子
C.在熔化状态和水溶液中均不能导电的化合物称为非电解质
D.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
12.(07南通一模)下列有关晶体的说法正确的是
A.金属晶体是由金属离子间的相互作用形成的
B.冰熔化时,水分子中的共价键发生断裂
C.白磷为分子晶体,分子结构为正四面体,其键角为109°28′
D.固体不导电,但熔融状态下和溶于水能导电不可能是分子晶体的性质
11.KO2的晶体结构和NaCl 相似,可以看作是Na+的位置用K+代替,Cl-的位置用O2-代替,下列对KO2的晶体结构的描述错误的是
A.和K+距离相同且最近的O2-共有8个
B.和K+距离相同且最近的K+共有12个
C.和K+距离相同且最近的O2-构成的多面体是正八面体
D.和K+距离相同且最近的O2-构成的多面体是正六面体
10.短周期的三种元素X、Y、Z位于同一周期,它们的最高价氧化物的水化物分别为HXO4、H2YO4、H3ZO4,下列判断中不正确的是
A.元素的非金属性:X>Y>Z B.阴离子的还原性:X<Y<Z
C.气态氢化物的稳定性:X>Y>Z D.最高价氧化物的水化物的酸性:Z>Y>X
9.(07年无锡市二模)我国科学家成功地研制出一种长期依赖进口、价格昂贵的物质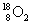 。下列说法正确的是
。下列说法正确的是
A.它是O3的一种同素异形体 B.它是 的同分异构体
的同分异构体
C.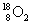 与
与 互为同位素 D.1mol
互为同位素 D.1mol 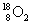 分子中含有20mol电子
分子中含有20mol电子
8.下列关于NaHSO4的说法中正确的是
A.NaHSO4固体是离子晶体
B.NaHSO4晶体中阳离子和阴离子的个数是2:1
C.NaHSO4晶体熔化时破坏的是离子键和共价键
D.NaHSO4的水溶液中有两种阳离子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com