
3£Æ»Ù≈◊ŒÔœþ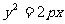 µƒΩ𵄔ÎÕ÷‘≤
µƒΩ𵄔ÎÕ÷‘≤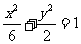 µƒ”“Ωπµ„÷ÿ∫œ£¨‘Ú µ ˝
µƒ”“Ωπµ„÷ÿ∫œ£¨‘Ú µ ˝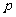 µƒ÷µ «°°°°°° £Æ
µƒ÷µ «°°°°°° £Æ
2£Æµ»≤Ó ˝¡–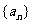 ÷–£¨π´≤Ó
÷–£¨π´≤Ó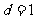 £¨
£¨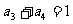 £¨‘Ú
£¨‘Ú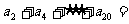 °°°°°°°°
£Æ
°°°°°°°°
£Æ
1£Æº∆À„£∫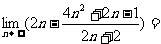 °°°°°°°°°°°°°°
£Æ
°°°°°°°°°°°°°°
£Æ
19£Æ(1)8°° 12°° °°(2)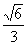 °° (3)
°° (3)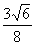
20¢≈Ω∏’ Ø°° ¢∆60°°°° (3)C60F60°° (4)ŒÂ‘™ª∑12°° ¡˘‘™ª∑25
18£Æ(l)Na‘≠◊”Ω·ππ æ“‚Õº°°°° N2∑÷◊”µƒµÁ◊” Ω
(2)O2∫ÕO3°° (3)H3O++OH-==2H2O
17°¢¢≈¢Ÿ¢€¢‚°° ¢∆¢Þ¢þ°° ¢«¢·°° ¢»¢ý°° ¢…¢Ð°° ¢ ¢⁄¢ð°° ¢À¢·
1£ÆA°° 2D°° 3D°°°° 4D°° 5B°° 6C°° 7BC°° 8AD°° 9A°° 10D°° 11AD°° 12D°° 13CD°° 14A°° 15D°° 16AD
20£Æ1996ƒÍ≈µ±¥∂˚ªØ—ßΩ± ⁄”Ë∂‘∑¢œ÷C60”–÷ÿ¥Ûπ±œ◊µƒ»˝Œªø∆—ߺ“°£C60∑÷◊” «–Œ»Á«Ú◊¥µƒ∂ý√ÊÃÂ(»Á”“Õº)£¨∏√Ω·ππµƒΩ®¡¢ª˘”⁄“‘œ¬øº¬«£∫
¢ŸC60∑÷◊”÷–√ø∏ˆÃº‘≠◊”÷ª∏˙œý¡⁄µƒ3∏ˆÃº‘≠◊”–Œ≥…ªØ—ߺ¸£ª
¢⁄C60∑÷◊”÷ª∫¨”–ŒÂ±þ–Œ∫Õ¡˘±þ–Œ£ª
¢€∂ý√Êõƒ∂•µ„ ˝°¢√Ê ˝∫Õ¿‚±þ ˝µƒπÿœµ£¨◊Ò—≠≈∑¿≠∂®¿Ì£∫∂•µ„ ˝ + √Ê ˝£≠¿‚±þ ˝ = 2°£æð…œÀ˘ ˆ£¨ø…Õ∆÷™C60∑÷◊””–12∏ˆŒÂ±þ–Œ∫Õ20∏ˆ¡˘±þ–Œ£¨C60∑÷◊”À˘∫¨µƒÀ´º¸ ˝Œ™30°£
«Îªÿ¥œ¬¡–Œ £∫
(1)πÃÃÂC60”ÎΩ∏’ Øœý±»Ωœ£¨»€µ„Ωœ∏þ’þ”¶ «°°°°°°°°°°°°°°°°
(2)Õ®π˝º∆À„£¨»∑∂®C60∑÷◊”À˘∫¨µ•º¸ ˝_______________°£
(3) ‘π¿º∆C60∏˙F2‘⁄“ª∂®Ãıº˛œ¬£¨∑¥”¶…˙≥…ªØ∫œŒÔø…ƒÐµƒªØ—ß Ω°°°°°°°°°°°°°°°°°°°°°°
(4)C70∑÷◊”“≤“—÷∆µ√£¨À¸µƒ∑÷◊”Ω·ππƒ£–Õø…“‘”ÎC60Õ¨—˘øº¬«∂¯Õ∆÷™°£Õ®π˝º∆À„(“™”–º∆À„π˝≥Ã)»∑∂®C70∑÷◊”÷–ŒÂ±þ–Œ∫Õ¡˘±þ–Œµƒ ˝ƒø°£
19£Æ(16∑÷) 1 183 K“‘œ¬¥øÃ˙æßõƒª˘±æΩ·π𵕑™»ÁÕº1À˘ 棨1183 K“‘…œ◊™±‰Œ™Õº2À˘ æΩ·π𵃪˘±æΩ·π𵕑™£¨‘⁄¡Ω÷÷æßÃÂ÷–◊Ó¡⁄Ω¸µƒÃ˙‘≠◊”º‰æý¿ÎœýÕ¨°£
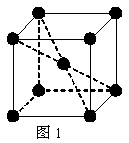 °°°°°°°°
°°°°°°°° 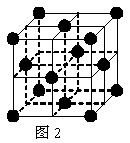
(1)‘⁄1 183 K“‘œ¬µƒ¥øÃ˙æßÃÂ÷–£¨”ÎÃ˙‘≠◊”µ»æý¿Î«“◊ÓΩ¸µƒÃ˙‘≠◊” ˝Œ™_______∏ˆ£ª‘⁄1 183 K“‘…œµƒ¥øÃ˙æßÃÂ÷–£¨”ÎÃ˙‘≠◊”µ»æý¿Î«“◊ÓΩ¸µƒÃ˙‘≠◊” ˝Œ™___________£ª
(2)¥øÃ˙æßÑ⁄æß–Õ◊™±‰«∞∫Û£¨∂˛’þª˘±æΩ·π𵕑™µƒ±þ≥§÷Ʊ»Œ™(1 183 K“‘œ¬”Î1 183 K“‘…œ÷Ʊ»)___________°£
(3)◊™±‰Œ¬∂»«∞∫Û¡Ω’þµƒ√Ð∂»±»(1 183 K“‘œ¬”Î1 183 K“‘…œ÷Ʊ»)_____________°£
18£Æ(10∑÷) œ÷”–A°¢B°¢C°¢DÀƒ÷÷∂Ã÷Ð∆⁄‘™Àÿ£¨A‘™Àÿµƒ‘≠◊”∞Îæ∂ «≥˝œ°”–∆¯ÃÂÕ‚∞Îæ∂◊Ó¥Ûµƒ£¨B‘™Àÿµƒ‘≠◊”◊ÓÕ‚≤„±»¥ŒÕ‚≤„∂ý3∏ˆµÁ◊”£¨C‘™Àÿ «»ÀÃÂ÷–÷ ¡ø∑÷ ˝◊Ó¥Ûµƒ£¨D‘™Àÿµƒ“ª÷÷∫ÀÀÿ÷ ¡ø ˝”Î÷ ◊” ˝œýµ»°£«Îæð¥ÀÃÓø’£∫
(1)Aµƒ‘≠◊”Ω·ππ æ“‚Õº «°°°°°°°°°°°°°° £ªB2∑÷◊”µƒµÁ◊” Ω «°°°°°°°°°°°°°° °£
(2)C‘™Àÿ‘⁄◊‘»ªΩÁ÷–µ•÷ µƒªØ—ß ΩŒ™°°°°°°°° °¢°°°°°°°° °£
(3)C∫ÕDø…–Œ≥…µÁ◊” ˝œýÕ¨µƒ¡Ω÷÷¡£◊”£¨∏√¡Ω÷÷¡£◊”∑¥”¶∫Û…˙≥…“ª÷÷÷––‘∑÷◊”(’‚»˝÷÷Œ¢¡£µƒµÁ◊” ˝æ˘œýµ»)£¨∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com